
Атомы элементов P в первой реакции и O во второй реакции (а также и вещества, в состав которых они входят PH3 в первой реакции и KClO3 во второй реакции) являются восстановителями (отдают электроны) и участвуют в процессе окисления (процессе отдачи электронов
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Для реакций:
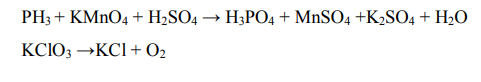
Составьте уравнения методом электронного баланса. Для каждой реакции укажите, какое вещество является окислителем, а какое – восстановителем и за счет каких атомов. Определите типы данных окислительно-восстановительных реакций.
Решение
Окислительно-восстановительные реакции характеризуются переходом электронов от одного вещества (восстановителя) к другому (окислителю). Для ответов на вопросы задачи вычислим степени окисления атомов, входящих в состав приведенных в уравнении реакции веществ, руководствуясь следующими правилами:
- степени окисления атомов в простых веществах (построенных из атомов одного и того же элемента) принимаются равными нулю;
- степень окисления атома водорода в соединениях с неметаллами равна +1;
- степень окисления атома кислорода в большинстве его соединениях равна -2 (к исключениям из правила относятся, например, пероксиды типа H2O2, в которых степень окисления атома О равна -1);
- степени окисления типичных металлов (I,II,III группы главные подгруппы периодической системы Д. И. Менделеева, кроме бора) в их соединениях постоянны и численно равны номеру группы, т.е. +1, +2, +3, соответственно;
- алгебраическая сумма степеней окисления атомов в молекуле равна нулю, в сложном ионе - заряду иона.
Запишем вычисленные степени окисления над символами элементов в уравнении реакции:
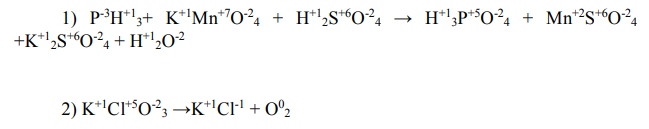
Для составления электронных уравнений выпишем атомы элементов, изменившие свои степени окисления, и укажем число электронов, отдаваемое или принимаемое атомами для осуществления такого изменения степеней окисления:

Атомы элементов P в первой реакции и O во второй реакции (а также и вещества, в состав которых они входят PH3 в первой реакции и KClO3 во второй реакции) являются восстановителями (отдают электроны) и участвуют в процессе окисления (процессе отдачи электронов).
Атомы элементов Mn в первой реакции и Cl во второй реакции (а также вещества, в состав которых они входят KMnO4 в первой реакции и KClO3 во второй реакции) являются окислителями (принимают электроны) и участвуют в процессах восстановления (процессе присоединения электронов):
Суммарное число электронов, отдаваемых в ходе реакции частицамивосстановителями, и суммарное число электронов, принимаемых в ходе реакции частицами-окислителями должны быть равны друг другу.
На этом основан один из методов расстановки коэффициентов в уравнениях окислительно-восстановительных реакций, называемый методом электронного баланса.
Для обеспечения указанного электронного равенства подберем множители к электронным уравнениям процессов окисления и восстановления, найдя наименьшее общее кратное для числа отданных и присоединенных электронов и поделив его на каждое из чисел.
Запишем полученные множители справа за чертой у каждого из уравнений:

Расстановку коэффициентов проведем в следующей последовательности:
- перенесем полученные в электронном балансе множители в левую и правую части уравнения реакции к формулам соответствующих веществ;
- уравняем атомы металлов;
- уравняем кислотные остатки;
- уравняем атомы водорода.
Итоговые коэффициенты в уравнениях данных реакций таковы:
Первая реакция:
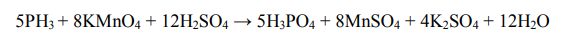
Вторая реакция:
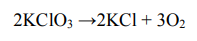
Для проверки их правильности просуммируем число атомов кислорода в левой и правой части уравнения: 80 = 80
6 = 6
Значит коэффициенты расставлены верно. Для определения типа рассматриваемой окислительновосстановительной реакции воспользуемся следующей классификацией:
- межмолекулярные окислительно-восстановительные реакции (атом-окислитель и атом-восстановитель входят в состав разных веществ);
- внутримолекулярные окислительно
-восстановительные реакции (атом-окислитель и атом-восстановитель входят в состав одного и того же вещества, являясь атомами разных элементов);
- реакции диспропорционирования (атом-окислитель и атомвосстановитель являются атомами одного и того же элемента в промежуточной степени окисления).
Рассматриваемые в задаче окислительно-восстановительные реакции относятся к типам:
Первая – межмолекулярная ОВР, т.к. (атом-окислитель и атомвосстановитель входят в состав разных веществ.
Вторая – внутримолекулярная ОВР, т.к. атом-окислитель и атомвосстановитель входят в состав одного и того же вещества, являясь атомами разных элементов.

Похожие готовые решения по химии:
- Катодный процесс заключается в восстановлении катионов, входящих в состав соли – электролита катода
- В чем различия в коррозии оцинкованного и луженого железа при нарушении целостности покрытий во влажной атмосфере? Приведите электронные уравнения анодного и катодного процессов в обоих случаях. Укажите продукты коррозии
- Как будет происходить электролиз водного раствора электролита NaCl (t = 25 мин, I = 8 А)? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях
- Следовательно, заряд ядра атома есть суммарный заряд его протонов (нейтроны заряда не несут), а массовое число – суммарная масса протонов и нейтронов
- Химическая реакция может быть охарактеризована скоростью ее протекания. Скорость химической реакции зависит от многих факторов, среди которых
- Как будет происходить электролиз водного раствора электролита Hg(NO3)2 (t = 1 ч 35 мин, I = 15 А)? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях
- Укажите соответствие между положением элемента в периодической системе Д.И. Менделеева и его электронной формулой (номером внешнего энергетического уровня, общим числом валентных электронов, характером их распределения по энергетическим подуровням
- Электроотрицательность (EN) характеризует способность атомов элементов к смещению электронной плотности. В периоде системы элементов Д. И. Менделеева она возрастает слева направо, в подгруппе убывает сверху вниз (для s- и p-элементов
- Электроотрицательность (EN) характеризует способность атомов элементов к смещению электронной плотности. В периоде системы элементов Д. И. Менделеева она возрастает слева направо, в подгруппе убывает сверху вниз (для s- и p-элементов
- Укажите соответствие между положением элемента в периодической системе Д.И. Менделеева и его электронной формулой (номером внешнего энергетического уровня, общим числом валентных электронов, характером их распределения по энергетическим подуровням
- В чем различия в коррозии оцинкованного и луженого железа при нарушении целостности покрытий во влажной атмосфере? Приведите электронные уравнения анодного и катодного процессов в обоих случаях. Укажите продукты коррозии
- Катодный процесс заключается в восстановлении катионов, входящих в состав соли – электролита катода

