
Чем отличается истинное химическое равновесие от ложного? Привести примеры истинных и ложных равновесий
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Чем отличается истинное химическое равновесие от ложного? Привести примеры истинных и ложных равновесий. Записать выражение для расчета константы равновесия через равновесные концентрации и равновесные парциальные давления газов для обратимых реакций:
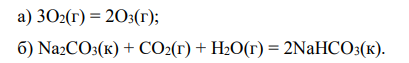
Ответ:
Истинное равновесие – это равновесие, которое характеризуется тремя признаками: - при отсутствии внешних воздействий оно остается постоянным по времени; - при изменении внешних воздействий (Р, Т, с …) состояние системы изменяется, но при восстановлении сходных условий оно восстанавливается; - к состоянию истинного равновесия можно подойти с двух сторон (со стороны продуктов реакции и со стороны исходных веществ). Пример истинного равновесия: синтез аммиака из азота и кислорода. 238 Ложное равновесие – это неизменное во времени состояние системы, которое при изменении внешних условий начинает необратимо изменяться. Например: взаимодействие железа с кислородом. Таким образом, от этого истинного равновесия следует отличать ложное, когда изменений нет потому, что не идут ни прямой, ни обратный процесс из-за кинетических затруднений. Если изменить условия так, что реакции ускорятся (например, нагреть или ввести катализатор), то система необратимо перейдет из ложного равновесия в истинное, и если потом вернуть ее в прежние условия, то прежнее состояние не вернется
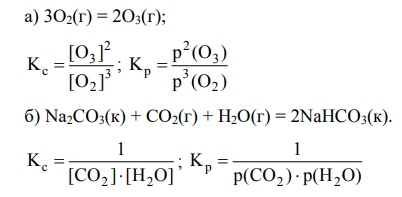

Похожие готовые решения по химии:
- Какая эта реакция – простая или сложная? Как изменяется ее скорость при увеличении концентрации в 4 раза: а) только водорода; б) только брома; в) водорода и брома одновременно
- Молярная концентрация NH3 в концентрированном растворе аммиака, полученном при 15 С, равна 18. Какой объем NH3, измеренный при н.у., затрачивается на приготовление 1 л такого раствора
- Раствор электролита с концентрацией 0,04 моль/л имеет осмотическое давление при 0 С, равное 217,8 кПа. Степень диссоциации растворенного вещества равна 70 %. Определить, на сколько ионов диссоциирует растворенное вещество и привести примеры таких веществ
- Написать уравнения гидролиза и выражения для констант гидролиза солей: KClO, K2S, AlCl3
- Перечислить основные типы гибридизации с участием s-, p- и dорбиталей, указать геометрическую форму частиц (когда все гибридные орбитали связывающие), привести примеры
- Если сравнить температуру кипения галогеноводородов HF (+19,5 °С), НCl (–85,1 °С), HBr (–66,8 °С), НI (–35,4 °C), то видна аномалия в поведении фтороводорода. Объяснить эту аномалию
- Не проводя расчетов, предсказать знак изменения энтропии при протекании реакций
- Разложение нитрата аммония при нагревании возможно по двум направлениям
- Имеются следующие данные о выполнении задания по товарообороту обувного магазина: фактический товарооборот 25000 тыс. руб., выполнение задания составило 103,5%. Определить задание
- Определить сумму ежегодных амортизационных отчислений способом уменьшаемого остатка при ликвидационной
- Определить сумму ежегодных амортизационных отчислений способом списания стоимости по сумме
- Определите изменение реальной заработной платы, если фонд заработной платы на предприятии увеличился с 2,5 млн. руб. до

