
Дайте характеристику гемоглобина и миоглобина. Напишите структурную формулу гема, поясните, из чего он состоит
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16962 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Дайте характеристику гемоглобина и миоглобина. Напишите структурную формулу гема, поясните, из чего он состоит. Опишите химическую природу гемоглобина. Опишите химическую природу гемоглобина и его производных.
Ответ:
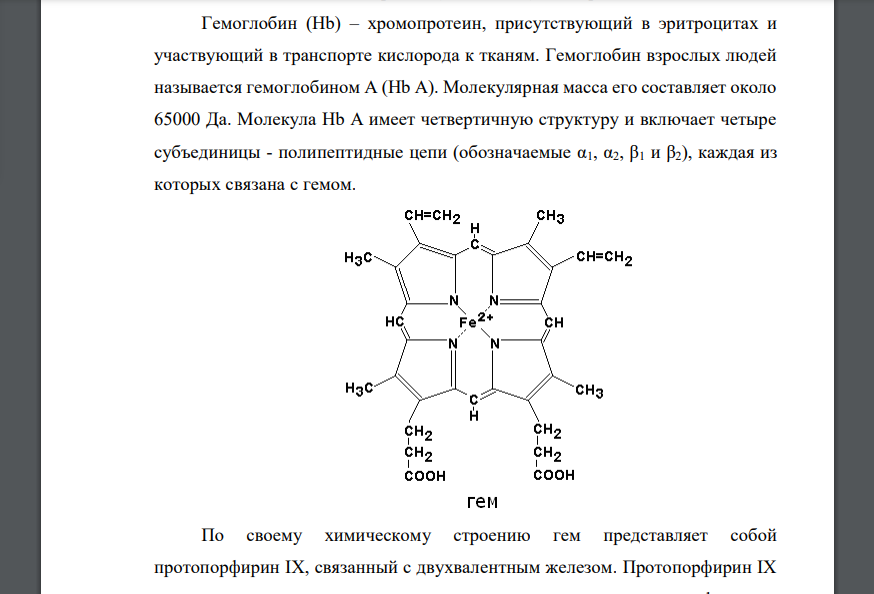
Миоглобин – хромопротеин, присутствующий в мышечной ткани и обладающий большим сродством к кислороду. Молекулярная масса этого белка около 16000 Да. Молекула миоглобина имеет третичную структуру и представляет собой одну полипептидную цепь, соединённую с гемом. Миоглобин не обладает аллостерическими свойствами, кривая насыщения его 191 кислородом имеет вид гиперболы. Функция миоглобина заключается в создании в мышцах кислородного резерва, который расходуется по мере необходимости, восполняя временную нехватку кислорода. Гемоглобин (Hb) – хромопротеин, присутствующий в эритроцитах и участвующий в транспорте кислорода к тканям. Гемоглобин взрослых людей называется гемоглобином А (Hb A). Молекулярная масса его составляет около 65000 Да. Молекула Hb А имеет четвертичную структуру и включает четыре субъединицы - полипептидные цепи (обозначаемые α1, α2, β1 и β2), каждая из которых связана с гемом. По своему химическому строению гем представляет собой протопорфирин IX, связанный с двухвалентным железом. Протопорфирин IX - органическое соединение, относящееся к классу порфиринов. Протопорфирин IX содержит четыре замещённых пиррольных кольца, соединённых метиновыми мостиками =СН-. Заместителями в пиррольных кольцах являются: четыре метильные группы СН3-, две винильные группы СН2=СН- и два остатка пропионовой кислоты -СН2-СН2-СООН. Гем соединяется с белковой частью следующим образом. Неполярные группы протопорфирина IX взаимодействуют с гидрофобными участками аминокислот при помощи гидрофобных связей. Кроме того, имеется координационная связь между атомом железа и имидазольным радикалом 192 гистидина в белковой цепи. Ещё одна координационная связь атома железа может использоваться для связывания кислорода и других лигандов


Похожие готовые решения по химии:
- Напишите химическую природу и охарактеризуйте пищевые источники, признаки авитаминоза и коферментные функции
- Напишите химические формулы гормонов коркового слоя надпочечников: кортизона, кортикостерона. Охарактеризуйте
- Напишите, как активируются пепсиноген, трипсиноген, химотрипсиноген и желудочно-кишечном
- Объясните, что такое обратимые и необратимые, экзергонические и эндергонические реакции. Приведите примеры
- В УФ-спектрах 4-диметиламинобензойной кислоты, снятых в этаноле, присутствует полоса поглощения с максимумом
- Охарактеризуйте компоненты клеточных мембран (липиды, холестерин, белки), структурную организацию биомембран и их функции
- Напишите формулы продуктов полного гидролиза рибонуклеиновой кислоты и назовите их
- Охарактеризуйте состав и строение гепарина и его использование в медицине. Ответ
- Что понимают под термином «скорость химической реакции»? От каких факторов она зависит
- Охарактеризуйте состав и строение гепарина и его использование в медицине. Ответ
- Выведите уравнение для периода полупревращения исходных веществ для реакции второго порядка, если начальные концентрации
- Напишите химическую природу и охарактеризуйте пищевые источники, признаки авитаминоза и коферментные функции

