
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Дайте обоснование реакциям подлинности фенола, приведенным в ФС Напишите их химизм и укажите внешний эффект
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16951 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
Дайте обоснование реакциям подлинности фенола, приведенным в ФС. (Приложение № 3). Напишите их химизм и укажите внешний эффект. Ответ: В соответствии с ФС. Для установления подлинности фенола используют две качественные реакции: 1. Реакция комплексообразования с ионами железа (III) Основана на свойствах фенольного гидроксила молекулы фенола образовывать растворимые комплексные соединения, окрашенные в фиолетовый цвет.
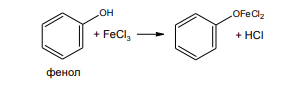
При избытке фенола:
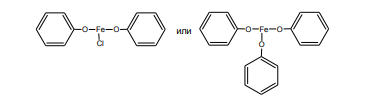
2. Реакция бромирования ароматического кольца Основана на электрофильном замещении водорода в о- и п- положениях на бром с образованием нерастворимого бромпроизводного (белый или светло-желтый осадок).
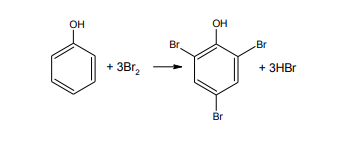
Похожие готовые решения по химии:
- Дайте обоснование определению примеси сульфатов в сульфадиметоксине в соответствии с требованиями ФС (Приложения № 3, 7)
- Дайте обоснование испытанию субстанции по показателю «Прозрачность», если ФС ГФ XIII издания предъявляет требование «раствор должен быть прозрачным»
- Обоснуйте определение норсульфазола во фталазоле по методике: 1 г фталазола взбалтывают с 10 мл разведенной хлористоводородной кислоты
- Дайте оценку качества субстанции ацетилсалициловой кислоты по количественному содержанию согласно требованию ФС
- Порог коагуляции золя гидроксида алюминия дихромат-ионами равен 0,63 ммоль/л. Какой объем 10%-ного раствора дихромата калия (плотность 1,07 г/мл) требуется для коагуляции
- В таблице 1 приведена зависимость концентрации реагентов С от времени t. В реакциях, в которых участвуют
- По значения констант скоростей реакции при двух температурах определите: 1) температурный коэффициент
- Определите структурную формулу углеводорода состава С8Н8, если известно, что он обесцвечивает
- Энергия активации реакции равна 10 кДж/моль. Во сколько раз изменится скорость реакции при повышении температуры
- Определите анодные и катодные участки. При необходимости подберите нужный металл согласно заданию Медное изделие + катодное покрытие
- Укажите характер связей в молекуле, для чего изобразите графическую формулу указанного соединения и рассчитайте H2CO3 GaCl3 [Cr(H2O)6]Cl3
- Найти константу равновесия реакции N2О4↔2NО2, если начальная концентрация N2О4 составляла 0,08 моль/л, а к моменту наступления равновесия

