
Даны электроды (см. вариант в табл. 14). 1. Подберите электролиты и обозначьте гальванический элемент,
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16813 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
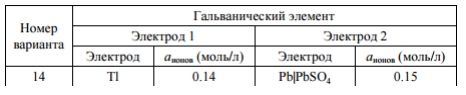
Даны электроды (см. вариант в табл. 14). 1. Подберите электролиты и обозначьте гальванический элемент, составленный из ваших электродов. 2. Запишите уравнения электродных реакций и суммарную (токообразующую) реакцию в гальваническом элементе. 3. Рассчитайте равновесные потенциалы для данных электродов (парциальное давление газа для газовых электродов во всех случаях равно 101 кПа). 4. Рассчитайте напряжение гальванического элемента.
Решение:
1. Схема гальванического элемента: 2. Уравнения электродных реакций: Рассчитаем электродные потенциалы электродов по уравнению Нернста: Напряжение гальванического элемента:

Похожие готовые решения по химии:
- Электролиз водных растворов 1. Для вашего варианта запишите катодную, анодную и суммарную
- Удельная электропроводность насыщенного водного раствора сульфата бария при 25 0С равна 4,31∙10-4 См/м. Его эквивалентная
- Оцените значение параметра а в уравнении второго приближения теории Дебая-Хюккеля по зависимости среднего ионного
- Найдите значение растворимости сульфата серебра при 298 К: а) в воде; б) в 0,01 М растворе нитрата натрия, если ПР = 1,58∙10-5 .
- Сколько литров кислорода расходуется при сжигании 100 г спирта:
- Для элемента задана электронная формула внешнего слоя
- Рассчитайте изменение скорости прямой реакции при одновременном изменении условий реакции (вариант в табл.). Если
- Даны уравнения реакций и концентрации веществ. Обозначения:с0 – исходная концентрация, [ ] – равновесная концентрация,
- При анализе методом газовой хроматографии смеси толуола (I), этилбензола (2), ксилола (3), стирола (4) к анализируемой пробе массой 2,034 г добавлено 0,4168 г н-октана в качестве внутреннего стандарта
- При электролизе 15 3 см раствора нитрата свинца на аноде выделилось 0,2564 г PbO2 . Определить молярную концентрацию исходного раствора.
- Рассчитать степень извлечения ионов цинка из 200 мл 0,1 Н раствора сульфата цинка катионитом, если на титрование выделенной из катионита в Н+ - форме кислоты израсходовано 18 мл 0,098 М раствора гидро
- Электролиз водных растворов 1. Для вашего варианта запишите катодную, анодную и суммарную

