
Дать названия, привести определения и обозначения величин, которые применяются для количественной характеристики процесса электролитической диссоциации. Какая из них является постоянной величиной при различных концентрациях раствора
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Дать названия, привести определения и обозначения величин, которые применяются для количественной характеристики процесса электролитической диссоциации. Какая из них является постоянной величиной при различных концентрациях раствора?
Ответ:
Количественные характеристики процесса диссоциации. 1) Степень диссоциации (α, %) – это отношение числа молекул электролита, которые продиссоцировали (Nдис.), к общему числу растворенных молекул электролита (N). 100% 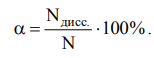
2) Константа диссоциации (Кдис) – это отношение произведения концентрации ионов в растворе электролита к концентрации неразрушенных молекул. Константа равновесия, отвечающая диссоциации слабого электролита, называется константой диссоциации. Величина Кдис зависит от природы электролита и растворителя, а также от температуры, но не зависит от концентрации раствора. Она характеризует способность данной кислоты или данного основания распадаться на ионы: чем выше Кдис, тем легче электролит диссоциирует.
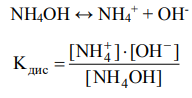

Похожие готовые решения по химии:
- Произведение растворимости гидроксида цинка равно 4,0·10-16 . Чему равны концентрации ионов Zn2+ и OHв насыщенном растворе этого вещества
- Для каких солей гидролиз проходит ступенями? Чем определяется их число и как изменяется полнота гидролиза от первой ступени к последней? Привести примеры солей, гидролиз которых проходит в две и три ступени, написать уравнения их гидролиза
- Для данного гальванического элемента написать схемы электродных процессов и уравнение токообразующей реакции в общем виде (ионном и молекулярном), вычислить ЭДС при указанных концентрациях и температуре
- В чем сущность протекторной защиты железа в электролите, содержащем растворенный кислород. Составьте электронные уравнения анодного и катодного процессов. Приведите схемы гальванических элементов с протекторной защитой и без
- Какое количество и какая масса алюминия, какое количество и какой объем кислорода (при н. у.) участвовали в реакции, в ходе которой выделилось 838 кДж тепла
- Определить расчетами возможность или невозможность самопроизвольного протекания в изолированной и неизолированной системах при стандартных условиях реакций
- При состоянии равновесия реакции: N2(г) + 3H2(г) ↔ 2NH3(г) равновесные концентрации азота, водорода и аммиака равны 3, 9 и 4 моль/л
- Оксид азота (II) и водород при 1000 К взаимодействуют по уравнению: 2H2 + 2NO = N2 + 2H2O. Опытные данные по влиянию концентрации реагирующих веществ на скорость реакции следующие
- Рассчитать структуру цеховой себестоимости годового выпуска и 1000 штук изделий, оптовую цену 1000
- Оксид азота (II) и водород при 1000 К взаимодействуют по уравнению: 2H2 + 2NO = N2 + 2H2O. Опытные данные по влиянию концентрации реагирующих веществ на скорость реакции следующие
- На производственном участке работали три лазерные установки, с 1-го июля вступили в строй и начали производить
- На предприятии плановый выпуск изделий составляет 8000 единиц, производственная себестоимость

