
Для данной окислительно-восстановительной реакции определить её тип; указать восстановитель и окислитель; подобрать коэффициенты методом электронного баланса; рассчитать эквивалентные массы окислителя и восстановителя
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Для данной окислительно-восстановительной реакции определить её тип; указать восстановитель и окислитель; подобрать коэффициенты методом электронного баланса; рассчитать эквивалентные массы окислителя и восстановителя
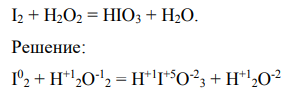
Вычисляем, как изменяют свою степень окисления восстановитель и окислитель, и отражаем это в уравнениях.
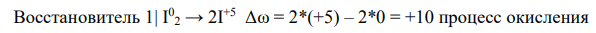
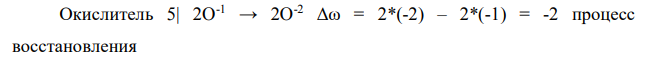
Наименьшее общее кратное равно 10. Коэффициент перед восстановителем равен 10/10 = 1, коэффициент перед окислителем равен 10/2 = 5.
Получаем уравнение окислительно-восстановительной реакции:
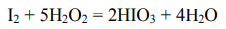
Тип реакция – межмолекулярная окислительно-восстановительная реакция. В этой реакции показатель эквивалентности (Z) восстановителя равен 10, а его эквивалентная масса равна
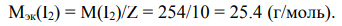
Показатель эквивалентности окислителя равен 2, а его эквивалентная масса равна
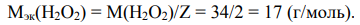

Похожие готовые решения по химии:
- Объясните, почему изменяется длина связи между атомами углерода в молекулах С2Н6 (0,154 нм), С2Н4 (0,135 нм), С2Н2 (0,120 нм
- Используя метод МО, объяснить, почему ионизационные потенциалы атомов кислорода (13,6 эВ) и фтора (17,4 эВ) выше, чем молекул O2 (12,2 эВ) и F2 (15,8 эВ
- Перечислить основные типы гибридизации с участием s-, p- и dорбиталей, указать геометрическую форму частиц (когда все гибридные орбитали связывающие), привести примеры
- Если сравнить температуру кипения галогеноводородов HF (+19,5 °С), НCl (–85,1 °С), HBr (–66,8 °С), НI (–35,4 °C), то видна аномалия в поведении фтороводорода. Объяснить эту аномалию
- Вычислить pH раствора и концентрацию ионов H+ , если при T=298 К известна эдс элемента (табл. 15). Стандартный электродный потенциал хингидронного электрода 0,699 В, каломельного - 0,337 В, хлоридсеребряного - 0,284
- Вычислить активность ионов металла по величине ЭДС концентрационной цепи при T=298 К, если активность иона в одном из электродов
- Массовая доля кислорода в оксиде четырехвалентного металла составляет 40,05 %. Вычислите эквивалентную и атомную массы металла, найти его в периодической системе, написать формулу оксида
- Среди гидроксидов Са(ОН)2, Fe(OH)2, Sn(OH)2 найти амфотерный и показать его амфотерность уравнениями реакций
- Среди гидроксидов Са(ОН)2, Fe(OH)2, Sn(OH)2 найти амфотерный и показать его амфотерность уравнениями реакций
- Массовая доля кислорода в оксиде четырехвалентного металла составляет 40,05 %. Вычислите эквивалентную и атомную массы металла, найти его в периодической системе, написать формулу оксида
- Используя метод МО, объяснить, почему ионизационные потенциалы атомов кислорода (13,6 эВ) и фтора (17,4 эВ) выше, чем молекул O2 (12,2 эВ) и F2 (15,8 эВ
- Объясните, почему изменяется длина связи между атомами углерода в молекулах С2Н6 (0,154 нм), С2Н4 (0,135 нм), С2Н2 (0,120 нм

