
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Для гальванического элемента, составленного из электродов Pt|A, B и Pt|C, Д, при активностях ионов А, В, С, Д, приведенных в таблице
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16707 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
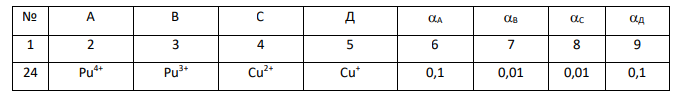
Для гальванического элемента, составленного из электродов Pt|A, B и Pt|C, Д, при активностях ионов А, В, С, Д, приведенных в таблице 11 и таблице 3 приложения, при Т = 298 К необходимо: 1. Вычислить электродные потенциалы по уравнению Нернста. 2. Привести условную запись гальванического элемента, составленного из указанных электродов. 3. Вычислить ЭДС (Е) этого элемента. 79 4. Написать уравнение окислительно-восстановительной реакции, протекающей в гальваническом элементе при его работе. 5. Вычислить константу равновесия (Ка) этой реакции. Таблица 11 Исходные данные
Решение:
В первую очередь необходимо рассчитать потенциалы отдельных электродов по уравнению Нернста, которое при имеет вид: стандартный электродный потенциал; Z - число электронов, участвующих в элементарном акте электродной реакции. Для электродная реакция: электродная реакция: Электродвижущая сила гальванического элемента (Е) всегда положительная величина, поэтому она рассчитывается по формуле: Условная запись гальванического элемента: Уравнение реакции, протекающей при работе этого элемента, складывается как сумма уравнений электродных реакций. При уравнивании реакции необходимо помнить, что число отданных на одном электроде электронов должно равняться числу принятых на другом. Таким образом, Уравнение окислительно-восстановительной реакции:

Решение:
В первую очередь необходимо рассчитать потенциалы отдельных электродов по уравнению Нернста, которое при имеет вид: стандартный электродный потенциал; Z - число электронов, участвующих в элементарном акте электродной реакции. Для электродная реакция: электродная реакция: Электродвижущая сила гальванического элемента (Е) всегда положительная величина, поэтому она рассчитывается по формуле: Условная запись гальванического элемента: Уравнение реакции, протекающей при работе этого элемента, складывается как сумма уравнений электродных реакций. При уравнивании реакции необходимо помнить, что число отданных на одном электроде электронов должно равняться числу принятых на другом. Таким образом, Уравнение окислительно-восстановительной реакции:


Похожие готовые решения по химии:
- По экспериментальным данным адсорбции адсорбтива А на адсорбенте В, представленным в таблице 15, построить изотерму адсорбции
- Для гидрофобного золя вещества А, полученного при взаимодействии избытка вещества В с веществом С (см. таблицу 16), составить формулу мицеллы
- Порог коагуляции гидрозоля вещества А под действием электролита В равен К (см. таблицу 17). C помощью правила Шульце-Гарди для этого золя
- По данным вискозиметрических определений характеристической вязкости [] растворов ВМС и значениям констант К и уравнения
- В таблице 6 приведены кинетические параметры реакций: Еа -энергия активации, А - предэкспоненциальный множитель в уравнении
- По данным, приведенным в таблице 8, для водных растворов рассчитать величину, указанную в последнем столбце таблицы
- Смесь состоит из mA (г) компонента А и mВ (г) компонента В и находится при температуре t1 (С) (см. таблицу 9). Определить: а) температуру начала
- По данным, приведенным в таблице 10, для водных растворов слабых электролитов рассчитать величины, указанные в последнем
- В начальный момент времени t0=0 в образце находилось в n = 3 раза меньше ядер первого радиоактивного изотопа, чем ядер второго радиоактивного
- Однозарядный ион натрия прошел ускоряющую разность потенциалов 1 кВ и влетел перпендикулярно силовым линиям в однородное
- По экспериментальным данным адсорбции адсорбтива А на адсорбенте В, представленным в таблице 15, построить изотерму адсорбции
- В зоне проводимости меди, имеющей энергию Ферми Eф = 7,00 эВ и температуру, близкую к 0 К, треть свободных электронов имеет энергии в интервале 0 E E1 . Нижний

