
Электрохимическая схема - это условная запись, в которой представлена информация о аноде и катоде с указанием металлов, состава электролитов, а также особенностях конструкции данного гальванического элемента
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Составьте схему гальванического элемента, напишите электронные уравнения электродных процессов и суммарное уравнение соответствующей окислительно-восстановительной реакции. Вычислите концентрацию раствора электролита или ЭДС.
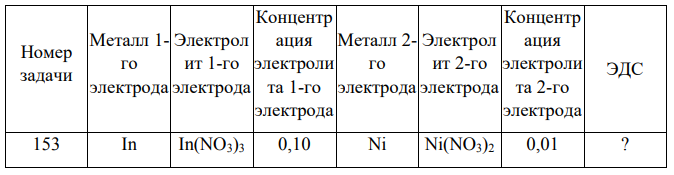
Решение
Гальванический элемент - это электрохимическая система, в которой энергия окислительно-восстановительной реакции трансформируется в электрическую энергию, т.е. такая система служит в качестве химического источника тока.
Анодный процесс заключается в окислении металла, характеризующегося более отрицательной величиной электродного потенциала Е0 , в катодном процессе участвует частица-окислитель, присутствующая в катодном электролите. Представлен концентрационный гальванический элементв.
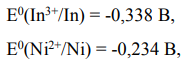
Электрод с меньшим равновесным потенциалом является анодом (In), с большим равновесным потенциалом – катодом (Ni).
Металл анода окисляется, что можно представить в виде электронного уравнения вида:

Катодный процесс заключается в восстановлении катионов, входящих в состав соли – электролита катода.
Соответствующее электронное уравнение имеет вид:

Электрохимическая схема - это условная запись, в которой представлена информация о аноде и катоде с указанием металлов, состава электролитов, а также особенностях конструкции данного гальванического элемента:


где Е0 – стандартный электродный потенциал металла анода или катода, n - число электронов, отдаваемых восстановителем или принимаемых окислителем, С - концентрация электролита, моль/л. Следовательно, ЭДС гальванического элемента может быть представлена следующей формулой:



Похожие готовые решения по химии:
- Объясните механизм защиты подземного стального трубопровода с помощью магниевого протектора, если почвенные воды в данной местности имеют ярко выраженный кислотный характер. Приведите электронные уравнения анодного и катодного процессов
- Как будет происходить электролиз водного раствора электролита ZnSO4 (t = 1 ч 15 мин, I = 12 А)? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях
- На нейтрализацию 3,28 г основания израсходовано 2,14 г HCl. Вычислите эквивалент основания. Какую массу магния можно окислить этим же количеством кислоты
- Определите скорость химической реакции N2(г) + 3Н2(г) = 2NH3(г) при исходных концентрациях [N2] = 2 моль/л и [H2] = 8 моль/л и в момент времени, когда концентрация азота уменьшилась на 10%
- Изменения термодинамических функций H, S, G в ходе химической реакции позволяют судить об особенностях протекания данной реакции и ее природе
- Большинство химических реакций являются обратимыми: одновременно с прямой реакций протекает обратная. В момент выравнивания скоростей прямой и обратной реакций в системе наступает состояние химического равновесия
- Необходимо произвести вычисления и найти недостающие величины в водных растворах величины под номером 113
- Степени окисления атомов в простых веществах (построенных из атомов одного и того же элемента) принимаются равными нулю
- Затраты организации на наем одного сотрудника в среднем составляют 56 тыс. руб., примерный срок в течении которого работник не исполняет
- Степени окисления атомов в простых веществах (построенных из атомов одного и того же элемента) принимаются равными нулю
- Объясните механизм защиты подземного стального трубопровода с помощью магниевого протектора, если почвенные воды в данной местности имеют ярко выраженный кислотный характер. Приведите электронные уравнения анодного и катодного процессов
- Кривая спроса на продукцию монополиста задана как Р = 30 - 0,2Q, где Q — количество товара, продаваемого за год; Р — цена товара

