
Как будет происходить электролиз водного раствора электролита NaCl (t = 25 мин, I = 8 А)? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Как будет происходить электролиз водного раствора электролита NaCl (t = 25 мин, I = 8 А)? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях. Составьте электронные уравнения процессов, протекающих на инертных электродах. Вычислите массу (для твердых и жидких) или объем (для газообразных) веществ, образующихся на электродах.
Решение
Электролиз - это окислительно-восстановительная реакция, происходящая на электродах при пропускании электрического тока через расплав или раствор электролита. В таких системах электролиты подвергаются диссоциации – распаду на положительно- (катионы) и отрицательно- (анионы) заряженные ионы.
Уравнение диссоциации электролита имеет вид:
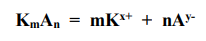
Для электролита, рассматриваемого в данной задаче:
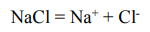
При электролизе расплавов веществ на катоде происходит процесс восстановления катионов (процесс присоединения электронов), а на аноде - процесс окисления анионов (процесс отдачи электронов). В результате, как правило, происходит разрядка ионов, т.е. переход их в нейтральное состояние:
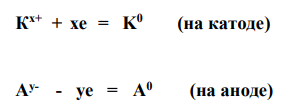
Если электролизу подвергается водный раствор, то необходимо учитывать возможность участия воды как в катодном, так и в анодном процессе.
Преимущественное участие молекул воды в катодном процессе:
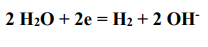
происходит в том случае, если в состав электролита входят катионы электрохимически активных металлов:
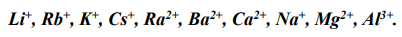
Такие катионы требуют для своей разрядки значительно больше энергии, чем ее затрачивается на выделение водорода из воды, поэтому получить эти металлы электролизом водных растворов их соединений невозможно.
Поскольку в состав электролита, указанного в условии задачи, входят катионы Na+ , то электронное уравнение катодного процесса имеет вид:
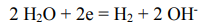
Если в состав электролита входят анионы кислородсодержащих кислот:(NO3 - , NO2 - , SO3 2- , SO4 2- , PO4 3- , CO3 2- и т.п.), а также фторид-анион F- , то по тем же энергетическим причинам в анодном процессе участвуют не анионы электролита, а молекулы воды:

Продуктами данного электролиза являются:
- непосредственно выделяющиеся на электродах H2 и Cl2,
- а также результаты вторичных взаимодействий между ионами, входящими в состав исходного электролита и не принимающие участие в электродных реакциях и ионами, образующимися в результате электродных реакций
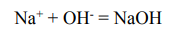
Для вычислений массы m (для газов - объема V) веществ, образующихся на электродах в результате электролиза, необходимо воспользоваться законом Фарадея:

I - сила тока, А z - число электронов в уравнении электродного процесса t - время проведения электролиза, секунды F - постоянная величина (число Фарадея), равная 96500 Кл/моль
В условии задачи дано: I = 8 A, t = 25 мин или 1500 сек Первый продукт электролиза H2 является газообразным (твердым, жидким или газообразным) веществом, поэтому для него необходимо вычислить объем (массу или объем). Подставляем в соответствующую формулу необходимые значения: 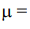 2 г/моль, z = 2.
2 г/моль, z = 2.
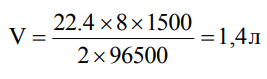
Второй продукт электролиза Cl2 (формула) является газообразным (твердым, жидким или газообразным) веществом, поэтому для него необходимо вычислить объем (массу или объем). Подставляем в соответствующую формулу необходимые значения: 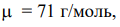 z = 4.
z = 4.
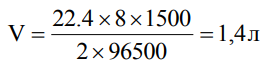

Похожие готовые решения по химии:
- Следовательно, заряд ядра атома есть суммарный заряд его протонов (нейтроны заряда не несут), а массовое число – суммарная масса протонов и нейтронов
- Охарактеризуйте валентные состояния атомов данного элемента в основном и возбужденных состояниях с помощью электронно-графических формул
- Определите тип химической связи (неполярная ковалентная, полярная ковалентная или ионная) в веществах нитрид лития и дихлорид серы
- Для реакции, указанной в условии задачи, выписываем необходимые справочные данные
- Электроотрицательность (EN) характеризует способность атомов элементов к смещению электронной плотности. В периоде системы элементов Д. И. Менделеева она возрастает слева направо, в подгруппе убывает сверху вниз (для s- и p-элементов
- Атомы элементов P в первой реакции и O во второй реакции (а также и вещества, в состав которых они входят PH3 в первой реакции и KClO3 во второй реакции) являются восстановителями (отдают электроны) и участвуют в процессе окисления (процессе отдачи электронов
- Катодный процесс заключается в восстановлении катионов, входящих в состав соли – электролита катода
- В чем различия в коррозии оцинкованного и луженого железа при нарушении целостности покрытий во влажной атмосфере? Приведите электронные уравнения анодного и катодного процессов в обоих случаях. Укажите продукты коррозии
- В чем различия в коррозии оцинкованного и луженого железа при нарушении целостности покрытий во влажной атмосфере? Приведите электронные уравнения анодного и катодного процессов в обоих случаях. Укажите продукты коррозии
- Катодный процесс заключается в восстановлении катионов, входящих в состав соли – электролита катода
- Финансовый директор компании «АРТ» составила прогнозный баланс. Ожидается рост выручки на 10 % от уровня прошлого года (330 млн.Р)
- Проведя статистический анализ деятельности компании, экономисты вывели следующие уравнения регрессии, увязывающие показатели баланса и отчета о прибылях и убытках

