
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Массовая доля кислорода в оксиде четырехвалентного металла составляет 40,05 %. Вычислите эквивалентную и атомную массы металла, найти его в периодической системе, написать формулу оксида
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
Массовая доля кислорода в оксиде четырехвалентного металла составляет 40,05 %. Вычислите эквивалентную и атомную массы металла, найти его в периодической системе, написать формулу оксида.
Решение:
Пусть масса оксида равна 100 г.
Тогда масса кислорода равна m(O) = w(O)*m = 0,4005*100 = 40,05 г m(Me) = 100 – m(O) = 100 – 40,05 = 59,95 г
По закону эквивалентов:
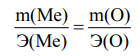
Эквивалентная масса металла равна
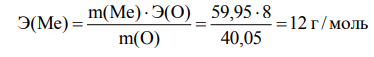
Учитывая, что металл четырехвалентен, атомная масса металла равна
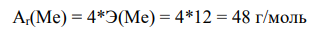
Это титан Ti – элемент 4 периода IVВ группы.
Формула оксида – 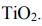
Ответ: 12 г/моль; 48 г/моль.

Похожие готовые решения по химии:
- Среди гидроксидов Са(ОН)2, Fe(OH)2, Sn(OH)2 найти амфотерный и показать его амфотерность уравнениями реакций
- Для данной окислительно-восстановительной реакции определить её тип; указать восстановитель и окислитель; подобрать коэффициенты методом электронного баланса; рассчитать эквивалентные массы окислителя и восстановителя
- Объясните, почему изменяется длина связи между атомами углерода в молекулах С2Н6 (0,154 нм), С2Н4 (0,135 нм), С2Н2 (0,120 нм
- Используя метод МО, объяснить, почему ионизационные потенциалы атомов кислорода (13,6 эВ) и фтора (17,4 эВ) выше, чем молекул O2 (12,2 эВ) и F2 (15,8 эВ
- Коэффициент распределения некоторого вещества между бензолом и водой равен К (табл. 11). Вычислить объем бензола, необходимый для извлечения Х % вещества при однократном экстрагировании из объема V. В обоих растворителях вещество имеет одинаковую молекулярную массу
- Константа скорости реакции второго порядка A + B = C при одинаковых концентрациях реагирующих веществ равна К. За какое время прореагирует Х % исходных веществ
- Вычислить pH раствора и концентрацию ионов H+ , если при T=298 К известна эдс элемента (табл. 15). Стандартный электродный потенциал хингидронного электрода 0,699 В, каломельного - 0,337 В, хлоридсеребряного - 0,284
- Вычислить активность ионов металла по величине ЭДС концентрационной цепи при T=298 К, если активность иона в одном из электродов
- Вычислить активность ионов металла по величине ЭДС концентрационной цепи при T=298 К, если активность иона в одном из электродов
- В первом ящике 6 белых и 11 черных шаров, а во втором ящике 10 белых и 3 черных шара. Из первого ящика во второй переложили два шара. а) после перекладывания из второго ящика вынуты 3 шара. Какова вероятность
- Для данной окислительно-восстановительной реакции определить её тип; указать восстановитель и окислитель; подобрать коэффициенты методом электронного баланса; рассчитать эквивалентные массы окислителя и восстановителя
- Среди гидроксидов Са(ОН)2, Fe(OH)2, Sn(OH)2 найти амфотерный и показать его амфотерность уравнениями реакций

