
На основании положения химического элемента № 35 и его электронной формулы составьте прогноз его химических свойств, ответив на следующие вопросы
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
На основании положения химического элемента № 35 и его электронной формулы составьте прогноз его химических свойств, ответив на следующие вопросы:
31. В каких периоде, группе и подгруппе располагается данный элемент в периодической системе Д.И. Менделеева?
32. Укажите соответствие между положением элемента в периодической системе Д.И. Менделеева и его электронной формулой (номером внешнего энергетического уровня, общим числом валентных электронов, характером их распределения по энергетическим подуровням).
33. К какому электронному семейству относится данный элемент?
34. Охарактеризуйте валентные состояния атомов данного элемента в основном и возбужденных состояниях с помощью электронно-графических формул.
35. Чему равны максимальная и минимальная степени окисления атомов этого элемента?
36. Каковы формулы высшего оксида и соответствующего гидроксида этого элемента?
Решение
Данный элемент располагается в периодической системе в периоде № 4, в группе № 7, в главной подгруппе. Электронная формула элемента имеет вид:
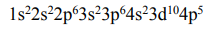
Номер внешнего энергетического уровня (n = 4) соответствует номеру периода. Общее число валентных электронов (электронов внешнего энергетического уровня, а также предвнешнего d-подуровня, если он застроен неполностью) для большинства элементов соответствует номеру группы

Принадлежность элементов к главным или побочным подгруппам определяется типом электронного семейства:
s- и p-элементы составляют главные подгруппы, d- и f-элементы образуют побочные подгруппы. Классификация химических элементов по электронным семействам основана на характере застройки электронных оболочек.
В соответствии с ним элементы подразделяются на следующие электронные семейства:
- s-элементы (застройка внешнего s-подуровня, все внутренние слои застроены);
- p-элементы (застройка внешнего p-подуровня, все внутренние слои застроены);
- d-элементы (застройка предпоследнего d-подуровня);
- f-элементы (застройка третьего снаружи f-подуровня). Исходя из указанной классификации элемент бром Br принадлежит к рэлектронному семейству и находится в периодической системе в главной подгруппе. Валентные состояния атомов определяются наличием одиночных неспаренных валентных электронов (спиновая валентность). Для определения спиновой валентности элемента в основном (т.е. отвечающем его минимальной энергии) распределяем его валентные электроны по квантовым ячейкам в соответствии с принципом Паули и правилом Хунда:
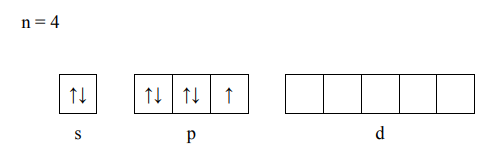
Число одиночных неспаренных валентных электронов равно 1. Кроме представленного выше основного состояния атома можно представить возбужденные состояния, в которые атом переходит при получении им дополнительных порций энергии, и которые характеризуются переходами электронов из занятых ячеек в свободные в пределах данного уровня, что проявляется в изменении спиновой валентности элемента. Если свободные квантовые ячейки на данном энергетическом уровне отсутствуют, то возбужденные состояние невозможны, и спиновая валентность в таком случае постоянна.
Возбужденные состояния для атома рассматриваемого в задаче элемента можно отобразить следующими схемами:
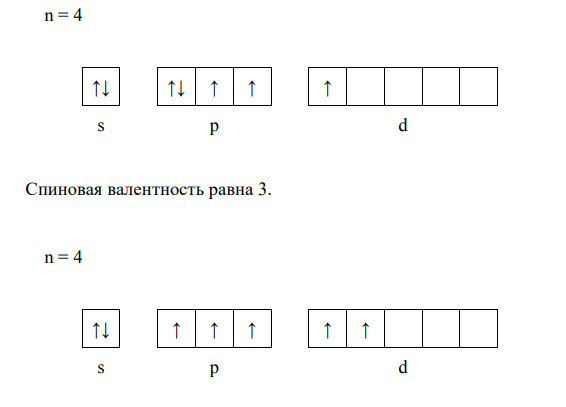
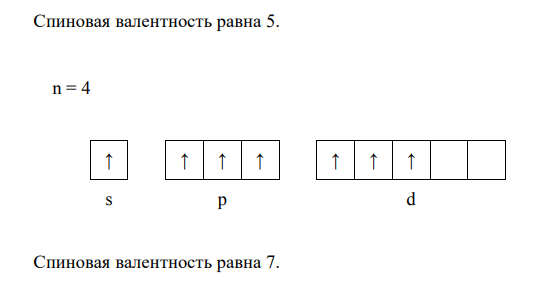
Высшую (максимальную) степень окисления атом приобретает, отдав все свои валентные электроны. Поэтому для большинства элементов максимальная степень окисления равна номеру группы, в которой находится данный элемент в таблице Д.И. Менделеева. Следовательно, для элемента бром Br максимальная степень окисления составляет: +7. Низшая (минимальная) степень окисления соответствует числу электронов, необходимых атому для достройки внешнего электронного слоя до октета восьмиэлектронной структуры). Поэтому минимальную степень окисления можно вычислить по формуле: Nгруппы - 8. Однако, присоединение электронов свойственно только атомам типичных неметаллов, поэтому для металлов и переходных элементов минимальная степень окисления равна нулю.
Рассматриваемый в задаче элемент бром Br проявляет минимальную степень окисления -1. Зная величины максимальной и минимальной степени окисления атомов элементов, можно составить формулы их соединений. Оксиды - это соединения элементов с кислородом. Общая формула оксида: ЭmOn (Э-символ элемента, О - символ кислорода, числа m и n показывают количественное соотношение между атомами элементов).
Кислород проявляет минимальную степень окисления -2 (элемент VI группы). Поэтому для обеспечения электронейтральности химической формулы необходимо подобрать следующие соотношения m:n для указанного в задаче элемента: бром Br и формула его оксида имеет вид: 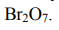
Гидроксиды - это основания (для типичных металлов и d-элементов, если их атомы находятся в степени окисления не выше +3) и кислоты (для типичных неметаллов и d-элементов в степенях окисления >3). Общая формула основания: 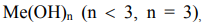 при этом число гидроксильных групп (ОН- ) соответствует валентности металла.
при этом число гидроксильных групп (ОН- ) соответствует валентности металла.
Для элемента, приведенного в условии задачи, формула основания имеет вид: - (если элемент не образует оснований, поставьте прочерк). Наиболее распространенные кислоты, в состав которых входят атомы элементов в максимальной степени окисления, имеют общую формулу HmЭO4. Используя значения степеней окисления атомов (H+1, O-2 , и высшей степени окисления элемента Э), составляем формулу кислоты: HBrO4 (если элемент не образует кислот, поставьте прочерк). Для кислот с m = 3 или 4 (орто-кислоты) возможно отщепление молекулы воды (- H2O) и образование второй формы кислоты - мета-формы (H m-2 ЭO3). Для данного элемента образование мета-кислоты невозможно (возможно или невозможно), ее формула: -.

Похожие готовые решения по химии:
- Определите тип химической связи (неполярная ковалентная, полярная ковалентная или ионная) в веществах бромид кальция и дибром
- Изменения термодинамических функций H, S, G в ходе химической реакции позволяют судить об особенностях протекания данной реакции и ее природе
- Большинство химических реакций являются обратимыми: одновременно с прямой реакций протекает обратная. В момент выравнивания скоростей прямой и обратной реакций в системе наступает состояние химического равновесия
- Необходимо произвести вычисления и найти недостающие величины в водных растворах величины под номером 113
- Более отрицательной величиной электродного потенциала характеризуется металл Mn, поэтому именно он и будет участником анодного процесса
- Изделие, составленное из медных и никелевых фрагментов, эксплуатируется в разбавленном растворе хлороводорода. Как будет 550 происходить процесс контактной коррозии? Составьте электронные уравнения анодного и катодного процессов
- Как будет происходить электролиз водного раствора электролита NaNO3 (t = 45 мин, I = 7 А)? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях
- Таким образом, число протонов в ядре численно совпадает с атомным (порядковым) номером элемента в периодической системе Д.И. Менделеева. Число нейтронов можно вычислить по разности между массовым числом и числом протонов
- Организация проводит обучение и тренинги персонала, за счет которых ожидает повышения производительности на 5%. Стоимость обучения
- Численность занятых альтернативной трудовой деятельностью – 215 тыс.чел. ; занятых – 1800 тыс. чел.; безработных, активно ищущих работу
- Изменения термодинамических функций H, S, G в ходе химической реакции позволяют судить об особенностях протекания данной реакции и ее природе
- Определите тип химической связи (неполярная ковалентная, полярная ковалентная или ионная) в веществах бромид кальция и дибром

