
Напишите формулы и латинские названия калия и натрия хлоридов, бромидов, иодидов
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16977 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Напишите формулы и латинские названия калия и натрия хлоридов, бромидов, иодидов. Охарактеризуйте их физические и химические свойства, стабильность. Приведите описание (реактивы, условия, эффекты) общих и специфических реакций идентификации, подтвердите их соответствующими уравнениями. Укажите особенности условий хранения.
Ответ:
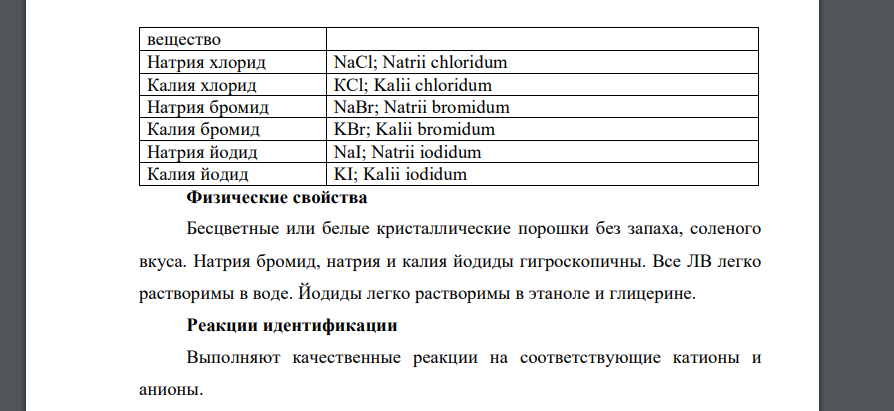
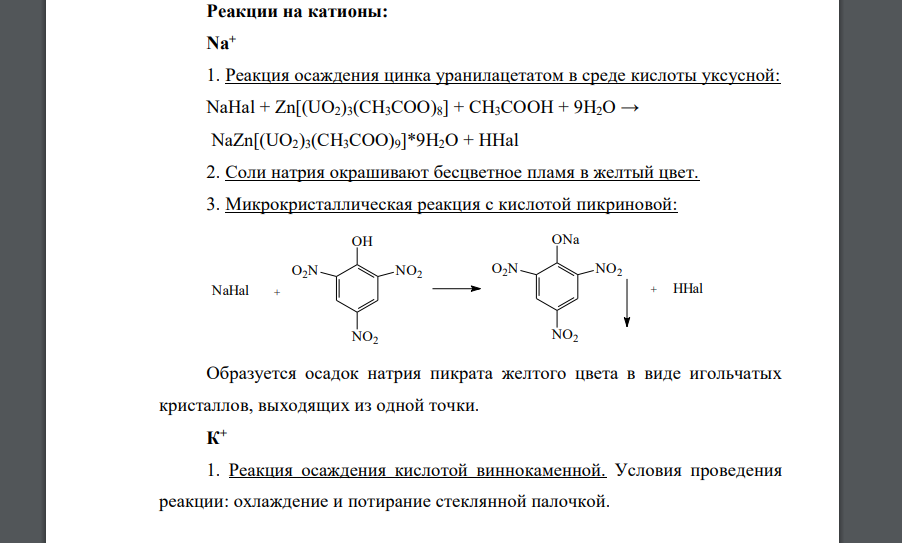
Физические свойства Бесцветные или белые кристаллические порошки без запаха, соленого вкуса. Натрия бромид, натрия и калия йодиды гигроскопичны. Все ЛВ легко растворимы в воде. Йодиды легко растворимы в этаноле и глицерине. Реакции идентификации Выполняют качественные реакции на соответствующие катионы и анионы. Реакции на катионы: Na+ 1. Реакция осаждения цинка уранилацетатом в среде кислоты уксусной. Соли натрия окрашивают бесцветное пламя в желтый цвет. 3. Микрокристаллическая реакция с кислотой пикриновой. Образуется осадок натрия пикрата желтого цвета в виде игольчатых кристаллов, выходящих из одной точки. К+ 1. Реакция осаждения кислотой виннокаменной. Условия проведения реакции: охлаждение и потирание стеклянной палочкой.Осадок калия гидротартрата растворим в разведенных минеральных кислотах и в растворах натрия или калия гидроксида. Для связывания выделяющейся галогенводородной кислоты добавляют натрия ацетат. 2. Реакция осаждения натрия гексанитрокобальтатом (III) в уксуснокислой среде. Образуется желтый кристаллический осадок. 3 Соли калия окрашивают бесцветное пламя в фиолетовый цвет или при рассматривании через синее стекло – в пурпурно-красный. Реакции на анионы: 1. Реакция осаждения серебра нитратом; проводится в азотнокислой среде– белый творожистый осадок, нерастворимый в кислоте азотной разведенной и растворимый в растворе аммиака– желтоватый творожистый осадок, нерастворимый в кислоте азотной разведенной и трудно растворимый в растворе аммиака. AgI↓ – желтый творожистый осадок, нерастворимый в кислоте азотной разведенной и в растворе аммиака. 2. Реакции окисления галогенид-ионов (бромидов и йодидов) до свободных галогенов. Основаны на восстановительных свойствах галогенидионов: Образующиеся галогены извлекают в хлороформ и наблюдают окраску хлороформного слоя. Галогениды отличаются по силе восстановительных свойств. Хлориды являются очень слабыми восстановителями. Окисляются лишь сильными окислителями, при нагревании; образующийся хлор доказать трудно. Поэтому для доказательства хлоридов реакция окисления обычно не используется Бромиды обладают более выраженными восстановительными свойствами; окисляются только сильными окислителями (KMnO4, Cl2). Йодиды являются сильными восстановителями; окисляются и сильными, и слабыми окислителями. 2.1. Для доказательства бромид-иона в качестве окислителя используют раствор хлорамина в присутствии кислоты хлороводородной разведенной.Слой хлороформа окрашивается в желто-оранжевый цвет. 2.2. Для подтверждения подлинности йодид-ионов в качестве реагента используют слабые окислители, которые окисляют йодиды, но не окисляют бромид-ионы и хлорид-ионы (т.е. избирательные окислители). 2.2.1. Раствор железа (III) хлорида или раствор натрия нитрита. Слой хлороформа окрашивается в фиолетовый цвет. 2.2.2. Кислота серная концентрированная. Наблюдают выделение фиолетовых паров йода. ХранениеВ хорошо укупоренной таре, в сухом месте (натрия бромид и йодид, калия йодид – гигроскопичны). Бромиды и йодиды легко окисляются до свободного галогена, поэтому их необходимо предохранять от действия света (хранят в склянках темного стекла).

Похожие готовые решения по химии:
- Опишите методики приготовления и установки титра 0,1 моль\л раствора натрия нитрита
- Дайте характеристику и укажите особенности кислотно-основного титрования в неводных средах
- Рассчитайте % содержание сульфатной золы в фолиевой кислоте (ГФХ, ст.13), если взята навеска
- Опишите методику определения примесей SO4 2- по ГФ ХI. Рассчитайте, какое количество
- Напишите на латинском языке состав лекарственной формы: Раствора кислоты соляной
- Напишите уравнения реакций, лежащих в основе определения примесей сульфидов
- Назовите методы количественного определения препаратов цинка, укажите условия
- Напишите формулы и латинские названия кислоты борной и натрия тетрабората
- Исходя из правила ПР, сформулируйте условия образования и растворения осадков.
- Найти индекс прироста реального ВВП , если известны следующие изменения: P1 =1,05P0 Для решения использовать формулу:
- в краткосрочном периоде Фирма действует в условиях совершенной конкуренции
- Опишите методики приготовления и установки титра 0,1 моль\л раствора натрия нитрита

