
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Определите термодинамическую возможность протекания реакции Н2(г) + СО2(г) = СО(г) + Н2О(г) при стандартных условиях. Как повлияет повышение температуры на термодинамическую вероятность протекания процесса
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
Определите термодинамическую возможность протекания реакции Н2(г) + СО2(г) = СО(г) + Н2О(г) при стандартных условиях. Как повлияет повышение температуры на термодинамическую вероятность протекания процесса? Решение:
Н2(г) + СО2(г) = СО(г) + Н2О(г)
Термодинамическая возможность протекания реакции в стандартных условиях определяется изменением энергии Гиббса реакции. Изменение энергии Гиббса рассчитаем по уравнению:
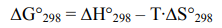
Рассчитаем изменение энтальпии и энтропии реакции при 298 К. Справочные данные представим в виде таблицы.
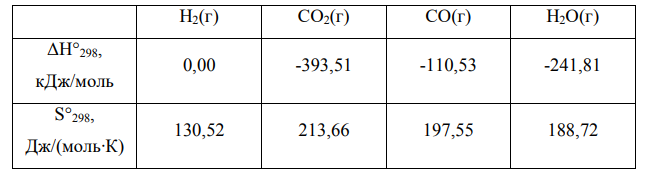

Ответ: не протекает; увеличивается.

Похожие готовые решения по химии:
- Укажите, при каких условиях можно создать гальванический элемент из двух электродов 1-го рода одинаковой химической природы. Приведите пример такого элемента, уравнения анодно-катодных процессов и рассчитайте ЭДС
- Рассчитайте, при каком напряжении можно выделить металлы Zn и Cd при электролизе
- Медное изделие покрыто оловом. Какое это покрытие? Составьте схему электрохимической системы, уравнения анодно-катодных процессов
- Применение анодных процессов электролиза в технике (оксидирование, анодное травление, полировка). Приведите конкретные примеры, запишите схемы электролизных систем и уравнения процессов, протекающих на аноде и катоде
- Вычислите концентрацию ионов и их количество, содержащихся в 100 мл 0,01 М раствора HNO2 (КД = 4⋅10–4 ). Запишите уравнение диссоциации и выражение для константы диссоциации, как изменятся значения α и КД HNO2 при уменьшении концентрации раствора
- Определите, сколько граммов щелочи КОН содержится в 500 мл его раствора, рН которого равен 12
- Вычислите стандартную энтальпию образования сульфида цинка (ZnS), используя стандартные энтальпии образования веществ, если известно, что тепловой эффект (∆H°298) реакции
- Рассчитайте изменение энтропии для реакции 2ZnS(кр) + 3О2(г) = 2ZnO(кр) + 2SO2(г), протекающей при постоянном давлении (P =101 кПа ) и T = 998 K. При расчетах принять, что в интервале 298 – 998 К Ср не зависит от Т
- Рассчитайте изменение энтропии для реакции 2ZnS(кр) + 3О2(г) = 2ZnO(кр) + 2SO2(г), протекающей при постоянном давлении (P =101 кПа ) и T = 998 K. При расчетах принять, что в интервале 298 – 998 К Ср не зависит от Т
- Вычислите стандартную энтальпию образования сульфида цинка (ZnS), используя стандартные энтальпии образования веществ, если известно, что тепловой эффект (∆H°298) реакции
- Рассчитайте, при каком напряжении можно выделить металлы Zn и Cd при электролизе
- Укажите, при каких условиях можно создать гальванический элемент из двух электродов 1-го рода одинаковой химической природы. Приведите пример такого элемента, уравнения анодно-катодных процессов и рассчитайте ЭДС

