
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Пpоизведите необходимые вычисления и найдите недостающие величины, обозначенные знаком "?" в стpоке табл.6, соответствующей номеpу
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16787 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
Пpоизведите необходимые вычисления и найдите недостающие величины, обозначенные знаком "?" в стpоке табл.6, соответствующей номеpу Вашей задачи (все pаствоpы – водные).
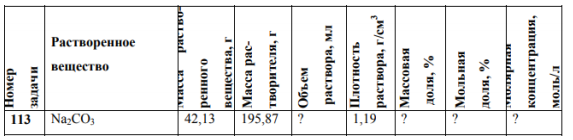
Решение:
Масса раствора:Массовая доля: Для определения мольной доли растворенного вещества необходимо рассчитать химические количества компонентов раствора. Мольная доля равна: 1 Молярная концентрация:

Похожие готовые решения по химии:
- Для pеакций, пpотекающих по пpиведенным схемам, составьте уpавнения методом электpонного баланса. Для каждой pеакции укажите, какое
- По заданию из табл.7 составьте схему гальванического элемента, напишите электронные уравнения электродных процессов и суммаpное
- Объясните механизм защиты подземного стального трубопровода с помощью магниевого протектора, если почвенные воды в данной местности
- Как будет происходить электролиз водного раствора электролита (табл. 8) при использовании инертных электродов? Приведите уравнение
- Определите символы элементов и найдите величины, помеченные знаком "?", в табл.
- Определите тип химической связи (ковалентная неполярная, ковалентная полярная или ионная) в веществах, указанных в табл. 3. В случае
- Вычислите величины ∆H0 298, ∆S0 298 и ∆G0 298 для реакций, уравнения которых приведены в табл. 4 (необходимые для расчетов данные см. в
- Для pеакции, соответствующей номеpу Вашей задачи (см. табл. 4): 1) составьте кинетическое уpавнение; 2) составьте выpажение для
- Составьте уравнения анодного и катодного процессов, происходящих при коррозии железа, покрытого серебром, во влажном воздухе и в кислой среде. Определите тип покрытия – анодное или катодное
- Свежеполученный осадок Fe(OH)3 разделили на две порции. К одной добавили небольшое количество FeCl3, а к другой – HCl. Получили в обоих случаях золь Fe(OH)3. Дайте
- Вычислите количество электричества, которое необходимо пропустить через раствор хлорида натрия, чтобы получить 1 т гидроксида натрия. 30 Приведите схемы электродных процессов
- Пороги коагуляции для золя Al(OH)3 оказались равными Спк (KNO3)=50,0 ммоль/л Спк (Na2SO4)=0,72 ммоль/л Спк (Na3PO4)=0,093 ммоль/л Как заряжены частицы

