
Сформулируйте понятие концентрации вещества в растворе. Приведите известные способы выражения концентрации раствора. К 100 мл воды при комнатной
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16718 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Сформулируйте понятие концентрации вещества в растворе. Приведите известные способы выражения концентрации раствора. К 100 мл воды при комнатной температуре добавили 4,00 г сахарозы (С12Н22О11). 1. Сделав разумные допущения, вычислить давление пара над полученным раствором при 373 К. 2. Вычислить температуру кипения этого раствора, если эбулиоскопическая постоянная равна 0,512 К·кг/моль. 3. Вычислить мольную и массовую долю обоих компонентов раствора, в также молярную концентрацию сахарозы в растворе, полученном после упаривания исходного раствора до 10 мл, если его масса равна 11,43 г.
Решение:
Концентрация – величина, характеризующая количественный состав раствора. Молярная концентрация – отношение количества вещества в молях (n) к объему раствора в литрах: Если вещество обозначить через то: , Нормальная концентрация или молярная концентрация эквивалента – отношение количества эквивалентов вещества к объему раствора , Молярная и нормальная концентрации связаны между собой: – титр раствора –это масса вещества в граммах в мл раствора раствора по определяемому веществу – это масса вещества в г, взаимодействующая с мл титранта. Массовая доля вещества – отношение массы растворенного вещества к массе раствора. Массовая доля – величина безразмерная, ее представляют либо в долях, либо в процентах. где – плотность раствора. Моляльная концентрация – отношение количества молей растворенного вещества к растворителя, т.е. число молей растворенного в-ва в растворителя. 1. По закону Рауля Рассчитаем мольную долю воды в поученном растворе (плотность воды равна 2. Температура кипения раствора определяется по уравнению Рассчитаем моляльность раствора сахарозы: 3. После упаривания масса сахарозы не изменилась, т.е. равна г. Масса воды равна Рассчитаем мольные доли компонентов: Рассчитаем массовые доли компонентов раствора. Молярная концентрация сахарозы в растворе после упаривания равна

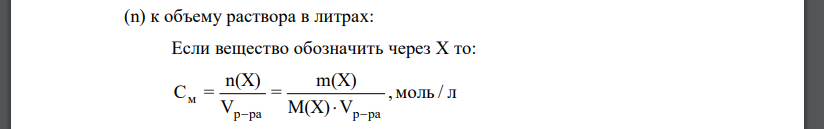
Похожие готовые решения по химии:
- Составить методику с полной расчетной аргументацией определения примеси сульфатов в натрия хлориде, если согласно ЧФС: Раствор 2 г препарата в 10 мл воды
- Какую массу натрия тиосульфата необходимо взять для количественного определения, чтобы на титрование затратить 24 мл 0,1 М раствора йода (теоретически)? Напишите
- Соответствует ли калия бромид требованиям ЧФС, если на титрование 0,2222 г препарата пошло 23,4 мл 0,1 М раствора нитрата серебра. Напишите уравнение химических
- Сколько необходимо взять раствора перекиси водорода 3%, чтобы на титрование его 0,1 М раствором перманганата калия пошло 24,1 мл (теоретически). Поправочный
- Какой объем 0,001 М раствора BaCl2 надо добавить к 0,02 л 0,0007 М раствора Al2(SO4)3, чтобы получить положительно заряженные частицы золя сульфата бария
- Определите количество совершаемой работы, теплоту процесса, изменение внутренней энергии, энтальпии, энергии Гиббса и энтропии, если 2 моля водорода
- Приведите вывод уравнения изотермы химической реакции (уравнение Льюиса) исходя из фундаментального уравнения Гиббса для системы с переменным
- Запишите уравнение Клаузиса-Клапейрона в дифференциальном виде для случая процессов испарения и возгонки. Давление насыщенного пара льда при -5,0 0С равно
- Напишите схему мицеллы золя серы (стабилизатор Какой из электролитов имеет наименьший порог коагуляции и наибольшую коагуляционную
- К источнику тока с ЭДС ε и внутренним сопротивлением r присоединены три сопротивления R1, R2 и R3 как показано на схеме (рис. 2). Определить: 1). силу
- В закрытом резервуаре объёмом V находится газ Х. Начальное состояние газа (состояние 1) характеризуется термодинамическими
- Даны результаты наблюдений случайной величины 𝑋. Разделив интервал значений 𝑋 на десять равных частей, построить группировку, гистограмму, эмпирическую функцию

