
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
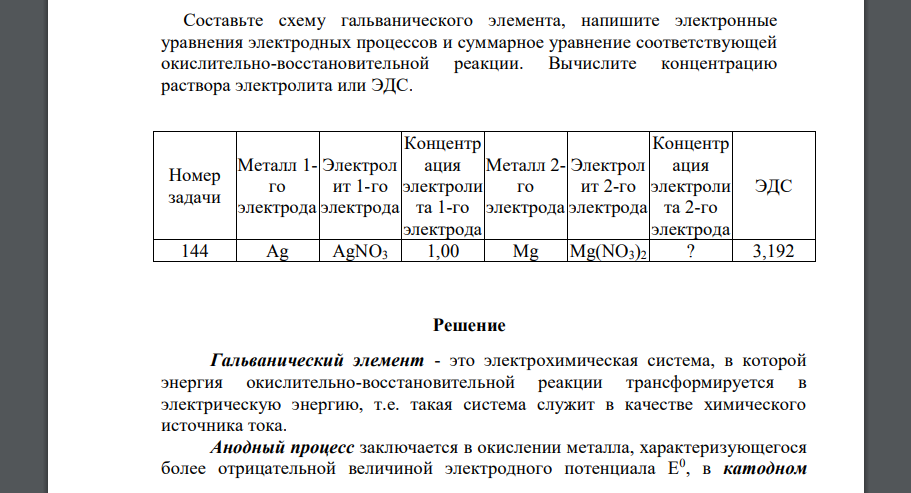
Составьте схему гальванического элемента, напишите электронные уравнения электродных процессов и суммарное уравнение соответствующей
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16800 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
Составьте схему гальванического элемента, напишите электронные уравнения электродных процессов и суммарное уравнение соответствующей окислительно-восстановительной реакции. Вычислите концентрацию раствора электролита или ЭДС. Номер задачи Металл 1- го электрода Электрол ит 1-го электрода Концентр ация электроли та 1-го электрода Металл 2- го электрода Электрол ит 2-го электрода Концентр ация электроли та 2-го электрода ЭДС 144 Ag AgNO3 1,00 Mg Mg(NO3)2 ? 3,192
Решение
Гальванический элемент - это электрохимическая система, в которой энергия окислительно-восстановительной реакции трансформируется в электрическую энергию, т.е. такая система служит в качестве химического источника тока. Анодный процесс заключается в окислении металла, характеризующегося более отрицательной величиной электродного потенциала, в катодном процессе участвует частица-окислитель, присутствующая в катодном электролите. Для металлов, приведенных в условии задачи: (таблицу стандартных электродных потенциалов см. ДОТ_Химия_2.2. Опорный конспект_Справочные материалы) ; Более отрицательной величиной электродного потенциала характеризуется металл Mg, поэтому именно он и будет участником анодного процесса. Металл анода окисляется, что можно представить в виде электронного уравнения вида: Для данного металла: Катодный процесс заключается в восстановлении катионов металла, входящих в состав соли – электролита катода. Соответствующее электронное уравнение имеет вид: Для системы, описанной в условии задачи: Электрохимическая схема - это условная запись, в которой представлена информация о аноде и катоде с указанием металлов, состава электролитов, а также особенностях конструкции данного гальванического элемента: Металл I | Электролит I || Электролит II | Металл II (с более .. (с менее отриц.Е0 ) отриц.Е0 ) АНОД КАТОД 256 Для рассматриваемого в задаче гальванического элемента электрохимическая схема имеет вид: Mg | Mg(NO3)2 || AgNO3 | Ag а н о д к а т о д Чтобы вычислить ЭДС гальванического элемента, необходимо найти разность потенциалов катода и анода: катода - Е анода Каждый из указанных потенциалов можно вычислить по формуле Нернста: электролит а стандартный электродный потенциал металла анода или катода, n - число электронов, отдаваемых восстановителем или принимаемых окислителем, С - концентрация электролита, моль/л. Следовательно, ЭДС гальванического элемента может быть представлена следующей формулой: ЭДС = (мет. катода Cэл-та катода) – (мет. анода Cэл-та анода) Подставляем численные данные условия задачи и производим необходимые вычисления: Е 0 мет. катода Cэл-та катода Cэл-та катода (для катодного процесса) (для анодного процесса) ЭДС Неизвестная величина:
Решение
Гальванический элемент - это электрохимическая система, в которой энергия окислительно-восстановительной реакции трансформируется в электрическую энергию, т.е. такая система служит в качестве химического источника тока. Анодный процесс заключается в окислении металла, характеризующегося более отрицательной величиной электродного потенциала, в катодном процессе участвует частица-окислитель, присутствующая в катодном электролите. Для металлов, приведенных в условии задачи: (таблицу стандартных электродных потенциалов см. ДОТ_Химия_2.2. Опорный конспект_Справочные материалы) ; Более отрицательной величиной электродного потенциала характеризуется металл Mg, поэтому именно он и будет участником анодного процесса. Металл анода окисляется, что можно представить в виде электронного уравнения вида: Для данного металла: Катодный процесс заключается в восстановлении катионов металла, входящих в состав соли – электролита катода. Соответствующее электронное уравнение имеет вид: Для системы, описанной в условии задачи: Электрохимическая схема - это условная запись, в которой представлена информация о аноде и катоде с указанием металлов, состава электролитов, а также особенностях конструкции данного гальванического элемента: Металл I | Электролит I || Электролит II | Металл II (с более .. (с менее отриц.Е0 ) отриц.Е0 ) АНОД КАТОД 256 Для рассматриваемого в задаче гальванического элемента электрохимическая схема имеет вид: Mg | Mg(NO3)2 || AgNO3 | Ag а н о д к а т о д Чтобы вычислить ЭДС гальванического элемента, необходимо найти разность потенциалов катода и анода: катода - Е анода Каждый из указанных потенциалов можно вычислить по формуле Нернста: электролит а стандартный электродный потенциал металла анода или катода, n - число электронов, отдаваемых восстановителем или принимаемых окислителем, С - концентрация электролита, моль/л. Следовательно, ЭДС гальванического элемента может быть представлена следующей формулой: ЭДС = (мет. катода Cэл-та катода) – (мет. анода Cэл-та анода) Подставляем численные данные условия задачи и производим необходимые вычисления: Е 0 мет. катода Cэл-та катода Cэл-та катода (для катодного процесса) (для анодного процесса) ЭДС Неизвестная величина:

Похожие готовые решения по химии:
- Как протекает электрохимическая коррозия в .......................... среде при контакте металлов ......... и .......... ? Какой из металлов разрушается
- Как будет происходить электролиз водного раствора электролита NaNO3 (t = 45 мин, I = 7 А)? Приведите уравнение диссоциации электролита и поясните
- Электрическая проводимость растворов (удельная, эквивалентная, молярная). Зависимость электрической проводимости
- Закон независимого движения ионов
- Вычислите стандартные величины H 0 298, S 0 298 и G 0 298 для реакции: C2Cl4(г) + Cl2(г) = C2Cl6(г) Объясните знак изменения энтальпии и энтропии
- Для реакции: C2Cl4(г) + Cl2(г) = C2Cl6(г) составьте кинетическое уравнение; составьте выражение для константы равновесия
- Пpоизведите необходимые вычисления и найдите недостающие величины, обозначенные знаком "?" в стpоке табл.6, соответствующей номеpу Вашей
- Для реакций: 251 1) NaAsO2 + I2 + Na2CO3+ H2O → NaH2AsO4 + NaI + CO2 2) Cu(NO3)2 → CuO + NO2 + O2 Составьте уравнения методом электронного баланса
- Вычислить индикаторную ошибку титрования раствора Mo(V) раствором NH4VO3 в сильнокислой среде: в) с N-фенилантраниловой
- Линза из крона лежит на пластинке, одна половина которой сделана из того же крона, а другая из флинта Прислойка между линзой и пластинкой
- При изучении физико-механических свойств обувных кож было испытано 𝑛 образцов и получены следующие значения предела прочности на
- Каково должно быть минимальное расстояние между двумя точками на поверхности Марса, чтобы их изображения в телескопе (рефракторе)

