
Составьте уравнение реакции гидролиза в ионной и молекулярной формах для солей СН3СООNH4 и Cu(ClO4)2. Как повлияет на их гидролиз подкисление раствора? Какой характер (кислый, нейтральный, щелочной) имеют растворы
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Составьте уравнение реакции гидролиза в ионной и молекулярной формах для солей СН3СООNH4 и Cu(ClO4)2. Как повлияет на их гидролиз подкисление раствора? Какой характер (кислый, нейтральный, щелочной) имеют растворы?
Ответ:
СН3СООNH4 – соль слабой кислоты CH3COOH и слабого основания NH4OH, поэтому гидролиз протекает и по катиону, и по аниону. CH3COO- + NH4 + + H2O = CH3COOH + NH4OH CH3COONH4 + H2O = CH3COOH + NH4OH Реакция раствора близка к нейтральной: 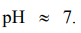 Подкисление не повлияет на гидролиз. Cu(ClO4)2 – соль сильной кислоты HClO4 и слабого основания Cu(OH)2, поэтому гидролиз протекает по катиону.
Подкисление не повлияет на гидролиз. Cu(ClO4)2 – соль сильной кислоты HClO4 и слабого основания Cu(OH)2, поэтому гидролиз протекает по катиону.
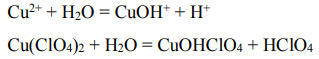
Среда раствора кислая, рН < 7. Подкисление раствора замедлит гидролиз, т.к. по принципу Ле-Шателье химическое равновесие сместится влево.

Похожие готовые решения по химии:
- Чему равна сумма коэффициентов перед формулами веществ правой части уравнения реакции
- Напишите формулу комплексного соединения, в котором комплексообразователь – Sn4+, лиганды – ионы фтора. Координационное число комплексообразователя 6. Во внешнюю координационную сферу включите либо ионы NO3 - , либо ионы рубидия
- Сколько граммов КСl требуется для приготовления 1 л раствора, содержащего в литре 1 г хлор-иона
- При определении массовой доли оксида кремния в минерале необходимо, чтобы масса прокаленного осадка SiO2 была не более 0,2 г. Вычислите массу минерала, необходимую для анализа, если в его составе 30% кремния
- Молярная масса вещества 90 г/моль. Выведите химическую формулу вещества, если в его состав входят: углерод – 26,7%, водород – 2,2%, кислород – 71,1%
- Атомы какого химического элемента имеют электронный слой 3s 23p 63d 3 ? Сколько протонов и нейтронов содержится в его атоме с массовым 290 числом 50? Приведите примеры двух-трех соединений данного химического элемента
- а) Как повлияет на растворимость углекислого газа в воде: 1) нагревание, 2) повышение давления, 3) прибавление кислоты, 4) прибавление щелочи
- В 1 л воды растворили 200 г Na2CO3·10Н2О. Получился раствор плотностью 1,05 г/мл. Рассчитайте процентную концентрацию раствора Na2CO3, а также его молярность и нормальность
- В 1 л воды растворили 200 г Na2CO3·10Н2О. Получился раствор плотностью 1,05 г/мл. Рассчитайте процентную концентрацию раствора Na2CO3, а также его молярность и нормальность
- а) Как повлияет на растворимость углекислого газа в воде: 1) нагревание, 2) повышение давления, 3) прибавление кислоты, 4) прибавление щелочи
- Напишите формулу комплексного соединения, в котором комплексообразователь – Sn4+, лиганды – ионы фтора. Координационное число комплексообразователя 6. Во внешнюю координационную сферу включите либо ионы NO3 - , либо ионы рубидия
- Чему равна сумма коэффициентов перед формулами веществ правой части уравнения реакции

