
В таблице 1 приведена зависимость концентрации реагентов С от времени t. В реакциях, в которых участвуют
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16951 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
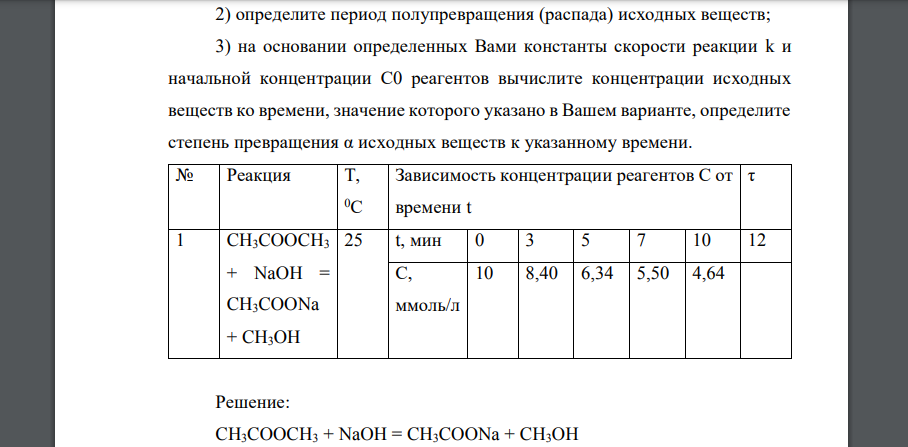
В таблице 1 приведена зависимость концентрации реагентов С от времени t. В реакциях, в которых участвуют два исходных вещества, начальные концентрации С0 реагирующих веществ одинаковы. По данным Вашего варианта 1) рассчитайте константу скорости реакции (с указанием ее единицы измерения) методом подстановки; 2) определите период полупревращения (распада) исходных веществ; 3) на основании определенных Вами константы скорости реакции k и начальной концентрации С0 реагентов вычислите концентрации исходных веществ ко времени, значение которого указано в Вашем варианте, определите степень превращения α исходных веществ к указанному времени.
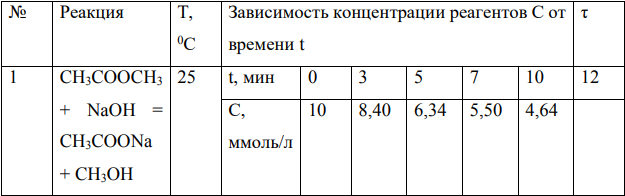
Решение:
1) Определим порядок реакции методом подстановки. Из условия задачи известно, что при t = 0 мин С = 10 ммоль/л, т.е. начальная концентрация реагирующих веществ С0 равна 10 ммоль/л. Предположим, что реакция имеет нулевой порядок. Константа скорости реакции нулевого порядка описывается уравнением. Подставим значения и рассчитаем константы скорости реакции в разные моменты времени. Получили различные значения константы скорости, поэтому реакция имеет не нулевой порядок. Предположим, что реакция имеет первый порядок. Константа скорости реакции первого порядка описывается уравнением. Подставим значения и рассчитаем константы скорости реакции в разные моменты времени. Получили различные значения константы скорости, поэтому реакция имеет не первый порядок. Предположим, что реакция имеет второй порядок. Константа скорости реакции второго порядка описывается уравнением. Подставим значения и рассчитаем константы скорости реакции в разные моменты времени. Получили близкие значения константы скорости, поэтому реакция имеет второй порядок. 2) Для реакции второго порядка период полупревращения определяется по формуле Подставляем значения. 3) Определим концентрации исходных веществ к моменту времени τ = 12 мин. Для реакции второго порядка. Степень превращения равна: 41,0%.
Похожие готовые решения по химии:
- По значения констант скоростей реакции при двух температурах определите: 1) температурный коэффициент
- Определите структурную формулу углеводорода состава С8Н8, если известно, что он обесцвечивает
- Дайте обоснование реакциям подлинности фенола, приведенным в ФС Напишите их химизм и укажите внешний эффект
- Дайте обоснование определению примеси сульфатов в сульфадиметоксине в соответствии с требованиями ФС (Приложения № 3, 7)
- Вычислите поверхностное натяжение толуола при 50 ºС, если при медленном выпускании его из сталагмометра масса 38 капель составила 1,486 г. При выпускании из того же сталагмометра
- Вычислить электрофоретическую скорость частиц золя трехсернистого мышьяка, если ξ-потенциал частиц равен 89,5 мВ; разность потенциалов между электродами 240 В, расстояние
- Коллоидный раствор получен в результате реакции обмена при смешивании равных объемов растворов А и В, имеющих разные молярные концентрации эквивалента. Написать и объяснить формулу
- Порог коагуляции золя гидроксида алюминия дихромат-ионами равен 0,63 ммоль/л. Какой объем 10%-ного раствора дихромата калия (плотность 1,07 г/мл) требуется для коагуляции
- Вероятность заболевания вакцинированного животного составляет 𝑝. Какова вероятность того, что из 𝑛 вакцинированных животных
- ДСВ 𝑋 имеет распределение Пуассона с параметром, равным 2. Найти вероятность того, что ДСВ 𝑋 принимает значение
- Задана интенсивность простейшего потока 𝜆=5. Найти: а) математическое ожидание; б) дисперсию; в) среднее квадратическое отклонение
- По значения констант скоростей реакции при двух температурах определите: 1) температурный коэффициент

