
Запишите в тетрадь уравнение реакции вашего варианта (см. табл.): 9. для обратимой газофазной реакции рассчитайте стандартное изменение энергии
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16722 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
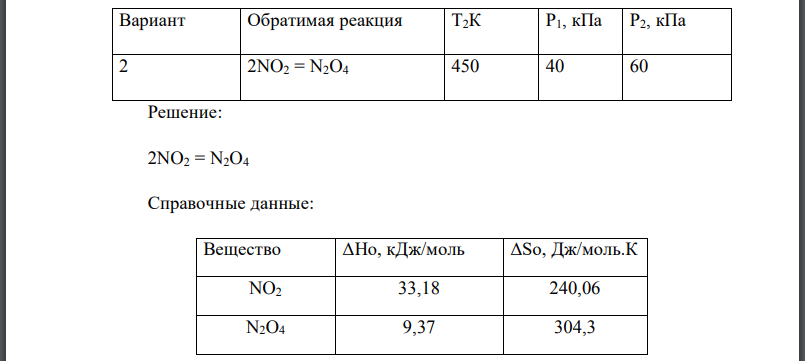
Запишите в тетрадь уравнение реакции вашего варианта (см. табл.): 9. для обратимой газофазной реакции рассчитайте стандартное изменение энергии Гиббса для: б) Т2 и значения констант равновесия для обеих температур; 10. определите направление протекания реакции при этих температурах: а) из стандартного состояния; б) при следующих начальных условиях: давление каждого из исходных веществ равно Р1, давление каждого из продуктов реакции равно 11. рассчитайте равновесные давления и концентрации всех компонентов равновесной системы при температуре предложите способы увеличения концентрации продуктов в равновесной смеси. При ответах на вопросы можно допустить: не зависят от температуры; б) ко всем газообразным компонентам системы применимы законы идеальных газов. Вариант Обратимая реакция
Решение:
Справочные данные: Вещество Учитывая, что изменения энтальпии и энтропии реакции на зависят от температуры, определим изменение энергии Гиббса реакции по формуле а) Изменение энергии Гиббса при б) Изменение энергии Гиббса при равно Рассчитаем константу равновесия реакции Получаем Константу равновесия определим по формуле Получаем константа равновесия поэтому реакция протекает в прямом направлении. При 450 К константа равновесия поэтому реакция протекает в обратном направлении. 96 б) Вычислим константу равновесия Кр по заданным значениям давлений компонентов реакционной смеси. Константа равновесия поэтому реакция протекает в обратном направлении. 3. Рассчитаем равновесные давления при 450 К. Примем, что исходное давление равно Тогда Получаем Решаем уравнение, получаем Рассчитаем равновесные концентрации. Примем, что объем реакционной смеси равен Тогда Получаем Решаем уравнение, получаем Увеличение концентрации продукта возникает при смещении равновесия вправо. В соответствии с принципом Ле-Шателье этому способствуют повышение давления, понижение температуры, добавление в реакционную смесь исходных веществ и вывод из реакционной смеси продукта реакции.

Похожие готовые решения по химии:
- По зависимости давления насыщенного пара от температуры и плотности данного вещества А с молекулярной массой М в твердом и жидком состояниях
- При температуре Т давление пара раствора концентрации с неизвестного нелетучего вещества в жидком растворителе равно Р Па; плотность этого раствора d. Зависимость
- Запишите в тетрадь уравнение реакции вашего варианта (см. табл.): 14. для обратимой газофазной реакции рассчитайте стандартное изменение энергии
- По зависимости давления насыщенного пара от температуры и плотности данного вещества А с молекулярной массой М в твердом и жидком состояниях в тройной точке
- Определите среды после реакции. После завершения реакции в растворе присутствуют вещества: На реакцию среды могут влиять и не гидролизуется
- Запишите в тетрадь уравнение реакции вашего варианта (см. табл.): 1. для обратимой газофазной реакции рассчитайте стандартное изменение энергии
- При температуре Т давление пара раствора концентрации с неизвестного нелетучего вещества в жидком растворителе равно Р Па; плотность этого
- При температуре Т давление пара раствора концентрации с неизвестного нелетучего вещества в жидком растворителе равно Р Па; плотность этого раствора
- Объясните, какой из комплексных ионов [HgCl4] 2- , [HgBr4] 2- , [HgI4] 2-
- Четыре одинаковые металлические пластины площадью S=30 см2 расположены на одинаковом расстоянии друг от друга d=1,5 мм. Пространство между второй
- Определите концентрации ионов серебра и хлорид-ионов в 1 М растворе
- Напишите уравнения диссоциации следующих комплексных соединений

