
Кондуктометрическое титрование. Сущность метода. Типы кривых кондуктометрического титрования. Понятие о высокочастотном кондуктометрическом титровании. Применение кондуктометрического
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16873 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Кондуктометрическое титрование. Сущность метода. Типы кривых кондуктометрического титрования. Понятие о высокочастотном кондуктометрическом титровании. Применение кондуктометрического титрования. Достоинства и недостатки метода.
Ответ:
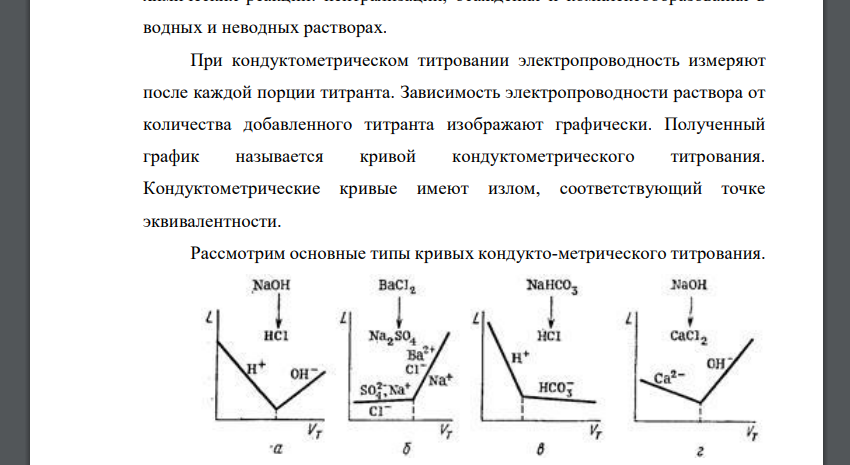
Кондуктометрическое титрование - один из методов объемного химического анализа, при котором точка эквивалентности устанавливается кондуктометрическим методом. В кондуктометрическом титровании для анализа индивидуальных веществ и разнообразных смесей используются самые различные типы химических реакций: нейтрализации, осаждения и комплексообразования в водных и неводных растворах. При кондуктометрическом титровании электропроводность измеряют после каждой порции титранта. Зависимость электропроводности раствора от количества добавленного титранта изображают графически. Полученный график называется кривой кондуктометрического титрования. Кондуктометрические кривые имеют излом, соответствующий точке эквивалентности. Рассмотрим основные типы кривых кондуктометрического титрования. Титруемое вещество и титрант имеют ионы с высокой подвижностью. При титровании, например, НСl раствором NaOH (рисунок а) в растворе сначала присутствуют Н+ – ионы, имеющие высокую подвижность, по мере титрования их концентрация уменьшается и электрическая проводимость раствора падает. В точке эквивалентности электрическая проводимость раствора минимальна. При добавлении избытка NaOH в растворе появляются свободные ОН- – ионы, имеющие высокую подвижность, и электрическая проводимость раствора снова возрастает. Восходящий участок кривой титрования имеет меньший угол наклона вследствие более низкой подвижности ионов ОН- . Титруемое вещество и титрант имеют ионы с низкой подвижностью. Например, при титровании Na2SO4 раствором ВаСl2 электрическая проводимость раствора до точки эквивалентности практически неизменна (рисунок б), так как малоподвижные SO4 2- -ионы связываются в сульфат бария и заменяются Сl- – ионами с близкой подвижностью, количество Na+ остается неизменным. После точки эквивалентности вследствие появления избытка Ba2+– и Сl- – ионов электрическая проводимость раствора возрастает. Титруемое вещество имеет ионы с высокой подвижностью, титрант – с низкой. В этом случае до точки эквивалентности электрическая проводимость раствора снижается, после точки эквивалентности – изменяется незначительно (в). Примером здесь может служить титрование НСl раствором NaHCO3. Титруемое вещество имеет ионы с низкой подвижностью, титрант – с высокой. Например, при титровании СаСl2 раствором NaOH электрическая проводимость раствора сначала несколько уменьшается вследствие замены ионов Са2+, связываемых в осадок Са(ОН)2 на Na+ , затем возрастает при появлении избытка ОН –ионов (рисунок г). Кривые кондуктометрического титрования могут искажаться вследствие гидролиза и других причин. Высокочастотное кондуктометрическое титрование – метод, который основан на измерении электропроводности при частотах несколько МГц. Существенное отличие высокочастотного титрования от низкочастотного заключается в том, что электроды можно расположить на наружных стенках сосуда – кондуктометрической ячейки. Это отличие важно при работе с агрессивными средами (царская водка, олеум). Этот метод точен и дает возможность измерить электропроводность любых сред. Достоинства кондуктометрического титрования: - титрование можно проводить в мутных, окрашенных, непрозрачных средах; - высокая чувствительность и малая погрешность определения; - анализ можно автоматизировать. Недостатки кондуктометрического титрования: - малая селективность. Применение кондуктометрического титрования: - титрование сильных и слабых кислот, оснований, аминов в широком диапазоне концентраций; - определение многих катионов (Fе3+, Сu2+, Ni2+ и др.) и анионов (Cl- , Br- , I- , оксалат, тартрат, салицилат и др.), общей жесткости

Похожие готовые решения по химии:
- Рассчитать селективность хроматографической колонки и коэффициент разделения, если при хроматографировании были получены 2 пика: - первый пик – время удерживания
- По представленной хроматограмме рассчитать времена удерживания компонентов, количетво теоретических тарелок, ВЭТТ, коэффициент разделения и селективности. (длина колонки 50 м
- Сформулируйте второй закон Коновалова. Приведите две диаграммы кипения в координатах t-состав с точкой "min" и "max" на кривой
- Поверхностно-активные и поверхностно-инактивные вещества. Структура и свойства поверхностно-активных веществ. Свойства поверхностно-инактивных веществ. Изотермы поверхностного
- Составьте формулы трех изомерных трипептидов из следующих αаминокислот: алифатических диамино-, гидроксиамино- и ароматической. Назовите. Дайте определение белкам
- Качественные реакции на α-аминокислоты, пептиды, белки: биуретовая, нингидриновая, ксантопротеиновая и цистеиновая реакции.
- Вычислить количество анилина, образующегося из 100 г нитробензола и 4 г водорода при 95%-ном выходе. Какое
- Хроматоскопия. Методы экспериментального получения хроматографических спектров. Понятие о хроматографическом спектре. Использование спектров для групповой и
- Хроматоскопия. Методы экспериментального получения хроматографических спектров. Понятие о хроматографическом спектре. Использование спектров для групповой и
- Вычислить количество анилина, образующегося из 100 г нитробензола и 4 г водорода при 95%-ном выходе. Какое
- По представленной хроматограмме рассчитать времена удерживания компонентов, количетво теоретических тарелок, ВЭТТ, коэффициент разделения и селективности. (длина колонки 50 м
- Рассчитать селективность хроматографической колонки и коэффициент разделения, если при хроматографировании были получены 2 пика: - первый пик – время удерживания

