
Перегонка (дистилляция) бинарных жидких смесей (определение). Перечислите виды перегонок, укажите основную закономерность, описывающую явление, на котором
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16875 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Перегонка (дистилляция) бинарных жидких смесей (определение). Перечислите виды перегонок, укажите основную закономерность, описывающую явление, на котором основана перегонка. Приведите диаграмму кипения для идеальной смеси и укажите состав остатка и дистиллята при ректификации в оптимальных условиях смеси произвольного состава.
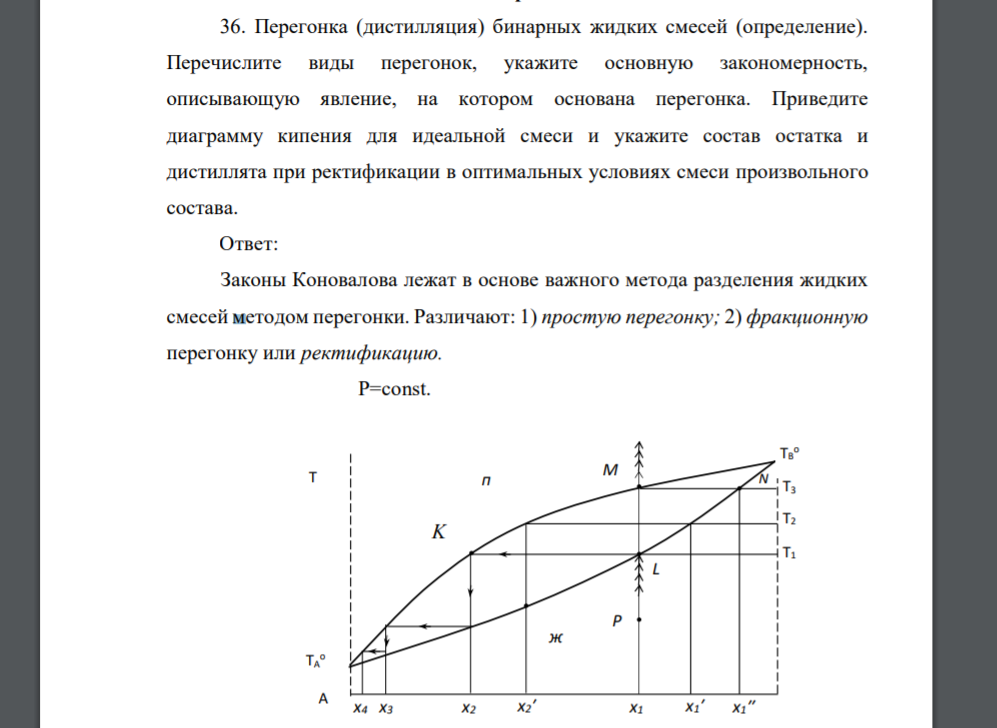
Ответ: Законы Коновалова лежат в основе важного метода разделения жидких смесей методом перегонки. Различают: 1) простую перегонку; 2) фракционную перегонку или ректификацию. Простая перегонка заключается в нагревании смеси жидкостей с отводом образующегося пара, и последующей его конденсацией. При такой перегонке разделить смесь, состоящую из двух летучих компонентов, не представляется возможным, так как пар и жидкость содержат оба компонента. Однако можно отобрать пар, обогащенный более летучим компонентом, получив при том в остатке жидкость с более высоким, по сравнению с исходной жидкостью, содержанием высококипящего компонента. Рассмотрим систему, подчиняющуюся закону Рауля. Допустим, что т.е. компонент А - более летучий (рис.). При нагревании до Т1 (температура начала кипения) исходной жидкой смеси образуется пар состава x2, сконденсировав который можно получить жидкость с увеличенным, по сравнению с исходным составом, содержанием более летучего компонента А. Если пар не отбирать, то при дальнейшем нагреве температура кипения жидкости повышается, так как состав исходной смеси обогащается менее летучим компонентом. Изменение состава жидкости в процессе кипения смеси будет происходить по линии жидкости LN, а равновесного с ней пара - вдоль линии пара КМ. Жидкость состава x1′ будет кипеть при более высокой температуре Т2 , а пар, отвечающий этой жидкости будет иметь состав x2′ . Жидкость состава x1′′ будет кипеть при температуре Т3, а пар будет иметь состав x1. При достижении температуры T3 состав пара будет отвечать составу исходной жидкости. При этой температуре пар конденсируют и перегонку в равновесии заканчивают, так как конденсат при дальнейшем нагревании будет содержать меньше более летучего компонента А, чем исходная смесь. Если ограничить кипение интервалом температур для исходной смеси состава x1, то можно получить в остатке жидкость состава x1′ с увеличенным содержанием высококипящего компонента и собрать конденсат промежуточного состава между обогащенный более летучим компонентом А. Собранный конденсат отвечает некоторому интервалу концентраций и называется фракцией. Простая перегонка целесообразна лишь при очень большой разнице в составах пара и жидкости. Приближенно эта разница характеризуется различием в температурах кипения чистых компонентов. Чаще всего простую перегонку используют при очистке веществ от небольшого количества примесей и тогда, когда не требуется высокой степени очистки получаемых продуктов. Более эффективным методом разделения веществ является фракционная перегонка, которая состоит в многократном повторении процессов испарения и конденсации. При этом соблюдается следующая последовательность операций: 1) нагревание исходной жидкой смеси до кипения для получения некоторого количества пара определенного состава; 2) конденсация полученного пара; 3) нагревание конденсата для получения пара нового состава, обогащенного легколетучим компонентом. Например, пар состава х2 может быть сконденсирован с получением жидкости такого же состава. При ее испарении образуется пар состава х3 с увеличенным содержанием более летучего компонента А. Этот конденсат может быть снова подвергнут кипению с образованием пара состава х4 и так далее. В результате многократного повторения последовательных процессов испарения и конденсации может быть достигнуто практически полное выделение легколетучего компонента из раствора. Число таких ступенек будет тем меньше, чем больше различие в составах жидкости и пара, находящихся в равновесии. На практике разделение смесей проводят непрерывной фракционной перегонкой, называемой ректификацией. Ректификация - сложный неравновесный процесс, в ходе которого происходит непрерывный обмен веществом между потоками жидкости и пара. Процесс осуществляется в специальных аппаратах - ректификационных колоннах. При их эффективной конструкции и правильно выбранном режиме работы достигается почти полное разделение смеси.
Похожие готовые решения по химии:
- Адсорбция на границе раздела жидкость-газ и жидкость-жидкость. Уравнение Гиббса, его анализ. Изотерма адсорбции, ее анализ. Строение адсорбционного слоя на границе
- Вычислите, используя данные табл.1, тепловой эффект (ΔНºr) реакции С2Н6(г) = С2Н4(г) + Н2(г) при 150ºС считая, что в интервале температур от 25ºС до 150ºС теплоемкость участников реакции постоянна
- При распределении янтарной кислоты, взятой в разных количествах, между водой и эфиром при 25ºС были получены следующие данные: равновесные концентрации янтарной кислоты
- Вычислите предельную молярную электрическую проводимость бензойной кислоты, если предельная молярная электрическая проводимость электролитов NaBr, HBr и C6H5COONa соответственно
- Сравните поверхностную активность пропионовой и масляной кислот в водных растворах в данном интервале концентраций, если известно: Выполняется ли правило
- Вычислить по среднему квадратичному сдвигу частичек гуммигута постоянную Авогадро NA, если радиус частиц 0,212 мкм, а за 1 минуту частица
- Коллоидный раствор получен в результате реакции обмена при смешивании равных объемов растворов А и В, имеющих разные молярные концентрации
- Рассчитайте молекулярную массу полистирола, если осмотическое давление при 25°С равно 120,9 Па, а массовая концентрация – 4,176 кг/м3 ; β = 1.
- Навеску смеси KCl и NaCl массой 1,479 г растворили в мерной колбе вместимостью 250,0 мл. К 25,00 мл полученного раствора прилили
- На титрование 20,00 мл раствора хлорида никеля (II) израсходовано 21,22 мл 0,02065 М раствора трилона Б. Определите концентрацию (г/мл)
- Конкурентный рыночный механизм — это способ: а) Согласования решений потребителей, производителей и владельцев факторов производства
- Вычислите ожидаемую доходность и риск акции. Сделайте вывод о необходимости приобретения акции, если сегодня акция стоит 30,25 руб

