
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Проставьте степени окисления элементов в исходных веществах и продуктах реакции KBr + KMnO4 + H2O = Br2 + MnO2 + KOH KBr Br
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16953 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
Проставьте степени окисления элементов в исходных веществах и продуктах реакции. 2. Укажите элементы, меняющие степень окисления в ходе реакции. 3. Составьте электронные уравнения реакций окисления и восстановления, укажите окислитель и восстановитель. 4. Проведите баланс электронов и найдите основные коэффициенты. 5. Проставьте найденные коэффициенты в уравнении реакции перед окислителем, восстановителем и продуктами их восстановления и окисления. 6. Исходя из баланса атомов, проставьте недостающие коэффициенты в левой и правой частях уравнения. 7. Докажите с точки зрения строения атома, какие свойства (окислительные, восстановительные или двойственные) может проявлять в реакциях указанный элемент в указанном веществе. № Уравнение Вещество Элемент 15 KBr + KMnO4 + H2O = Br2 + MnO2 + KOH KBr Br
Решение:
Степень окисления изменяют восстановление, окислитель окисление, восстановитель находится в низшей степени окисления поэтому в окислительно-восстановительных реакциях может проявлять свойства только восстановителя.

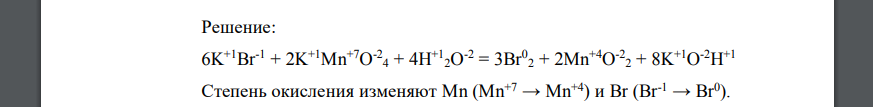
Похожие готовые решения по химии:
- Исходя из значений стандартных электродных потенциалов, сделайте вывод, какой из электродов является анодом, какой – катодом 15 Au, K
- Определите анодные и катодные участки. При необходимости подберите нужный металл согласно заданию Свинцовое изделие + катодное покрытие
- Приведите формулировки основных стехиометрических законов NO2 FeCl3
- дайте названия по формулам и укажите формулы по названиям сульфат алюминия; нитрат гидроксожелеза (II), карбонат гидроксоникеля
- Укажите характер связей в молекуле, для чего изобразите графическую формулу указанного соединения и рассчитайте NOF3 BeI2 Na2[BeF4]
- На основании агрегатных состояний веществ, участвующих в реакции, предположите, как должна меняться энтропия системы С2Н5ОН(ж)+2О2(г) = 2СО2(г)+3Н2О(г)
- Запишите выражение закона действия масс (ЗДМ) для уравнения реакции данного варианта Pb(NO3)2(ж)+2NaOH(ж)= Pb(OH)2(ж)+2NaNO3(ж)
- Запишите выражение для константы равновесия для заданного уравнения реакции СО(г)+ Н2О(г)= Н2(г)+ СО2(г)
- Составить примерный план анализа при подозрении на отравление Δ9 -тетрагидроканнабинолом (ТГК).
- Запишите выражение для константы равновесия для заданного уравнения реакции СО(г)+ Н2О(г)= Н2(г)+ СО2(г)
- Исходя из значений стандартных электродных потенциалов, сделайте вывод, какой из электродов является анодом, какой – катодом 15 Au, K
- Изолирование но-шпы проводили из 100 г биологического объекта методом Крамаренко (изолирование водой, подкисленной серной кислотой).

