
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Рассчитаем тепловой эффект реакции при постоянном давлении и Т = 298 К. 3Fe2O3 + CO
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16894 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
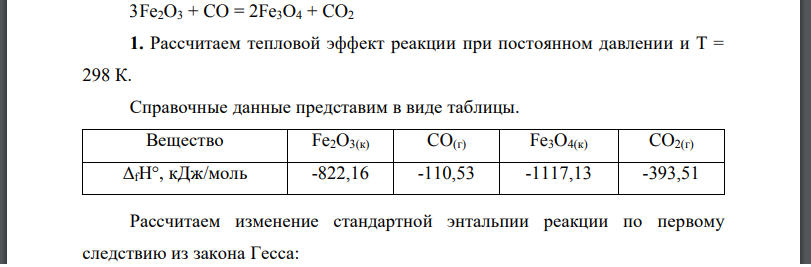
Рассчитаем тепловой эффект реакции при постоянном давлении и Т = 298 К. 3Fe2O3 + CO = 2Fe3О4 + CO2
Решение:
Справочные данные представим в виде таблицы. Вещество Рассчитаем изменение стандартной энтальпии реакции по первому следствию из закона Гесса: Тепловой эффект при постоянном давлении и температуре 298 К равен: Qp = 50,76 кДж
Похожие готовые решения по химии:
- Рассчитаем тепловой эффект реакции при постоянном объеме и Т = 298 К. 3Fe2O3 + CO
- Рассчитаем тепловой эффект реакции при постоянном давлении и Т = 800 К. 3Fe2O3 + CO
- Рассчитаем изменение энтропии при Т = 298 К. 3Fe2O3 + CO
- Рассчитаем изменение энтропии при 800 К. Эта величина равна разности абсолютных энтропий продуктов реакции
- Рассчитаем константу равновесия при 1100 К
- Рассчитаем изменение энергии Гиббса при заданной температуре и составе газовой фазы
- Реакция С + О2 = СО2 протекает на внутренней поверхности угольного канала, по которому протекает воздух. Измеренная константа скорости
- Поверхностное натяжение σ водного раствора масляной кислоты при t = 18 0C подчиняется эмпирическому уравнению σ0 – σ = 29,8·10-3 ·ln(1 + 19,64·С), где
- Рассчитайте содержание ингредиентов в порошке: Папаверина гидрохлорида 0,02; Глюкозы 0,2
- Эффект дохода возникает в связи с тем, что: А) снижение цены товара увеличивает при прочих равных условиях реальный доход
- Напишите на латинском языке состав лекарственной формы: Раствора цинка сульфата 0,25% - 15,0 Кислоты борной 0,3 Предложите методики качественного и количественного анализа
- Напишите структурные формулы изомеров соединений заданного состава (учесть все виды изомерии). Назовите их. Молочная кислота; 1,3-дихлорциклопентан.

