
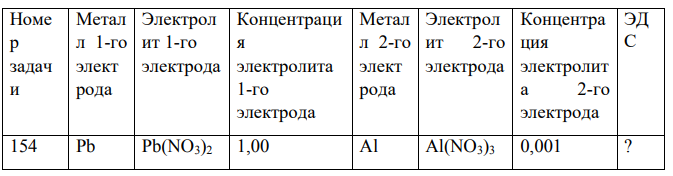
Составьте схему гальванического элемента, напишите электронные уравнения электродных процессов и суммарное уравнение соответствующей окислительно
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17021 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
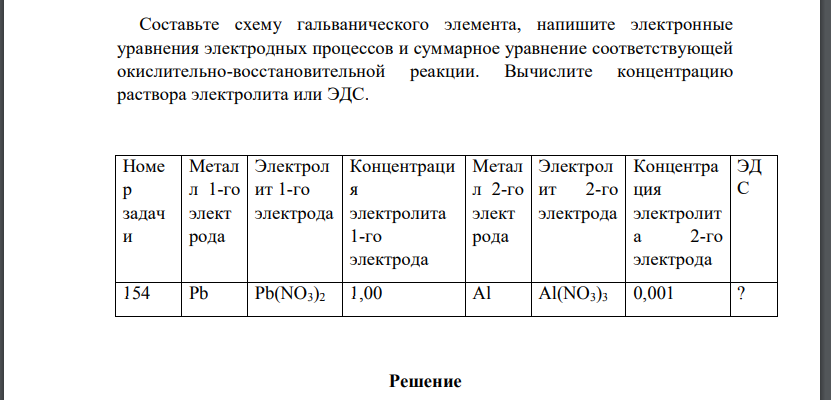
Составьте схему гальванического элемента, напишите электронные уравнения электродных процессов и суммарное уравнение соответствующей окислительно-восстановительной реакции. Вычислите концентрацию раствора электролита или ЭДС.
Решение
Гальванический элемент - это электрохимическая система, в которой энергия окислительно-восстановительной реакции трансформируется в электрическую энергию, т.е. такая система служит в качестве химического источника тока. Анодный процесс заключается в окислении металла, характеризующегося более отрицательной величиной электродного потенциала в катодном процессе участвует частица-окислитель, присутствующая в катодном электролите. Для металлов, приведенных в условии задачи:

Похожие готовые решения по химии:
- Как будет происходить электролиз водного раствора электролита HgCl2? Приведите уравнение диссоциации электролита и поясните возможность
- На основании положения химического элемента № 52 и его электронной формулы составьте прогноз его химических свойств, ответив на следующие вопросы:
- Определите тип химической связи (неполярная ковалентная, полярная ковалентная или ионная) в веществах тетрабромид углерода и бромид бария
- Вычислите стандартные величины H 0 298, S 0 298 и G 0 298 для реакции: 2NO(г) + Br2(г) = 2NOBr(г)
- Составьте схему гальванического элемента, напишите электронные уравнения
- Как будет происходить электролиз водного раствора электролита AlCl3? Приведите уравнение диссоциации электролита и поясните возможность участия
- На основании положения химического элемента № 13 и его электронной формулы составьте прогноз его химических свойств, ответив на следующие
- Для реакций: 1) H2C2O4 + KClO3 → K2CO3+ CO2+ ClO2 + H2O 2) NH4NO2 → N2 + H2O
- 1.Приведите уравнения реакций количественного определения пирацетама (Mr 142,2) методом Кьельдаля
- Для реакций: 1) H2C2O4 + KClO3 → K2CO3+ CO2+ ClO2 + H2O 2) NH4NO2 → N2 + H2O
- Приведите уравнения реакций количественного определения дикаина (тетракаина гидрохлорида)
- Как будет происходить электролиз водного раствора электролита HgCl2? Приведите уравнение диссоциации электролита и поясните возможность

