
Во влажном воздухе находятся две железные пластинки. Часть поверхности одной из них покрыта оловом, а часть поверхности другой – медью. Как происходит коррозия в том и другом случае? Составьте электронные уравнения анодных и катодных процессов. Какие продукты при этом образуются
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Во влажном воздухе находятся две железные пластинки. Часть поверхности одной из них покрыта оловом, а часть поверхности другой – медью. Как происходит коррозия в том и другом случае? Составьте электронные уравнения анодных и катодных процессов. Какие продукты при этом образуются?
Электрохимическая коррозия металлов происходит в среде электролита (растворы кислот, щелочей, солей, влажный воздух) и может быть представлена как совокупность анодного (окисление) и катодного (восстановление) процессов.
При контакте металлов разной электрохимической активности коррозионному разрушению в первую очередь подвергается металл с наиболее отрицательной величиной электродного потенциала E0 . При этом такой металл выполняет функции анода в электрохимической системе и окисляется.
Электронное уравнение анодного процесса можно представить в общем виде:
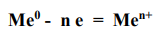
Рассмотрим железную пластину, покрытую оловом. Из двух металлов анодом является Fe, т.к. его электродный потенциал (E0 = -0,44 В) является величиной более отрицательной, чем электродный потенциал Sn (Е0 = -0,14 В). Следовательно, в данном случае коррозионному разрушению будет подвергаться железная пластина. Анодный процесс имеет вид:
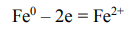
В катодном процессе при электрохимической коррозии участвуют частицы-окислители, находящиеся в электролите:

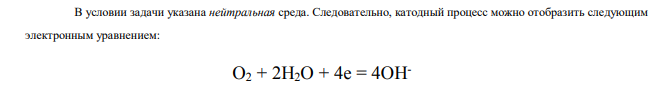
Продукты коррозии определяются результатами анодного и катодного процессов:
- в кислой среде выделяется газообразный водород и образуется соль металла-анода и кислоты, создающей среду;
- в нейтральной среде продуктом коррозии является гидроксид металлаанода (как результат взаимодействия катионов металла-анода и гидроксидионов, образующихся на катоде).
Во влажной среде протекает превращение:
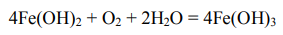
В рассматриваемой в задаче системе продуктами коррозии являются: Fe(OH)3.
Рассмотрим железную пластину, покрытую медью. Из двух металлов анодом является Fe, т.к. его электродный потенциал (E0 = -0,44 В) является величиной более отрицательной, чем электродный потенциал Cu (Е0 = +0,35 В). Следовательно, в данном случае коррозионному разрушению будет подвергаться железная пластина. Анодный процесс имеет вид:
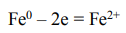
Катодный процесс::
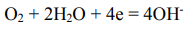
Во влажной среде протекает превращение:
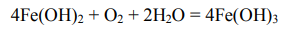
В рассматриваемой в задаче системе продуктами коррозии являются: Fe(OH)3.

Похожие готовые решения по химии:
- На основании положения химического элемента № 49 и его электронной формулы составьте прогноз его химических свойств, ответив на следующие вопросы
- Определите тип химической связи (неполярная ковалентная, полярная ковалентная или ионная) в веществах нитрид лития и дихлорид серы. В случае полярной или ионной связи укажите направление смещения электронов
- Изделие, изготовленное из стали, эксплуатируется в нейтральном растворе хлорида натрия. Какие металлы можно использовать в качестве протектора? Приведите электронные уравнения анодного и катодного процессов для одного из протекторов
- Как будет происходить электролиз водного раствора электролита KBr? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях
- Определите тип химической связи (неполярная ковалентная, полярная ковалентная или ионная) в веществах бромид лития и теллуроводород. В случае полярной или ионной связи укажите направление смещения электронов
- Пpоизведите необходимые вычисления и найдите недостающие величины, обозначенные знаком "?" в стpоке табл.6, соответствующей номеpу Вашей задачи (все pаствоpы – водные
- Составьте уравнения методом электронного баланса. Для каждой реакции укажите, какое вещество является окислителем, а какое – восстановителем и за счет каких атомов. Определите типы данных окислительновосстановительных реакций
- Составьте схему гальванического элемента, напишите электронные уравнения электродных процессов и суммарное уравнение соответствующей окислительно-восстановительной реакции. Вычислите концентрацию раствора электролита или ЭДС
- Составьте схему гальванического элемента, напишите электронные уравнения электродных процессов и суммарное уравнение соответствующей окислительно-восстановительной реакции. Вычислите концентрацию раствора электролита или ЭДС
- Составьте уравнения методом электронного баланса. Для каждой реакции укажите, какое вещество является окислителем, а какое – восстановителем и за счет каких атомов. Определите типы данных окислительновосстановительных реакций
- Организация в соответствии с заключенными контрактами должна была поставить на экспорт в отчетном периоде 1000 ед. товара по цене 200
- На основании положения химического элемента № 49 и его электронной формулы составьте прогноз его химических свойств, ответив на следующие вопросы

