
Вычислите, сколько граммов кислоты (Z) содержится в 500 см3 раствора, если на титрование 25 см3 этого раствора расходуется Х см3 раствора гидроксида натрия с заданной молярной концентрацией эквивалент
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16852 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
а) Вычислите, сколько граммов кислоты (Z) содержится в 500 см3 раствора, если на титрование 25 см3 этого раствора расходуется Х см3 раствора гидроксида натрия с заданной молярной концентрацией эквивалента Y (табл.15). X,Y Гидроксид натрия Z Кислоты Концентрация, моль/дм3 Объем, см3 X Y Z 0 1 2 3 Уксусная Щавелевая Янтарная Бензойная 0,1085 0,1170 0,1250 0,1395 24,50 23,25 21,85 21,05 4 5 6 7 8 9 Винная Серная Яблочная Фталевая Азотная Соляная 0,1305 0,1460 0,1550 0,1615 0,1705 0,1825 20,15 18,75 17,55 16,45 15,90 15,10 б) Рассчитайте массу окислителя (Z) в растворе, если после его замещения на I действием избытка KI и кислоты (либо иодата калия) на титрование затрачено Х см3 раствора тиосульфата натрия с указанным титром Y (табл.16). X Окислители Тиосульфат натрия Y Титр, Т.103 ,г/см3 Объем, см3 Z Z Y X 0 1 2 3 4 5 6 7 8 9 Na2S2O3 KBrO4 H2O2 HNO3 KClO4 MnO2 K2Cr2O7 HNO3 KMnO4 PbO2 3,226 3,971 4,716 5,212 5,957 6,701 7,446 8,190 8,935 9,679 25,00 26,50 28,00 29,50 31,00 32,50 34,00 35,50 37,00 38,50
Решение: А) По закону эквивалентов: Ответ: Б) По закону эквивалентов Ответ:
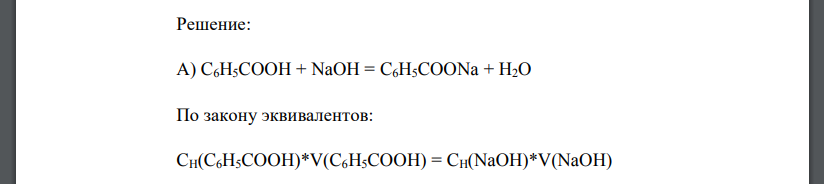
- Рассчитайте содержание (в массо-объемной процентной концентрации) H2SО4, если на титрование 5 см3 раствора H2SО4 израсходовано
- Сколько NaI содержалось в навеске 0,3010 г, если на ее титрование израсходовано 15,6 см3 0.11 н. раствора AgNO3?
- Приведите уравнения реакций количественного определения гексаметилентетрамина (метенамина) в таблетках и растворе для инъекций по
- Приведите уравнения реакций количественного определения анестезина (бензокаина) (Mr 165,19) методом нитритометрии. Укажите переход окраски

