
Рассчитайте материальный баланс процесса очистки сточных вод в количестве 16 м 3 /ч. В сточных водах содержится 620 мг/дм3 взвешенных веществ, 95 мг/дм3 сульфида натрия
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16951 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Рассчитайте материальный баланс процесса очистки сточных вод в количестве 16 м 3 /ч. В сточных водах содержится 620 мг/дм3 взвешенных веществ, 95 мг/дм3 сульфида натрия. Для полного осаждения сульфидов вводят раствор Fe2(SO4)3 с концентрацией 14% и дополнительно 185 мг/дм3 сульфата железа в качестве коагулянта для полного осаждения взвешенных веществ. Образующуюся серную кислоту нейтрализуют известковым молоком (10 г/дм3 Ca(OH)2). Оседающий шлам имеет влажность 97,6%. Степень выделения взвешенных веществ 96 %, сульфидов — до остаточной концентрации 0,2 мг/дм3, а содержание гипса в очищенной воде 0,2 % масс.
Решение:
Рассчитаем количество коагулянта Fe2(SO4)3 для осаждения взвешенных частиц: 16м3 /ч∙0,185кг/м3 = 2,96 кг/ч. Осаждение сульфидов:
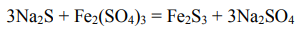
Масса сульфида натрия: 16м 3 /ч∙0,095кг/м 3 = 1,52 кг/ч Для осаждения такого количества сульфида натрия потребуется
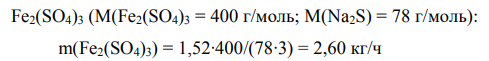
Масса раствора Fe2(SO4)3 равна: 2,60/0,14 = 18,57 кг/ч Гидролиз коагулянта:
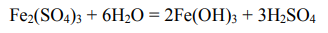
Масса Fe2(SO4)3 для осаждения взвешенных частиц: 16м 3 /ч∙0,185кг/м 3 = 2,96 кг/ч Масса образовавшегося Fe(OH)3 (M(Fe2(SO4)3 = 400 г/моль; М(Fe(OH)3) = 107 г/моль):
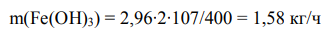
Масса образовавшейся кислоты H2SO4 (M(Fe2(SO4)3 = 400 г/моль; М(H2SO4) = 98 г/моль):
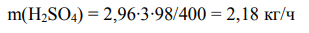
Нейтрализация серной кислоты:
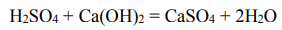
Масса образовавшегося CaSO4 (M(CaSO4) = 136 г/моль; М(H2SO4) = 98 г/моль):
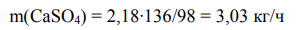
При введении коагулянта в шлам переходит взвешенных веществ: 16м3 /ч∙0,620кг/м3 ∙0,96 = 9,52 кг/ч. Кроме того, в шлам полностью перейдет образовавшийся Fe(OH)3 – 1,58 кг/ч и CaSO4: 0,998∙3,03 = 3,02 кг/ч. Таким образом, масса твердых частиц в шламе составит 9,52 + 1,58 + 3,02 = 14,12 кг/ч. При влажности шлама 97,6 % его масса составит 14,12/0,024 = 588,33 кг/ч. Все остальное составит массу осветленной воды. Остаточное содержание сульфидов: 16м3 /ч∙0,0002кг/м3 = 0,0032 кг/ч. Содержание гипса в очищенной воде: 15559,19∙0,002 = 31,12 кг/ч. 648 Сведем результаты в таблицу материального баланса отстойника. Таблица 1. Материальный баланс
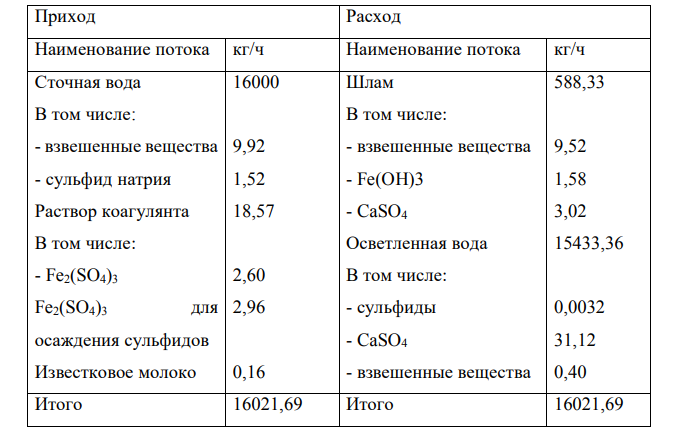
При решении задачи не учтено возможное частичное выделение СО2 и паров воды в газовую фазу.

Похожие готовые решения по химии:
- Рассчитайте экобаланс производства хлора для обеззараживания воды расход которой составил 225000 м3 /ч, если вводят дозу хлора 16 мг/м3 . Хлор производят методом электролиза раствора поваренной соли
- На очистку от нефтепродуктов поступают сточные воды, содержащие 80 мг/дм3 нефтепродуктов, причем 15 мг/дм3 растворенные, а остальные эмульгированные. pH стока 6,5. Очистку проводят реагентной напорной флотацией, а в качестве коагулянта используют 10 %-й раствор сульфата алюминия в дозах 70 мг/дм3 по оксиду
- Рассчитайте материальный баланс установки умягчения природной воды методом катионирования
- Выведите уравнение изотермы адсорбции Ленгмюра. Укажите условия его применимости
- Определите массу влажного шлама, выделенного из воды объемом V, если содержание взвешенных веществ в исходной воде
- В исходную сточную воду с pH = 8,2 для осаждения взвешенных веществ вводят коагулянт — гидроксохлорид алюминия
- В усреднитель поступает 11 м3 /ч сточной воды с pH = 10,5. В него же подают второй поток сточной воды с расходом 5 м3 /ч с pH = 3,1. Рассчитайте pH среды усредненного стока
- Определите ХПК исходной сточной воды и воды после фотохимического реактора, если на очистку подают сточную воду с расходом Q = 6 м3 /ч, содержащей фенол
- Определите ХПК исходной сточной воды и воды после фотохимического реактора, если на очистку подают сточную воду с расходом Q = 6 м3 /ч, содержащей фенол
- В усреднитель поступает 11 м3 /ч сточной воды с pH = 10,5. В него же подают второй поток сточной воды с расходом 5 м3 /ч с pH = 3,1. Рассчитайте pH среды усредненного стока
- На очистку от нефтепродуктов поступают сточные воды, содержащие 80 мг/дм3 нефтепродуктов, причем 15 мг/дм3 растворенные, а остальные эмульгированные. pH стока 6,5. Очистку проводят реагентной напорной
- Рассчитайте экобаланс производства хлора для обеззараживания воды расход которой составил 225000 м3 /ч, если вводят дозу хлора 16 мг/м3 . Хлор производят методом электролиза раствора поваренной соли

