
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Для приведенных элементов (см. задания в таблице 3): 1) укажите строение изотопов 12C, 13C, 14C
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16953 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
Для приведенных элементов (см. задания в таблице 3): 1) укажите строение изотопов; 2) приведите полные, сокращенные электронные формулы: а) атома и б) иона; 3) по приведенной характеристике определите элемент; 4) напишите, какие значения принимают 4 квантовых числа элемента, определенного по электронной формуле а) для формирующего электрона; б) для электронов внешнего квантового слоя; 5) объясните периодичность изменения указанной характеристики атома. № Укажите строение изотопов Запишите электронн ые. формулы Определите элемент Объясните периодичность изменения указанной характеристики атома 16 12C, 13C, 14C Si Si4- [ ]6s2 окислительные свойства
Решение:
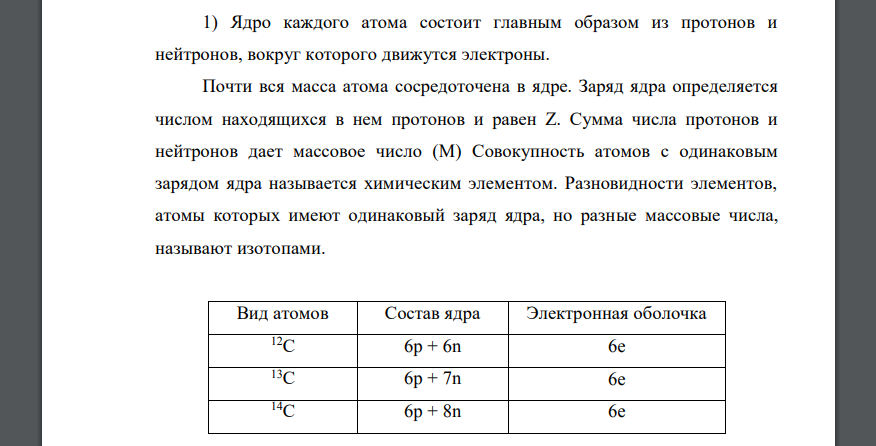
Ядро каждого атома состоит главным образом из протонов и нейтронов, вокруг которого движутся электроны. Почти вся масса атома сосредоточена в ядре. Заряд ядра определяется числом находящихся в нем протонов и равен Z. Сумма числа протонов и нейтронов дает массовое число Совокупность атомов с одинаковым зарядом ядра называется химическим элементом. Разновидности элементов, атомы которых имеют одинаковый заряд ядра, но разные массовые числа, называют изотопами. Вид атомов Состав ядра Электронная оболочка 2) Кремний: символ, порядковый номер, что равно общему числу электронов. полная электронная формула, сокращенная электронная формула. Ион содержит электронов. полная электронная формула – сокращенная электронная формула. 3) VI период, сумма внешних электронов (II группа, A подгруппа) − это 4) Формирующий электрон: Электрон внешнего электронного слоя: 5) Окислительные свойства определяются способностью атома элемента притягивать к себе электроны. По периоде слева направо увеличивается заряд ядра и уменьшается радиус атома, поэтому окислительные свойства увеличиваются. По группе сверху вниз увеличивается радиус атома, поэтому окислительные свойства уменьшаются

Похожие готовые решения по химии:
- Укажите характер связей в молекуле, для чего изобразите графическую формулу указанного соединения и рассчитайте K2CO3
- На основании агрегатных состояний веществ, участвующих в реакции, предположите, как должна меняться энтропия системы 2Fe(к) + O2(г) = 2FeO(к)
- Запишите выражение закона действия масс (ЗДМ) для уравнения реакции данного варианта 2H2(г) + O2(г) = 2H2O(г)
- Запишите выражение для константы равновесия для заданного уравнения реакции 2NO(г) + O2(г)= = 2NO2
- Проставьте степени окисления элементов в исходных веществах и продуктах реакции NO + KMnO4 + H2SO4 = MnSO4 + NO2 + K2SO4 + H2O NO2 N
- Определите анодные и катодные участки. При необходимости подберите нужный металл согласно заданию Никелевое изделие + катодное покрытие
- Приведите формулировки основных стехиометрических законов
- дайте названия по формулам и укажите формулы по названиям иодид алюминия, ортофосфат магния; нитрат гидроксоцинка (II), оксид серебра
- Напишите в молекулярной и краткой ионной форме уравнения гидролиза солей. Если гидролиз идёт по стадиям
- дайте названия по формулам и укажите формулы по названиям иодид алюминия, ортофосфат магния; нитрат гидроксоцинка (II), оксид серебра
- Укажите характер связей в молекуле, для чего изобразите графическую формулу указанного соединения и рассчитайте K2CO3
- Рассчитать ЭДС следующих гальванических элементов: Pt, H2 | р-р с рН = 9 | | CdSO4 0,03 н. | Cd

