
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Получите 3-нитропентан и напишите для него реакции: с NaOH
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17039 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
- Получите 3-нитропентан и напишите для него реакции: с NaOH, c HNO2.
Ответ:
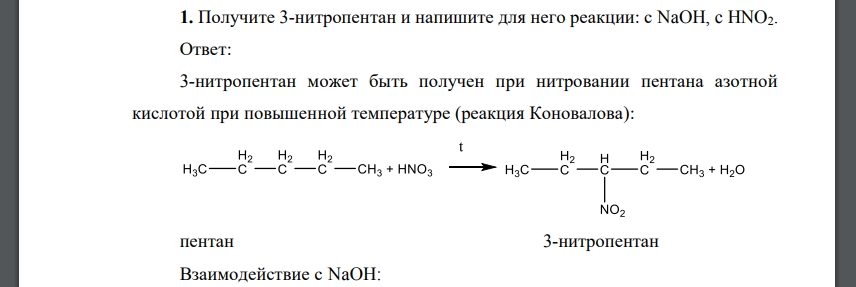
3-нитропентан может быть получен при нитровании пентана азотной кислотой при повышенной температуре (реакция Коновалова): Взаимодействие с NaOH: Взаимодействие с азотистой кислотой:
Похожие готовые решения по химии:
- Для 3-аминобутановой кислоты напишите реакции: с HCl, c NaOH, c C2H5OH (H
- Напишите формулу тетрапептида: Вал-Тир-Сер-Цис. Какие цветные реакции может проявить вышеприведенный
- Напишите формулу и название одного вторичного радикала на основе первого соединения. в) Напишите формулы двух ближайших
- Дайте названия заданных соединений. Определите, какие из них не существуют (неустойчивы), реагируют с NaOH
- Напишите структурную формулу соединения C5H10O3, растворимого в щелочах, а при нагревании образующего соединение C5H8O2
- Напишите структурные формулы изомеров соединений заданного состава (учесть все виды изомерии). Назовите их. Молочная кислота; 1,3-дихлорциклопентан.
- Предложите способ получения заданного амина. Напишите уравнения реакций с H2SO4 (с получением кислой и средней соли), HNO2
- Для заданных аминокислот напишите уравнения диссоциации в водном растворе, состояние ионизации в сильно кислой и сильно щелочной
- Чему равна энергия активации реакции, если при повышении температуры от 290 до 300 К скорость увеличится в 2 раза. Дано: 2 1 2 Т1 = 290 К Т2 = 300 К Еа - ?
- В три одинаковых земельных участка вложены капиталы по 1 млн.рублей. Первый наиболее плодородный, но расположен дальше остальных
- Для реакции: C2Cl4(г) + Cl2(г) = C2Cl6(г) составьте кинетическое уравнение;
- Вычислите равновесные концентрации реагентов для обратимого процесса А + B = C + D, если константа равновесия равна 1, а начальные концентрации (моль/л): [A] = 5; [B] = 3. Дано

