
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Пользуясь зависимостью между временем полураспада и начальным давлением, определите порядок реакции
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16707 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
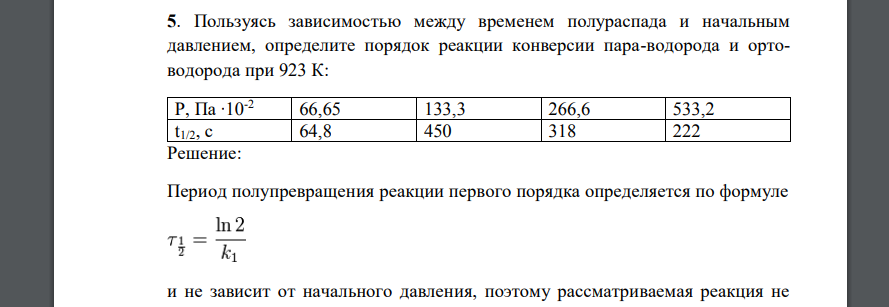
Пользуясь зависимостью между временем полураспада и начальным давлением, определите порядок реакции конверсии пара-водорода и ортоводорода при 923 К: Р, Па ∙10-2 66,65 133,3 266,6 533,2 t1/2, с 64,8 450 318 222
Решение:
Период полупревращения реакции первого порядка определяется по формуле и не зависит от начального давления, поэтому рассматриваемая реакция не является реакцией первого порядка. Для реакции второго порядка: Т.е. должна наблюдаться линейная зависимость периода полупревращения от Зависимость является линейной, поэтом рассматриваемая реакция имеет второй порядок.
Решение:
Период полупревращения реакции первого порядка определяется по формуле и не зависит от начального давления, поэтому рассматриваемая реакция не является реакцией первого порядка. Для реакции второго порядка: Т.е. должна наблюдаться линейная зависимость периода полупревращения от Зависимость является линейной, поэтом рассматриваемая реакция имеет второй порядок.
Похожие готовые решения по химии:
- Скорость реакции разложения N2O5 в CCl4 изучали, измеряя объем х кислорода, выделяющегося через различные промежутки времени
- Рассчитать ЭДС медно-цинкового ГЭ, в котором концентрация Cu2+ равна 0,001 н и Zn2+ - 0,1 н. Значения Е0 равны
- Рассчитайте константу равновесия реакции ZnSO4 + Cd = CdSO4 + Zn при 25 0С по данным о стандартных электродных потенциалах
- ЭДС элемента, в котором обратимо протекает реакция 0,5Hg2Cl2 + Ag = AgCl + Hg равна 0,456 В при 298 К и 0,439 В при 293 К. Рассчитайте
- Напишите структурную формулу алкина, изомерного приведенному диену, имеющему тот же самый углеродный скелет
- Напишите стадии механизма реакции электрофильного присоединения на примере гидробромирования (1 моль реагента) алкадиена
- Напишите уравнение реакции хлорирование (1 моль) ароматического УВ учитывая ориентирующее действие имеющейся группы
- Для реакции 2N2O = 2N2 + O2 константа скорости при 986 К равна 6,72 л/моль∙мин, а при 1165 К – 977,0 м/моль∙мин. Найдите энергию активации
- Для реакции 2N2O = 2N2 + O2 константа скорости при 986 К равна 6,72 л/моль∙мин, а при 1165 К – 977,0 м/моль∙мин. Найдите энергию активации
- Напишите уравнение реакции хлорирование (1 моль) ароматического УВ учитывая ориентирующее действие имеющейся группы
- Рассчитать ЭДС медно-цинкового ГЭ, в котором концентрация Cu2+ равна 0,001 н и Zn2+ - 0,1 н. Значения Е0 равны
- Скорость реакции разложения N2O5 в CCl4 изучали, измеряя объем х кислорода, выделяющегося через различные промежутки времени

