
Рассчитайте массу навески стандартного вещества (Z), необходимую для приготовления указанного объема раствора(Y) с заданной молярной концентрацией эквивалента Х
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16852 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
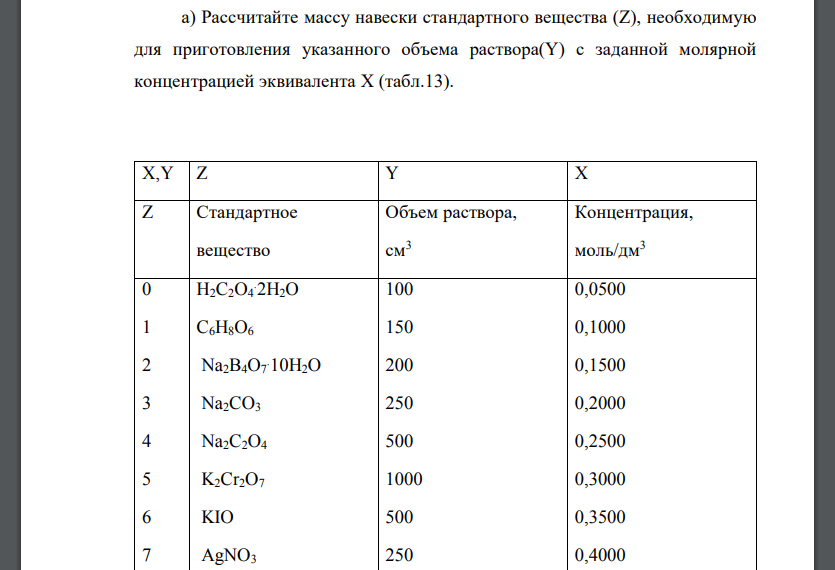
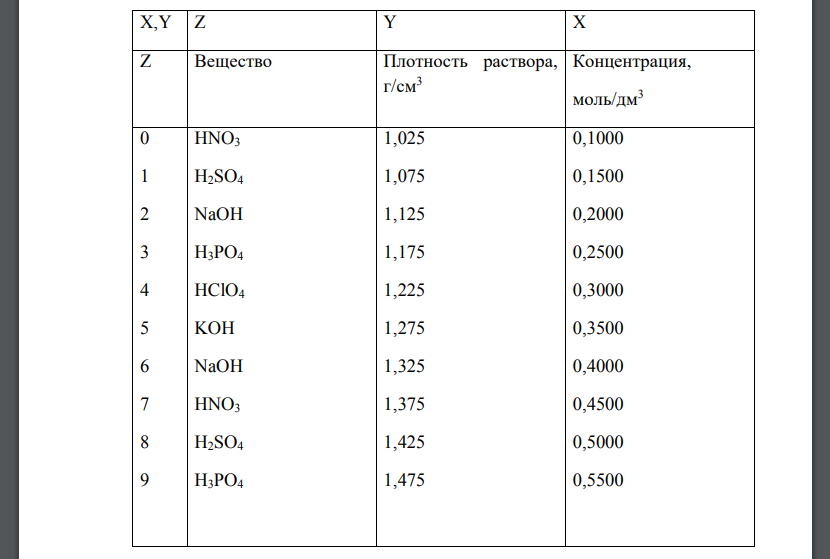
а) Рассчитайте массу навески стандартного вещества (Z), необходимую для приготовления указанного объема раствора(Y) с заданной молярной концентрацией эквивалента Х (табл.13). X,Y Z Y X Z Стандартное вещество Объем раствора, см3 Концентрация, моль/дм3 0 1 2 3 4 5 6 7 8 9 H2C2O4 .2H2O C6H8O6 Na2B4O7 .10H2O Na2CO3 Na2C2O4 K2Cr2O7 KIO AgNO3 NaCl MgSO4 .6H2O 100 150 200 250 500 1000 500 250 200 150 0,0500 0,1000 0,1500 0,2000 0,2500 0,3000 0,3500 0,4000 0,4500 0,5000 б) Вычислите, сколько см3 раствора кислоты или основания (Z) с плотностью (Y) требуется для приготовления 2 дм3 раствора с молярной концентрацией эквивалента X (табл.14). X,Y Z Y X Z Вещество Плотность раствора, г/см3 Концентрация, моль/дм3 0 1 2 3 4 5 6 7 8 9 HNO3 H2SO4 NaOH H3PO4 HClO4 KOH NaOH HNO3 H2SO4 H3PO4 1,025 1,075 1,125 1,175 1,225 1,275 1,325 1,375 1,425 1,475 0,1000 0,1500 0,2000 0,2500 0,3000 0,3500 0,4000 0,4500 0,5000 0,5500
Решение: А) Химическое количество растворенного вещества равно Масса навески равна: Б) Определим массу Плотность имеет раствор серной кислоты концентрацией 29 % (справочные данные). Масса исходного раствора равна Объем исходного раствора серной кислоты равен Ответ:


Похожие готовые решения по химии:
- Вычислите, сколько граммов кислоты (Z) содержится в 500 см3 раствора, если на титрование 25 см3 этого раствора расходуется Х см3 раствора гидроксида натрия с заданной молярной концентрацией эквивалента Y
- Рассчитайте величину потенциала в точке стехиометричности, начале и конце скачка на кривой титрования восстановителя (Z) с молярной концентрацией эквивалента (Y) перманганатом калия той же концентрации при различных pH (X)
- Вычислите процентное содержание элемента (Z) в навеске массой Y, если на её титрование после растворения израсходовано Х см3 раствора комплексона III c молярной концентрацией эквивалента 0,1000 моль/дм3
- Чему равна нормальность раствора, содержащего в 1 л 4,8059 г H2SO4?
- Опишите сущность титриметрических методов анализа. Приведите примеры определения веществ с соответствующими реакциями. Укажите стандартные вещества метода и требования, предъявляемые к ним
- Укажите рабочие растворы метода, способы их приготовления и стандартизации, условия хранения. Приведите примеры расчёта молярной концентрации эквивалента.
- Опишите способы фиксирования точки стехиометричности, применяемые индикаторы. Объясните механизм изменения окраски индикаторов. Укажите, от каких факторов зависит величина скачка на кривой титрования.
- Рассчитайте и постройте кривую титрования раствора слабого основания (YZ 0 - 49) или слабой кислоты (YZ 50 - 99) раствором сильной кислоты (YZ 0 - 49) или сильного основания (YZ 50 - 99). Молярные концентрации эквивалентов реагирующих веществ примите равными 0,1 моль/дм3
- В структуре приведённого вещества:
- Рассчитайте и постройте кривую титрования раствора слабого основания (YZ 0 - 49) или слабой кислоты (YZ 50 - 99) раствором сильной кислоты (YZ 0 - 49) или сильного основания (YZ 50 - 99). Молярные кон
- Используя уравнение Лангмюра, вычислить адсорбцию пропионовой кислоты на поверхности раздела “водный раствор - воздух” при температуре для
- Вычислите, сколько граммов кислоты (Z) содержится в 500 см3 раствора, если на титрование 25 см3 этого раствора расходуется Х см3 раствора гидроксида натрия с заданной молярной концентрацией эквивалент

