
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Рассчитайте рН 0,05 М раствора NaCN
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16800 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
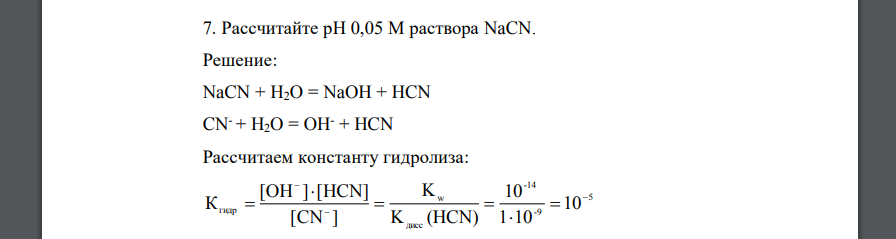
Рассчитайте рН 0,05 М раствора NaCN.
Решение:
Рассчитаем константу гидролиза: По уравнению гидролиза видим, что гидролиз протекает в незначительной степени, поэтому Получаем: Ответ:
Решение:
Рассчитаем константу гидролиза: По уравнению гидролиза видим, что гидролиз протекает в незначительной степени, поэтому Получаем: Ответ:
Похожие готовые решения по химии:
- Подберите коэффициенты в следующих уравнениях реакций: Cr3+ + Br2 + OH- = CrO4 2- + Br- + H2O
- Рассчитайте рН раствора, полученного при смешении 20 мл 0,2 М раствора аммиака и 10 мл 0,1 М хлороводородной кислоты
- При гравиметрическом определении бария в растворе хлорида бария при перенесении осадка на фильтр
- Слили следующие растворы сульфата меди: 100 мл раствора с концентрацией 30,00 (0,25) г/л, 150 мл раствора с концентрацией
- Вычислите и сравните растворимость (моль/л) AgCl в воде
- Рассчитайте концентрацию ОН- иона в 0,5 М растворе HNO3
- Рассчитайте концентрацию иона водорода в раствора с рН 11,2
- Рассчитайте молярную концентрацию раствора бензойной кислоты, имеющего
- Двумерная случайная величина (𝑋, 𝑌) задана таблицей. Найти ковариацию, коэффициент корреляции и сделать вывод
- Сколько моль оксида серы (IV) можно получить при обжиге 1028 г пирита, содержащего 70 масс.% FeS2
- Подберите коэффициенты в следующих уравнениях реакций: Cr3+ + Br2 + OH- = CrO4 2- + Br- + H2O
- При восстановлении водородом 20,34 г оксида металла образовалось 4,50 г воды, масса моль-эквивалента

