
Рассмотреть фазовую диаграмму, приведенную на рисунке. Номера рисунков даны в табл. 6. а) Рассмотрите фазовый состав полей. Дайте характеристику линий
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16718 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
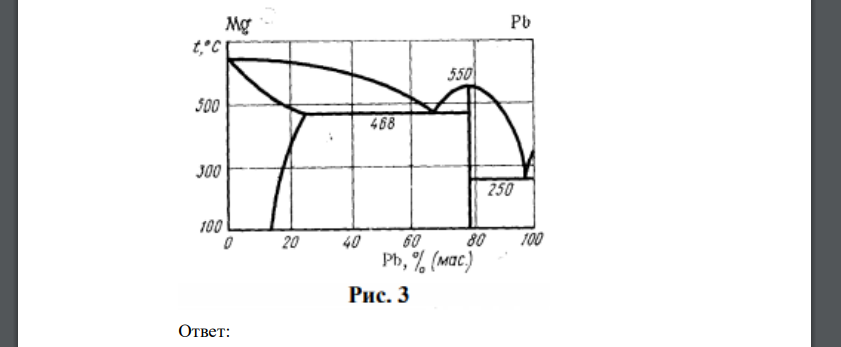
Рассмотреть фазовую диаграмму, приведенную на рисунке. Номера рисунков даны в табл. 6. а) Рассмотрите фазовый состав полей. Дайте характеристику линий и точек на диаграмме. б) Постройте кривую охлаждения расплава состава g. По правилу фаз Гиббса рассчитайте число степеней свободы системы. Что означает это число степеней свободы? Температура начала охлаждения расплава (Т1) дана в табл. 6. в) Для заданной температуры (Т2) рассчитайте массы твердой и жидкой фаз полученных из 400 г первоначального расплава. г) Рассчитайте составы химических соединений. Т1 = 700 К, Т2 = 300 К, g = 80 %
Ответ:
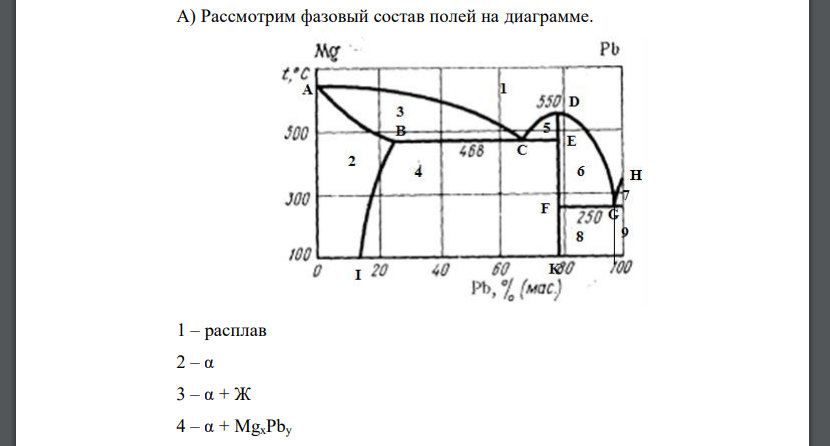
А) Рассмотрим фазовый состав полей на диаграмме. Площадь соответствует твердому раствору. Линия соответствует устойчивому химическому соединению, точки – точки эвтектики. 2. Построим кривую охлаждения: По правилу фаз Гиббса рассчитаем число степеней свободы системы в точке В точке число компонентов , число фаз Это значит, что можно нагреть или охладить сплав в определенном интервале температур без изменения его состояния. В) Рассчитаем массу твердых и жидких фаз по правилу рычага: По условию задачи г) Определим состав химического соединения. Химическое соединения отвечает составу Формула соединения:

Похожие готовые решения по химии:
- Рассчитайте растворимость соли А в воде и ее произведение растворимости по значениям удельного сопротивления насыщенного раствора малорастворимой соли
- По данным, приведенным в табл. 3 (даны номера вариантов), составьте: а) гальванический элемент, состоящий из двух окислительновосстановительных электродов
- Считая порядок данной реакции равным молекулярности, найдите константу скорости данной реакции, протекающей при заданной температуре T, пользуясь данными
- В табл. 5 приведены значения констант скоростей k1 и k2 реакции при двух различных температурах T1 и T2. Вычислите: а) энергию активации данной реакции
- Константа равновесия реакции 2NO + O2 = 2NO2 при 2673 К и давлении 1,013·105 Па равна 0,0035 Па–1 . Какой выход NO получится при этой температуре из смеси
- Зависимость константы равновесия реакции (табл. 3) от температуры выражается уравнением типа lgK = a/T + b·lgT + c·T + d а) определите численное значение
- По зависимости давления насыщенного пара от температуры: а) постройте график зависимости ln p от 1/T; б) рассчитайте среднюю теплоту испарения; в) определите
- При температуре T давление пара растворителя над раствором концентрации g, % (мас.) неизвестного нелетучего вещества в жидком растворителе равно p, Па (плотность
- Образуется ли осадок гидроксида меди (II) при смешивании 0,1 моль/дм3 раствора сульфата тетраамминмеди (II) с равным объемом
- Рассчитать ионную силу раствора, полученного при смешивании равных объемов 0,5 моль/дм3 растворов хлорида свинца
- Вычислить константу равновесия реакции, протекающей между перманганат-ионами и бромид-ионами в кислой среде
- Рассчитать равновесную концентрацию ионов цинка в 0,05 моль/дм3 растворе тетрагидроксоцинката (II) натрия, если водородный

