
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Вещества образуют азеотропную смесь определенного состава. Что будет отгоняться и что будет находиться в кубовом остатке при ректификации
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16850 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
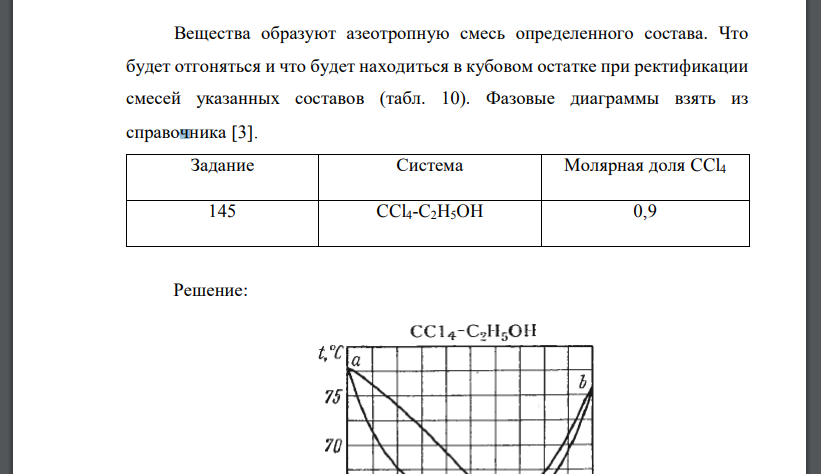
Вещества образуют азеотропную смесь определенного состава. Что будет отгоняться и что будет находиться в кубовом остатке при ректификации смесей указанных составов (табл. 10). Фазовые диаграммы взять из справочника 3. Задание Система Молярная доля CCl4 145 CCl4-C2H5OH 0,9
Решение:
При перегонке смеси, образующей азеотроп с минимальной температурой кипения, сначала отгоняется азеотропная смесь, в кубовом остатке будет находиться .
Похожие готовые решения по химии:
- Вычислить активность ионов металла по величине ЭДС концентрационной цепи при T=298 К, если активность иона в одном из
- Рассчитать КС и КР при T=450 К (P=const) для равновесных процессов, если известен равновесный состав смеси. Все вещества в
- Константа скорости реакции второго порядка A + B = C при одинаковых концентрациях реагирующих веществ равна К. За какое время прореагирует
- Вычислить G o и константу равновесия реакции, протекающей в гальваническом элементе, составленном из электродов A и B при
- Вычислить энергию активации реакции, для которой известны константы скорости реакции K1 и K2 при соответствующих температурах T1 и
- Вычислить pH раствора и концентрацию ионов H+ , если при T=298 К известна эдс элемента (табл. 15). Стандартный электродный потенциал
- По значениям коэффициента преломления и плотности (табл.1) вычислите молярную рефракцию указанного вещества и сопоставьте ее с
- Вычислить константу равновесия некоторой реакции при температуре T2, если известны константа равновесия этой реакции при температуре
- Вычислить константу равновесия некоторой реакции при температуре T2, если известны константа равновесия этой реакции при температуре
- Дан закон распределения двумерной случайной величины (𝜉, 𝜂). 𝜉 = −1 𝜉 = 0 𝜉 = 2 𝜂 = 1 0,1 0,1 0,1 𝜂 = 2 0,1 0,2 0,1 𝜂 = 4 0,1 0,1 0,1 1) Выписать
- Вычислить активность ионов металла по величине ЭДС концентрационной цепи при T=298 К, если активность иона в одном из
- Дан совместный закон распределения системы двух дискретных случайных величин (𝑋; 𝑌): 𝑋 𝑌 0 1 4 0 0,2 0,1 0 2 0 0,1 0,1 5 0,1 0,3 0,1 Найти условное

