
Для концентрационного элемента, составленного из металла А в растворах электролита В с концентрациями m1 и m2 моль/1000 г
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16785 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
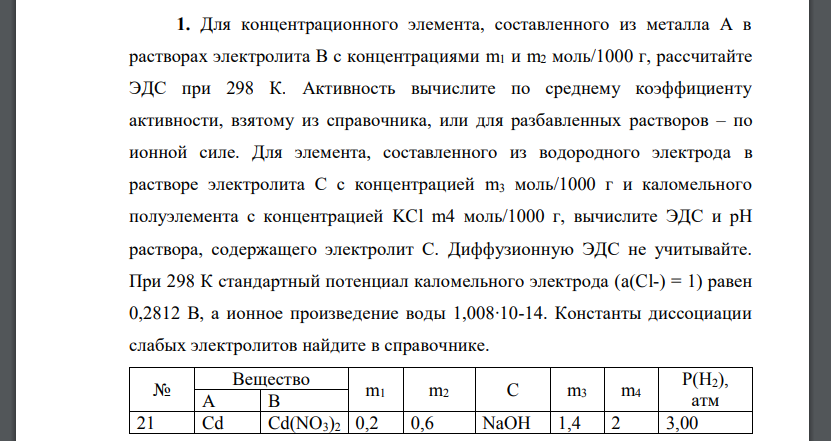
- Для концентрационного элемента, составленного из металла А в растворах электролита В с концентрациями m1 и m2 моль/1000 г, рассчитайте ЭДС при 298 К. Активность вычислите по среднему коэффициенту активности, взятому из справочника, или для разбавленных растворов – по ионной силе. Для элемента, составленного из водородного электрода в растворе электролита С с концентрацией m3 моль/1000 г и каломельного полуэлемента с концентрацией KCl m4 моль/1000 г, вычислите ЭДС и рН раствора, содержащего электролит С. Диффузионную ЭДС не учитывайте. При 298 К стандартный потенциал каломельного электрода (a(Cl-) = 1) равен 0,2812 В, а ионное произведение воды 1,008∙10-14.
Решение:
Рассмотрим концентрационный элемент. Рассчитаем ионную силу раствора. По уравнению Дебая-Хюккеля: Рассчитаем ионную силу раствора. По уравнению Дебая-Хюккеля: Рассчитаем ЭДС Составим схему гальванического элемента из водородного и каломельного электрода. Рассчитаем электродные потенциалы анода и катода. Анодом является водородный электрод. В соответствии с уравнением Нернста его потенциал описывается уравнением Рассчитаем рН раствора. Потенциал водородного электрода равен Определим электродный потенциал катода – каломельного электрода. Рассчитаем активность хлорид ионов в растворе. КCl – сильный электролит. По уравнению Дебая-Хюккеля Электродный потенциал катода равен Ответ:1) 0,006 В; 2) 1,046 В; 12,72.
Похожие готовые решения по химии:
- Для окислительно-восстановительного элемента типа Pt | А, В||С, D | Pt по стандартным электродным потенциалам полуэлементов
- Для реакции, протекающей обратимо в гальваническом элементе, дано уравнение зависимости ЭДС от
- При какой температуре установится равновесие в системе: СН4(г) + 2СО2(г) = 2СО(г) + 2Н2(г), ΔН°298 = +247,37 кДж?
- В химической реакции Na2S2O3 + 2HCl = 2NaCl + S + SO2 + H2O исходная концентрация реагирующих веществ
- Сколько граммов фосфата натрия (Na3PO4) надо прибавить к 1 м3 воды, чтобы устранить ее жесткость
- Вычислить молярную Сm, моляльную m концентрации вещества и его мольную долю Х в водном растворе с концентрацией
- Сколько граммов глюкозы нужно добавить к 100 г воды, чтобы раствор закипел при 102,5 °С
- С использованием таблиц физико-химических величин рассчитать удельную электропроводность и pH раствора слабой кислоты
- Чему равна температура кристаллизации водного раствора этилового спирта С2Н5ОН, если массовая доля спирта составляет 35 %. Дано: w(C2H5OH) = 35 % = 0,35
- Метод кислотно-основного титрования в водной среде. Применение в фармацевтическом анализе
- Составьте схему гальванического элемента из магния и свинца, погруженных в растворы их солей с концентрацией ионов: [Mg2+] = 0,001 моль/л, [Pb2+] = 1 моль/л
- Для случайных величин, принимающих значения 𝑋 = 𝑥𝑖 , 𝑌 = 𝑦𝑖 , (𝑖 = 1̅̅̅,̅𝑛̅): 1) вычислить коэффициент корреляции; 2) получ

