
Изделие, составленное из медных и никелевых фрагментов, эксплуатируется в разбавленном растворе хлороводорода. Как будет 550 происходить процесс контактной коррозии? Составьте электронные уравнения анодного и катодного процессов
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Изделие, составленное из медных и никелевых фрагментов, эксплуатируется в разбавленном растворе хлороводорода. Как будет 550 происходить процесс контактной коррозии? Составьте электронные уравнения анодного и катодного процессов.
Решение
Электрохимическая коррозия металлов происходит в среде электролита (растворы кислот, щелочей, солей, влажный воздух) и может быть представлена как совокупность анодного (окисление) и катодного (восстановление) процессов. При контакте металлов разной электрохимической активности коррозионному разрушению в первую очередь подвергается металл с наиболее отрицательной величиной электродного потенциала E0 . При этом такой металл выполняет функции анода в электрохимической системе и окисляется.
Электронное уравнение анодного процесса можно представить в общем виде:
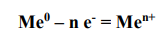
Из двух металлов, представленных в условии задачи, анодом является Ni, т.к. его электродный потенциал (E0 = -0,234 В) является величиной более отрицательной, чем электродный потенциал Cu (Е0 = 0,338 В). Следовательно, в данном случае коррозионному разрушению будет подвергаться металл Ni. Анодный процесс имеет вид:
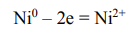
В катодном процессе при электрохимической коррозии участвуют частицы-окислители, находящиеся в электролите:
- в кислой среде:
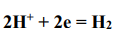
- в нейтральной среде (влажный воздух, атмосферная коррозия):
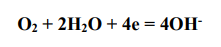
Продукты коррозии определяются результатами анодного и катодного процессов: - в кислой среде выделяется газообразный водород и образуется соль металла-анода и кислоты, создающей среду; - в нейтральной среде продуктом коррозии является гидроксид металлаанода (как результат взаимодействия катионов металла-анода и гидроксидионов, образующихся на катоде). В рассматриваемой в задаче системе продуктами коррозии являются: NiCl2 и H2.

Похожие готовые решения по химии:
- Как будет происходить электролиз водного раствора электролита NaNO3 (t = 45 мин, I = 7 А)? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях
- Таким образом, число протонов в ядре численно совпадает с атомным (порядковым) номером элемента в периодической системе Д.И. Менделеева. Число нейтронов можно вычислить по разности между массовым числом и числом протонов
- На основании положения химического элемента № 35 и его электронной формулы составьте прогноз его химических свойств, ответив на следующие вопросы
- Определите тип химической связи (неполярная ковалентная, полярная ковалентная или ионная) в веществах бромид кальция и дибром
- Укажите, как необходимо изменить внешние параметры (температуру, общее давление, концентрации реагентов), чтобы сместить равновесие вправо
- Нужно провести вычисления и найти недостающие величины водных веществ и заполнить таблицу
- Для ответов на вопросы задачи вычислим степени окисления атомов, входящих в состав приведенных в уравнении реакции веществ, руководствуясь следующими правилами
- Более отрицательной величиной электродного потенциала характеризуется металл Mn, поэтому именно он и будет участником анодного процесса
- Начислите заработную плату за июнь председателю правления, главному бухгалтеру, экономисту, кассиру потребительского общества
- Более отрицательной величиной электродного потенциала характеризуется металл Mn, поэтому именно он и будет участником анодного процесса
- Для производства продукции в плановом периоде при сохранении достигнутого уровня выработки требуется 600 рабочих. Общая экономия
- Дайте оценку производительности труда и определите влияние изменения цен на изменение производительности труда. Оцените соотношение

