
Раствор электролита с концентрацией 0,04 моль/л имеет осмотическое давление при 0 С, равное 217,8 кПа. Степень диссоциации растворенного вещества равна 70 %. Определить, на сколько ионов диссоциирует растворенное вещество и привести примеры таких веществ
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Раствор электролита с концентрацией 0,04 моль/л имеет осмотическое давление при 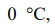 равное 217,8 кПа. Степень диссоциации растворенного вещества равна 70 %. Определить, на сколько ионов диссоциирует растворенное вещество и привести примеры таких веществ.
равное 217,8 кПа. Степень диссоциации растворенного вещества равна 70 %. Определить, на сколько ионов диссоциирует растворенное вещество и привести примеры таких веществ.
Решение:
Осмотическое давление электролита рассчитывается по формуле 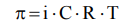 Выразим и рассчитаем изотонический коэффициент, учитывая, что С =
Выразим и рассчитаем изотонический коэффициент, учитывая, что С =
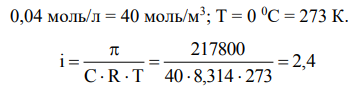
Изотонический коэффициент связан со степень диссоциации и количеством ионов, на которой диссоциирует электролит, соотношением
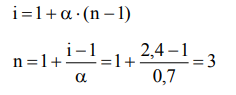
Получаем, что электролит в водном растворе диссоциирует на 3 иона. Примеры таких электролитов: 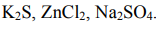

Похожие готовые решения по химии:
- Написать уравнения гидролиза и выражения для констант гидролиза солей: KClO, K2S, AlCl3
- Какие из пар солей взаимно усиливают гидролиз: a) NiCl2 и CH3COONa; б) NaAlO2 и CrCl3; в) Na2SiO3 и KNO2? Объяснить причину взаимного усиления гидролиза, написать уравнения реакций
- Какими законами и какими формулами выражаются количественные показатели электролиза? Привести пример электролиза и его количественного расчета
- Как происходит атмосферная коррозия луженого и оцинкованного железа при нарушении покрытия? Составьте электронные уравнения анодного и катодного процессов. Запишите схемы гальванических элементов, возникающих в каждом случае
- Разложение нитрата аммония при нагревании возможно по двум направлениям
- Чем отличается истинное химическое равновесие от ложного? Привести примеры истинных и ложных равновесий
- Какая эта реакция – простая или сложная? Как изменяется ее скорость при увеличении концентрации в 4 раза: а) только водорода; б) только брома; в) водорода и брома одновременно
- Молярная концентрация NH3 в концентрированном растворе аммиака, полученном при 15 С, равна 18. Какой объем NH3, измеренный при н.у., затрачивается на приготовление 1 л такого раствора
- Определить брутто-ставку при нагрузке 0,25 (недостающие данные взять из задачи № 3)
- Определить нетто-ставку при доверительной вероятности 0,95 с помощью таблицы распределения
- Написать уравнения гидролиза и выражения для констант гидролиза солей: KClO, K2S, AlCl3
- Определить страховую премию при страховой сумме 100 тыс. руб. (недостающие данные взять из задачи № 4)

