
Какими законами и какими формулами выражаются количественные показатели электролиза? Привести пример электролиза и его количественного расчета
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Какими законами и какими формулами выражаются количественные показатели электролиза? Привести пример электролиза и его количественного расчета.
Ответ:
Для реакций электролиза существуют специфичные количественные соотношения, названные законами Фарадея.
1. Масса электролита, подвергшаяся превращению при электролизе, а также массы образующихся на электродах веществ прямо пропорциональны количеству электричества, прошедшего через раствор или расплав электролита:
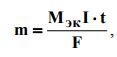
где m - масса выделившегося или подвергшегося превращению вещества, МЭК - эквивалентая масса вещества (г/моль экв), I - сила тока (а), t - время (с), F - постоянная Фарадея (96500 Кл /моль экв), т. е. количество электричества, необходимое для выделения или превращения одного моля эквивалента вещества. 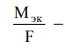 электрохимический эквивалент.
электрохимический эквивалент.
2. При прохождении одного и того же количества электричества через раствор или расплав электролита массы (объемы) веществ, выделившихся на электродах, прямо пропорциональны их химическим эквивалентам.
Пример. Ток силой 6 А проходил в течение 1,5 часа через разбавленный раствор 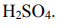 Вычислить массу разложившейся воды и объемы
Вычислить массу разложившейся воды и объемы 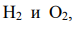 выделившихся на электродах
выделившихся на электродах 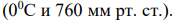
Решение.
В растворе кислота диссоциирует по уравнению: 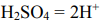
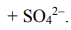
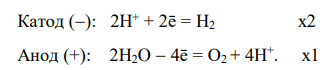
Токообразующая реакция: 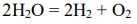
Процессы электролиза подчиняются закону Фарадея: 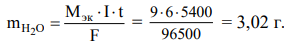
При вычислении объемов выделившихся газов представим уравнение в следующей форме: 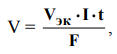 где V -объем выделившегося газа,
где V -объем выделившегося газа, 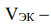 его эквивалентный объем. Поскольку при н.у.
его эквивалентный объем. Поскольку при н.у.  водорода равен 11,2 л/моль, а кислорода 5,6 л/моль (см. раздел 1), то получаем:
водорода равен 11,2 л/моль, а кислорода 5,6 л/моль (см. раздел 1), то получаем:
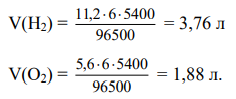

Похожие готовые решения по химии:
- Как происходит атмосферная коррозия луженого и оцинкованного железа при нарушении покрытия? Составьте электронные уравнения анодного и катодного процессов. Запишите схемы гальванических элементов, возникающих в каждом случае
- Железные изделия покрыли кадмием. Какое это покрытие – анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе и в соляной кислоте
- Опишите физические свойства (агрегатное состояние, оптическую активность, запах, цвет, вкус) заданных соединений
- Напишите формулу строения заданной α-аминокислоты, исходя из строения радикала. К какому типу аминокислот она относится? С помощью, каких цветных реакций можно открыть эту аминокислоту
- Молярная концентрация NH3 в концентрированном растворе аммиака, полученном при 15 С, равна 18. Какой объем NH3, измеренный при н.у., затрачивается на приготовление 1 л такого раствора
- Раствор электролита с концентрацией 0,04 моль/л имеет осмотическое давление при 0 С, равное 217,8 кПа. Степень диссоциации растворенного вещества равна 70 %. Определить, на сколько ионов диссоциирует растворенное вещество и привести примеры таких веществ
- Написать уравнения гидролиза и выражения для констант гидролиза солей: KClO, K2S, AlCl3
- Какие из пар солей взаимно усиливают гидролиз: a) NiCl2 и CH3COONa; б) NaAlO2 и CrCl3; в) Na2SiO3 и KNO2? Объяснить причину взаимного усиления гидролиза, написать уравнения реакций
- Известно, что заявки на телефонные переговоры, в пункт услуг по предоставлению связи поступают с интенсивностью
- Рассматривается круглосуточная работа пункта проведения профилактического осмотра автомашин с одним каналом (одной группой проведения
- Железные изделия покрыли кадмием. Какое это покрытие – анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе и в соляной кислоте
- Как происходит атмосферная коррозия луженого и оцинкованного железа при нарушении покрытия? Составьте электронные уравнения анодного и катодного процессов. Запишите схемы гальванических элементов, возникающих в каждом случае

