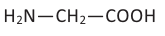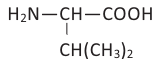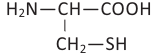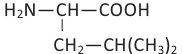Азотсодержащие органические соединения в химии - формулы и определения с примерами
Содержание:
Азотсодержащие органические соединения:
Азотсодержащими органическими соединениями называются органические вещества, содержащие в своем составе атомы азота.
Нитросоединения. Способы их получения и свойства
Органические вещества, получаемые путем замещения одного или нескольких атомов водорода в составе насыщенных или ароматических углеводородов на нитрогруппу 
Номенклатура: По рациональной номенклатуре при названии нитросоединений к названию соответствующего углеводорода прибавляют приставку «нитро».
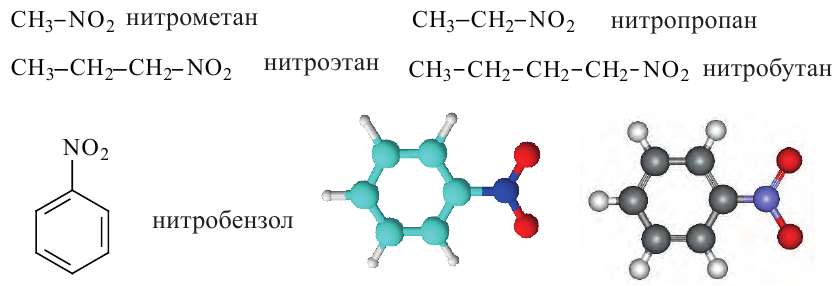
Систематическая номенклатура.
На основе международной номенклатуры нитросоединения называются в следующем порядке:
- Нитрогруппа должна быть связана с основной углеродной цепью.
- Нумерация атомов углерода в основной цепи начинается с того конца, с Сначала называются радикалы или нитрогруппа (в зависимости от алфавитного порядка) с указанием атома углерода в котором он находится, и только после этого называется основная цепь.
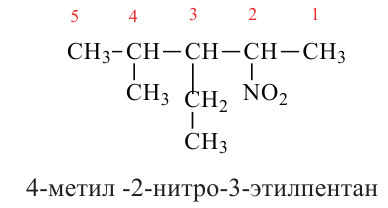
Способы получения: Введение нитрогруппы в состав органических соединений называется нитрованием. Этот процесс можно осуществить следующими способами.
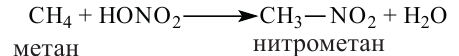
1. Нитрование насыщенных углеводородов. Для этого к насыщенным углеводородам воздействуют азотной кислотой.
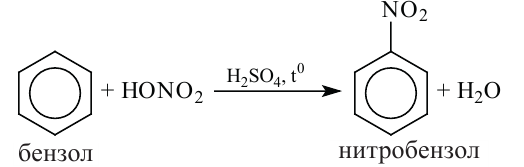
2. Воздействие концентрированной азотной кислотой (при помощи концентрированной серной кислоты) на бензол. В результате данной реакции образуется нитробензол.
Физические свойства: Низкомолекулярные гомологи нитросоеди-нений являются бесцветными жидкостями с неприятным запахом, которые хорошо растворяются в эфире и легко смешиваются со спиртами. Пары нитросоединений токсичны.
Химические свойства: Химические свойства нитросоединений разнообразны и в основном зависят от нитрогруппы в составе их молекулы.
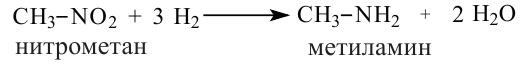
1. Нитросоединения при восстановлении превращаются в первичные амины.
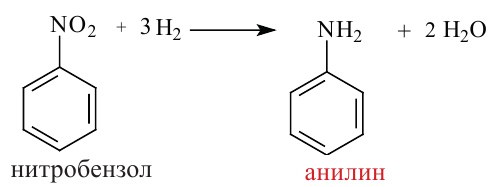
2. При восстановлении ароматических нитросоединений они превращаются в соответствующие ароматические амины.
Амины. Способы получения и свойства
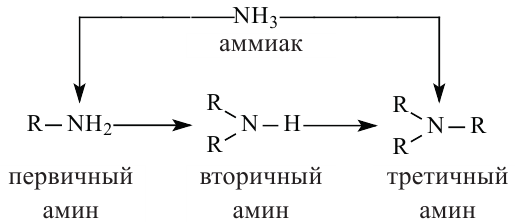
Амины - это продукты, полученные замещением атомов водорода в составе аммиака на углеводородный радикал.
По своему строению амины рассматриваются как производные аммиака.
При замещении одного атома водорода на углеводородный радикал получается первичный амин, двух атомов водорода - вторичный амин и, соответственно, при замещении трех атомов получается - третичный амин.
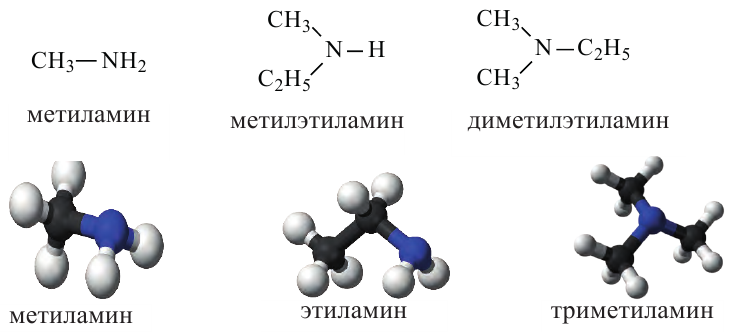
Номенклатура и изомерия: При использовании рациональной номенклатуры, название амина получается путем добавления слова «амин» к названию радикала.
По систематической номенклатуре название аминов образуется путем прибавления слова «амино» к названию соответствующего углеводорода. При этом нумерация начинается с той стороны цепи, к которой ближе аминогруппа.
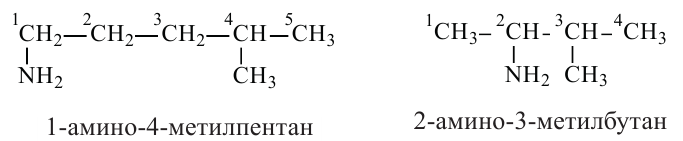
Если в составе амина имеется несколько одинаковых радикалов, то к названию радикала прибавляется приставки ди- или три-. Например: 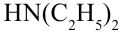 - диэтиламин,
- диэтиламин, 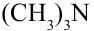 - триметиламин.
- триметиламин.
Изомерия: У аминов наблюдается структурная изомерия по строению углеводородной цепи и по расположению аминогруппы. Например, вещество с составом 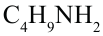 имеет 4 изомера.
имеет 4 изомера.
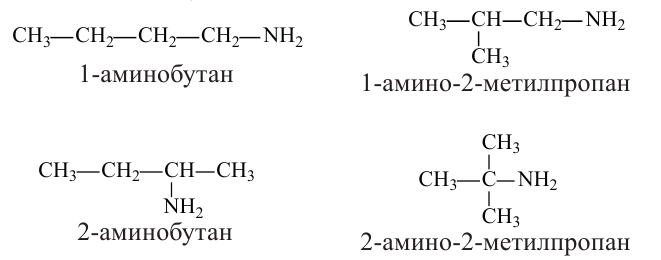
Способы получения:
Амины являются продуктами восстановления нитросоединений с помощью атомов водорода.
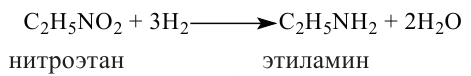
Физические свойства:
Первые представители аминов - метиламин, диметиламин и триметиламин являются газами, остальные имеют жидкое агрегатное состояние и только высокомолекулярные амины являются твердыми веществами.
Химические свойства:
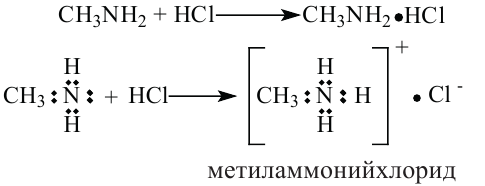
1. Образование солей: При воздействии на амины кислотами образуются соли. Эта реакция протекает за счет присоединения иона водорода к свободной паре электронов атома азота с образованием положительно заряженного иона аммония.
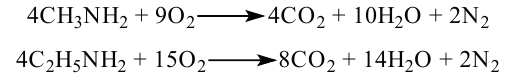
2. Горение аминов. Амины горят в воздухе. В результате реакции, кроме 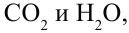 образуется еще и молекула
образуется еще и молекула 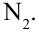
Ароматические амины
Органические вещества, образованные замещением атома водорода в составе бензольного кольца на аминогруппу или замещением атома водорода в составе молекулы аммиака на фенильный 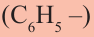 радикал, называются ароматическими аминами.
радикал, называются ароматическими аминами.
В зависимости от числа замещенных атомов водорода в молекуле аммиака на фенильную группу образуются первичные, вторичные или третичные амины.
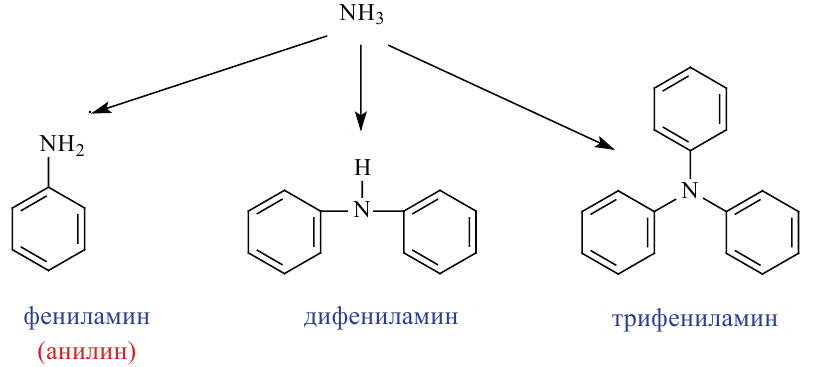
Номенклатура. Название ароматических аминов образуется путем добавления слова «амин» к названию радикала.
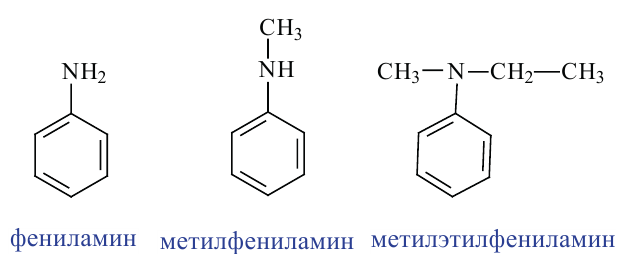
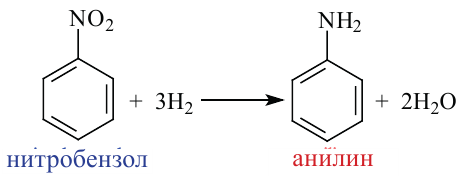
Способы получения. Впервые способ получения ароматических аминов путем восстановления нитросоединений было осуществлено русским ученым Н.Н.Зининым:
Физические свойства: Низшие представители ароматических аминов являются жидкостями, а высшие - имеют твердое агрегатное состояние. Большинство их обладают резко выраженным запахом и плохо растворяются в воде.
Химические свойства: Химические свойства ароматических аминов обусловлены наличием аминогруппы и бензольного кольца в своем составе.
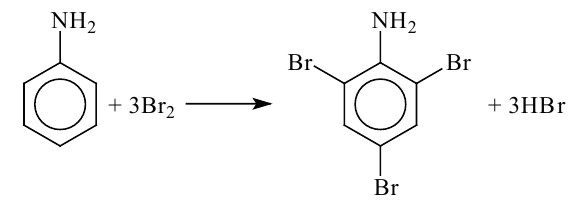
1. При воздействии на анилин бромной водой образуется осадок триброманилин. (бензол не реагирует с бромной водой)
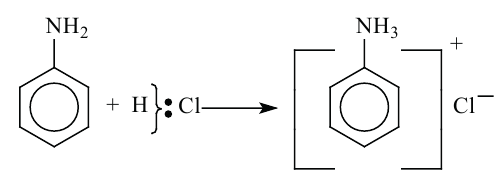
2. При воздействии на анилин соляной кислотой образуется соль хлорид фениламмония.
Применение: Анилин в основном применяется в лакокрасочной отрасли. При воздействии на анилин окислителями можно получить разноцветные вещества, к примеру, черный анилин. Кроме того, анилин считается основой для получения большинства лекарственных веществ.
Аминокислоты и белки. Получение и свойства
Органические вещества, содержащие в своем составе амино  и карбоксильную
и карбоксильную 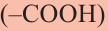 группы называются аминокислотами. Также аминокислот можно рассматривать как производных органических кислот, где атом водорода в составе углеводородного радикала заменен на аминогруппу.
группы называются аминокислотами. Также аминокислот можно рассматривать как производных органических кислот, где атом водорода в составе углеводородного радикала заменен на аминогруппу.
Аминокислоты имеют следующую общую формулу.
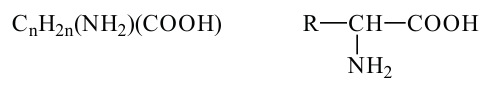
Аминокислоты по числу амино 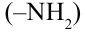 и карбоксильных
и карбоксильных 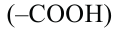 групп делятся на три группы.
групп делятся на три группы.
1. Аминокислоты, содержащие одну амино- 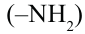 и одну карбоксильную группы
и одну карбоксильную группы 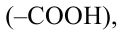 называются моноамино- монокарбоновыми кислотами.
называются моноамино- монокарбоновыми кислотами.
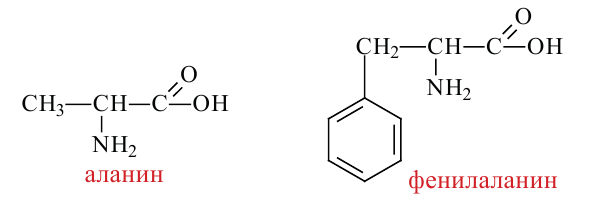
2) Аминокислоты, содержащие две амино- и одну карбоксильную
и одну карбоксильную 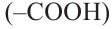 группы, называются диамино- монокарбоновыми кислотами.
группы, называются диамино- монокарбоновыми кислотами.
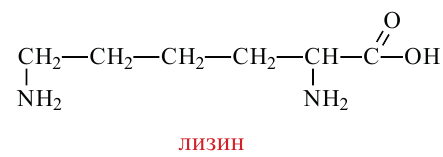
3) Аминокислоты, содержащие одну амино- 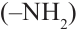 и две карбоксильные
и две карбоксильные 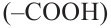 группы, называются моноамино- дикарбоновыми кислотами.
группы, называются моноамино- дикарбоновыми кислотами.
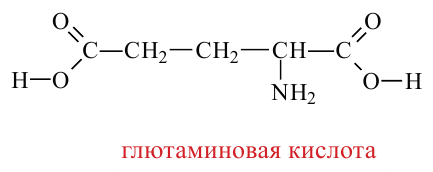
Наряду с этим, встречаются аминокислоты, содержащие в своем составе и другие функциональные группы.
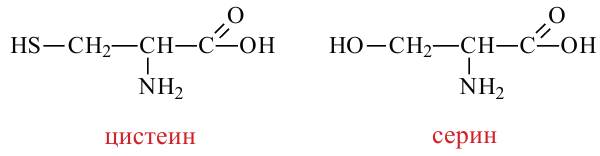
Номенклатура: По рациональной номенклатуре аминокислоты называются следующим образом. Для начала углеродная цепь нумеруется греческими буквами алфавита и определятся место расположения аминогруппы по отношению к карбоксильной группе.
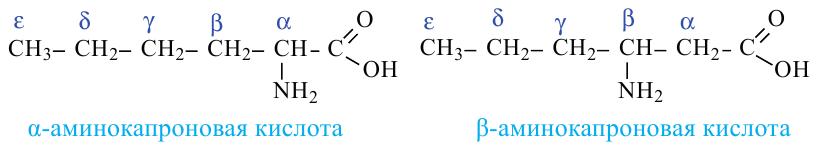
По систематической номенклатуре определяется углеродная цепь, содержащая и амино, и карбоксильную группу, после этого цепь нумеруется, начиная с атома углерода карбоксильной группы.
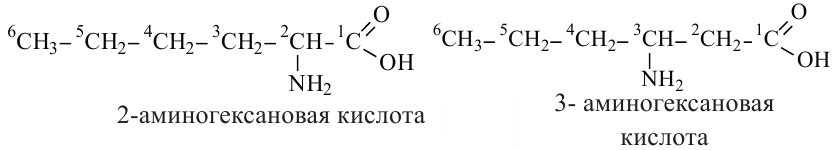
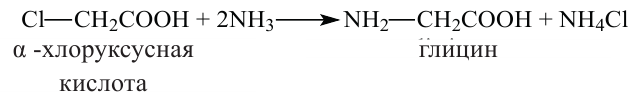
Способы получения: Аминокислоты получают путем гидролиза белков. Кроме того, их еще можно получить воздействием аммиака на хлорорганические кислоты.
Физические и химические свойства, 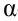 -аминокислоты - это бесцветные кристаллические вещества. Большинство из них хорошо растворяются в воде, зачастую имеют сладкий вкус, но среди них встречаются и аминокислоты с неприятным и горьким вкусом.
-аминокислоты - это бесцветные кристаллические вещества. Большинство из них хорошо растворяются в воде, зачастую имеют сладкий вкус, но среди них встречаются и аминокислоты с неприятным и горьким вкусом.
Изменения цвета индикатора: Моноамино-монокарбоновые и диамино-дикарбоновые аминокислоты не меняют цвета индикатора. Диамино-монокарбоновые аминокислоты имеют щелочные свойства, а моноамино-дикарбоновые аминокислоты имеют кислотные свойства и цвет индикаторов они меняют соответствующим образом.
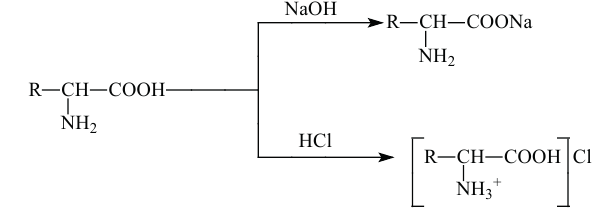
Образование солей: Как вещества, имеющие в своем составе одновременно и амипо-, и карбоксильную группы, аминокислоты обладают амфотерным свойством и могут образовывать соли, реагируя как кислотами, так и щелочами.
Применение: Аминокислоты являются самыми важными компонентами при образовании белка в организме. Они входят в состав употребляемой пищи. Порой аминокислоты употребляются в чистом виде. К примеру, после тяжелых операций, из-за которых пища не может преодолеть желудочно-кишечный тракт или истощенным больным, аминокислоты используют для питания. Аминокислоты используют при лечении некоторых болезней (глютаминовая кислота при лечении болезней нервной системы, гистидин при лечении язвы желудка).
В сельском хозяйстве некоторые аминокислоты добавляют в корм для нормализации роста животных.
Пептиды и белки
Пептиды - это вещества, составляющие основу белка и образующиеся в результате поликонденсации двух или нескольких аминокислот. Если пептид состоит из остатков двух аминокислот, то он называется дипептидом, из трех-трипептидом и т.д.
Любая молекула пептида имеет строение длинной цепи с двумя концами, один конец заканчивается атомом азота в аминогруппе - 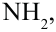 а второй атомом углерода в карбоксильной группе -
а второй атомом углерода в карбоксильной группе - 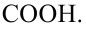
Белки - это сложные высокомолекулярные органические соединения, состоящие из 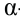 -аминокислот. Принято называть соединения, содержащие до 50 аминокислот пептидами (до 10 олигопептидами, больше 10 полипептидами), а соединения, содержащие больше 50 аминокислот, условно называются белками.
-аминокислот. Принято называть соединения, содержащие до 50 аминокислот пептидами (до 10 олигопептидами, больше 10 полипептидами), а соединения, содержащие больше 50 аминокислот, условно называются белками.
Природные источники. Белки составляют основу протоплазмы растений. Они содержатся и выполняют ключевую жизненную роль в крови, молоке, мышцах и хряще животных. Белки также входят в состав волос, ногтей, кожи, пуха, шерсти, шелка. Кроме того, белок составляет основную часть яиц.
В органах растений и животных белки выполняют разные функции. Большинство гормонов, ферментов, антибиотиков и токсинов имеют белковую природу. Часто белки образуют клеточную оболочку животных и играют важную роль в росте и обмене веществ.
Классификация: Белки по химическому составу делятся на простые и сложные.
Белки, при полном гидролизе которых образуются только аминокислоты, называются простыми. Они составляют большую часть среди белков.
Сложные белки при гидролизе образуют, кроме аминокислот, еще и соединения (углеводы, остаток фосфорной кислоты, нуклеиновые кислоты и т.д.) не белковой природы.
Общие свойства белков: Биологическая активность белков зависит от пространственного и химического строения их молекулы. Белки обладают разными физическими свойствами: некоторые образуют коллоидные растворы в воде (яичный белок), другие растворяются в растворах солей, третьие совсем не растворяются (белки тканей кожи).
Денатурация белков - это разрушение конфигурации белков (вторичного и третичного строения) под воздействием нагрева, радиации, сильных кислот, щелочей, солей тяжелых металлов или сильного сотрясения. В результате денатурации белков (разрушение водородных, солевых, эфирных, полисульфидных связей) теряется биологическая активность белков.
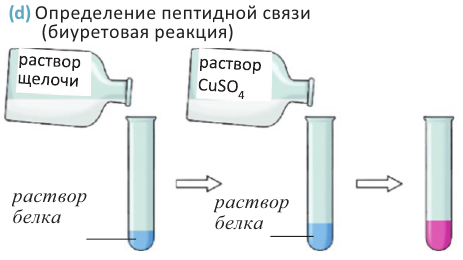
Качественные реакции белков: Одной из качественных реакций на белки является биуретовая реакция: в щелочной среде раствор сульфата меди (II) окрашивается в фиолетовый цвет. Биуретовая реакции характерна для пептидных 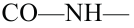 связей. К примеру, дипептиды дают -синий, трипептиды - фиолетовый, высокомолекулярные пептиды -красный цвет.
связей. К примеру, дипептиды дают -синий, трипептиды - фиолетовый, высокомолекулярные пептиды -красный цвет.
Биологическое значение белков. Белки являются основной составной частью живого организма, входят в состав протоплазмы и ядра клеток животных. Жизнь есть способ существования белковых тел! Животный организм строит свои белки на основе аминокислот в белках, полученных с пищей.
Недостаток или отсутствие белков в пище приводит к тяжелым болезням. Пищевая ценность белков определяется их аминокислотным составом, а точнее количеством незаменимых аминокислот, входящих в состав белка. Животные получают белки в составе употребляемой растительной или животной пищи. Белки подвергаются гидролизу под воздействием ферментов в желудке и кишечнике. Полученные аминокислоты всасываются через стенки кишечника в кровь и дальше транспортируются к тканям и клеткам. Там из аминокислот синтезируются нужные белки. Из белков строятся клетки и ткани организма.
Изучение белков дает возможность понять и разумно контролировать жизненные процессы организма.
Производство белковых препаратов: гормонов, сывороток и кровезаменителей имеет важное значение для медицины.
Пример №1
Если в результате реакции неизвестной аминокислоты массой 37,5 г с гидроксидом натрия выделяется 9 г воды, определите название аминокислоты в данной реакции.
Решение:
Для начала напишем уравнение реакции в условии задачи.

На основе реакции с помощью пропорции определим молекулярную массу неизвестной аминокислоты.
Теперь определим, какая из аминокислот имеет массу 75 г/моль. Данную молекулярную массу имеет глицин 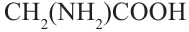
Ответ: 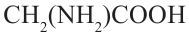
Высокомолекулярные соединения
Высокомолекулярные соединения (ВМС) по своим свойствам сильно отличаются от низкомолекулярных соединений. Это связано полидисперсностью и большими размерами молекул данных веществ.
По происхождению высокомолекулярные вещества разделяются на три вида: природные, синтетические и искусственные.
Природные ВМС широко распространены в животном и растительном мире. К ним можно отнести целлюлозу, крахмал, белки, нуклеиновые кислоты, натуральные каучуки и другие. Искусственные ВМС получают химической переработкой натуральных ВМС.
К синтетическим ВМС можно отнести синтетические пластмассы, каучуки и синтетические волокна. Синтетические ВМС получают из мономеров, которые не встречаются в природе путем реакций полимеризации и поликонденсации.
ВМС в большинстве случаев называются полимерами (из греческого «поли» -много, «мерос» - часть). Молекулы, которые, связываясь между собой ковалентными связями, образуют полимер, называются мономерами.
Например, в нижеприведенной реакции:
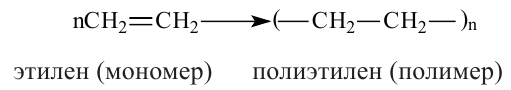
этилен (мономер) полиэтилен (полимер) Слово полимер можно также заменить словом макромолекула, они равноценны по смыслу. Группа атомов, образующие состав макромолекулы, называется звеном. Значение 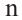 является показателем степени полимеризации, и указывает, из какого количества молекул мономера образована молекула полимера.
является показателем степени полимеризации, и указывает, из какого количества молекул мономера образована молекула полимера.
Молекулярная масса полимера 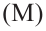 находится путем умножения масс звеньев
находится путем умножения масс звеньев 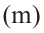 на степень полимеризации.
на степень полимеризации. 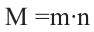
Физические и механические свойства ВМС зависят, в основном, от их природы и молекулярной массы. С повышением молекулярной массы теряются такие свойства как диффузия, летучесть, взамен вещество приобретает свойства как набухание, высокая липучесть, разложение при нагревании вместо перехода в жидкое состояние и т.д.
Общая классификация важнейших пластмасс
Название Мономер Формула полимера и способ получения Использование
Полиэтилен
- Мономер:
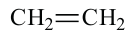 этилен
этилен - Формула
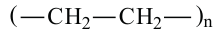 Полимеризация
Полимеризация - Для изготовления различных частей приборов, водопроводных труб, различных пленок, и бытовых изделий
Полипропилен
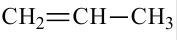 пропилен
пропилен 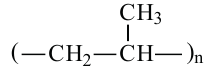 Полимеризация
Полимеризация - Намного прочнее, чем полиэтилен. Из него изготавливают детали различных устройств, тонких пленок, веревку, трубы, изоляционные материалы.
Поливинил хлорид
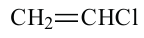 винилхлорид
винилхлорид -
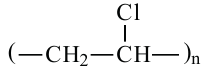 Полимеризация
Полимеризация - Получают искуственную кожу, плащи, клеенки, трубы, изоляционное покрытие для электропроводов.
Фенол формальдегидная смола
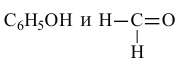 фенол и формальдегид
фенол и формальдегид 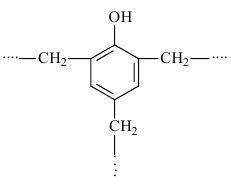 Поликонденсация
Поликонденсация - В основном фенопласты. Из них заготавливают шариковые подшипники для автомобилей, ступени эскалаторов, телефонные аппараты.

Некоторые представители полимеров
Полипропилен 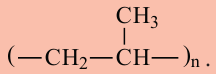 Получается путем полимеризации пропилена. Полипропилен является бесцветным и твердым материалом. Его механическая прочность выше, чем у полиэтилена.
Получается путем полимеризации пропилена. Полипропилен является бесцветным и твердым материалом. Его механическая прочность выше, чем у полиэтилена.
Полипропилен в основном применяется в электротехнике и радиотехнике. В последние годы разработали метод получения прочных волокон из полипропилена, которые по своим свойствам не отстают от самых прочных натуральных волокон. Поливинилхлорид считается продуктом полимеризации винилхлорида.
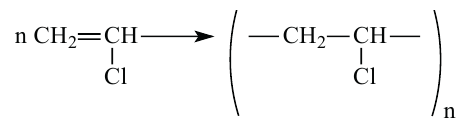
Это твердый полимер, не способный кристаллизоваться. При прямом контакте с пламенем он не плавится и не горит, а разлагается. В обычных условиях поливинилхлорид трудно растворяется в органических растворителях. Он устойчив к воздействию агрессивных веществ. Поэтому его применяют для производства труб, покрытия внутреннего слоя реакторов. Также используется для получения лаков, химических волокон. Почти все виды линолеума изготовлены из поливинилхлорида.
Каучук, мономером которого является изопрен (2-метилбутадиен-1,3), входит в класс природных полимеров.
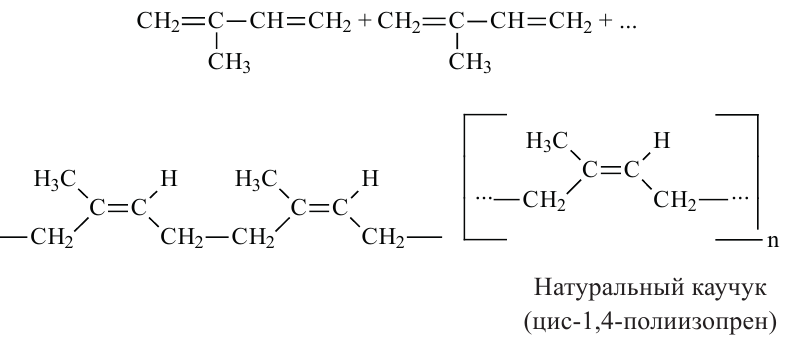
Натуральный каучук (цис-1,4-полиизопрен) Мономером синтетического каучука является бутадиен - 1,3. Каучук и продукт его вулканизации - резина - применяется почти во всех отраслях народного хозяйства. Но количество каучука, получаемого из растений, недостаточно для полного удовлетворения нужд на данный материал. Поэтому возникла потребность на промышленное производство каучука:
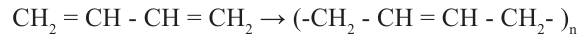
В настоящее время бутадиен-1,3 получают не из этилового спирта, а каталитическим дегидрированием бутана. Бутадиеновый каучук по эластичности и стойкости к разъеданию уступает натуральному каучуку.
Важнейшие синтетические каучуки, их свойства и применение
Название Мономер Важное свойство и применение
Бутадиеновый каучук
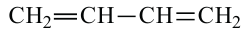 бутадиен-1,3
бутадиен-1,3 - Газо- и водонепроницаемость. По эластичности уступает натуральному каучуку. Из него изготавливают автомобильные шины, кабели, обувь, хозяйственные товары.
Изопреновый каучук
-
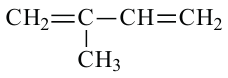 2-метил-бутадиен-1,3 (изопрен)
2-метил-бутадиен-1,3 (изопрен) - По эластичности и прочности схож с натуральным каучуком. Из него производят автомобильные шины.
Хлорпреновый каучук
-
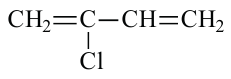 2-хлорбутадиен-1,3 (хлорпрен)
2-хлорбутадиен-1,3 (хлорпрен) - Устойчив к высоким температурам, горению бензина и масла. Не пропускает газы. Из него изготавливаются кабели, бензо- и нефтепроводы.
Пример №2
Определите степень полимеризации полиизобутилена с молекулярной массой 56280 г/моль. Решение задачи:
Полиизобутилен получается путем полимеризации изобутилена. Запишем данную реакцию.
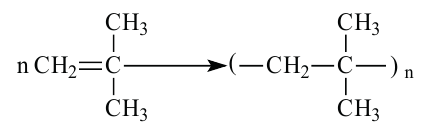
Для определения степени полимеризации высокомолекулярного соединения нужно найти число мономеров, которые участвовали в образовании макромолекулы полимера.
Молекулярная масса изобутилена 56 г/моль Молекулярная масса полимера 56280 г/моль
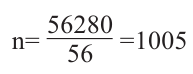
Значит, в процессе полимеризации участвовало 1005 молекул изобутилена.
Ответ: 1005
Пример №3
Если степень полимеризации полиизобутилена равна 550, определите его молекулярную массу.
Решение задачи:
Для решения данной задачи воспользуемся формулой вычисления молекулярной массы полимера: 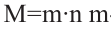 -молекулярная масса мономера, для изобутилена 56 г/моль,
-молекулярная масса мономера, для изобутилена 56 г/моль, 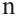 - степень полимеризации, в нашем случае она равна 550.
- степень полимеризации, в нашем случае она равна 550.

Молекулярная масса полиизобутилена: 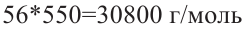
Значит, молекулярная масса полимера равна к 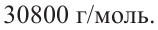
Ответ: 30800 г/моль
Азотсодержащие органические соединения
Нитросоединения
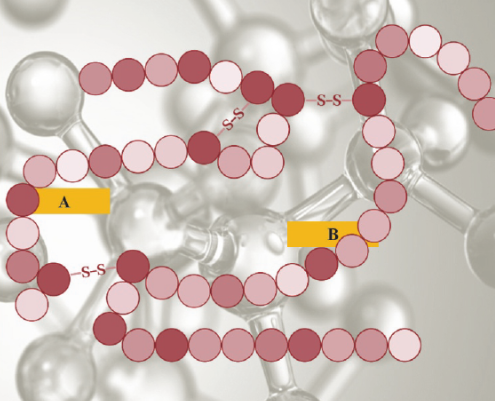
Среди азотсодержащих органических соединений особое место принадлежит белкам и образующим их аминокислотам.
Белки - основа структуры и функций живых организмов. Само название протеины (от греч. protos - "первый", "важнейший") и отражает первостепенное биологическое значение этого класса веществ. Несмотря на то, что они образуются всего из 20 аминокислот, их очень много. Подсчитано, что в природе встречается примерно 1010-1012 различных белков, обеспечивающих существование около 106 видов живых организмов. Из них в организме человека насчитывается более 50 000 разнообразных белков. До настоящего времени установлено строение около 2500 белков.
Белки образуются в клетках живых организмов из аминокислот в ходе биосинтеза. Белки можно синтезировать и в химических лабораториях. Для этого необходимо установить их первичную структуру и далее, соединить аминокислотные остатки в полипептидную цепь в соответствии с первичной структурой. Однако эта задача очень сложная. Например, для синтеза одной полипептидной цепи (А) простейшего белка - инсулина пришлось осуществить 89 химических реакций, а другой полипептидной цепи (В) - 138 реакций, на что потребовалось около 10 лет.
- -NH2 функциональная группа называется аминогруппой
К азотсодержащим органическим соединениям относятся нитросоединения, амины, аминокислоты, белки и др.
- Нитросоединения - это органические соединения, в молекулах которых одна или несколько нитрогрупп (-NO2) связаны с углеводородным радикалом.
- Амины - это производные аммиака, в молекуле которого атомы водорода замещены углеводородными радикалами.
В зависимости от числа радикалов, связанных с атомом азота, различают первичные, вторичные и третичные амины:
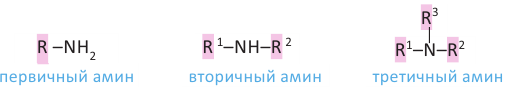
Функциональная группа -NH2 называется аминогруппой. Амины, содержащие в молекуле одну аминогруппу, называют моноаминами, две аминогруппы - диаминами; например, CH3-NH2 и С6Н5-NН2 моноамины, H2N-CH2-CH2-NH2 (этилендиамин) и H2N-(CH2)6-NH2 (гексаметилендиамин) - диамины.
Обычно ди-, три- и др. амины, а также ароматические амины, например, фениламин (C6H5NH2), рассматриваются как производные углеводородов. В средней школе, в основном, изучают предельные моноамины, а из ароматических аминов только анилин (фениламин).
Аминокислоты - это органические вещества, в молекулах которых содержатся амино- (-NH2) и карбоксильная (-СООН) группы.
Белки - это высокомолекулярные органические соединения сложного состава и строения, в молекулах которых остатки а-аминокислот соединены между собой пептидной связью.
Нитросоединения
Предполагают, что прототипом современных взрывчатых веществ является "греческий огонь", который был разработан в конце VII века. В последующие годы для изготовления взрывчатых смесей применялись в основном производные азотной кислоты, в том числе и нитросоединения. В годы Первой мировой войны для изготовления артиллерийских снарядов широко использовали пикриновую кислоту и ее соли, а также тротил.
Органические соединения, в молекулах которых одна или несколько нитрогрупп (-NO2) связаны с углеводородным радикалом, называются нитросоединениями. Например, CH3-NO2, C2H5-NO2, C3H7-NO2 и др. - нитросоединения. По природе углеводородного радикала нитросоединения можно подразделить на нитроалканы, ароматические нитросоединения и т.д.
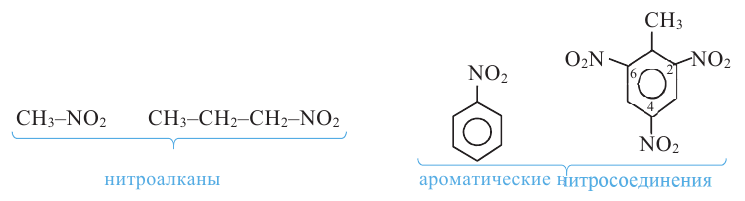
По Международной номенклатуре названия нитросоединений составляют добавлением приставки "нитро" к названию алкана, соответствующего углеводородному радикалу нитросоединения и при необходимости указывают место нитрогруппы в цепи цифрой, например:
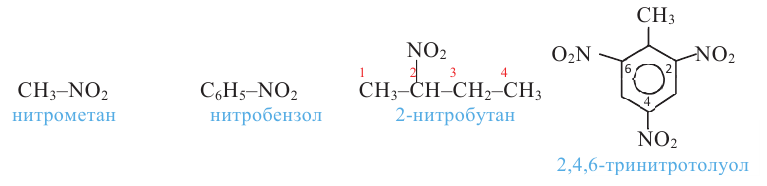
Изомерия в нитросоединениях обусловлена положением нитрогруппы в углеводородной цепи (1, 2) и строением этой цепи (3, 4), например:

В нитросоединениях валентность атома азота IV, а степень окисления равна +3. Как и в случае молекулы азотной кислоты, несмотря на то, что в нитрогруппе одна из N-O связей образована за счет неподеленной электронной пары атома азота, длина обеих связей N-O одинакова. Атом азота находится в состоянии sp2 гибридизации (а).
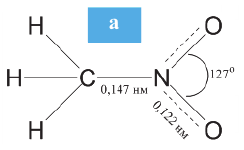
Получают нитросоединения в основном реакцией нитрования углеводородов. Нитроалканы получают взаимодействием алканов с разбавленной азотной кислотой (реакция Коновалова) или с парами этой кислоты 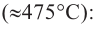
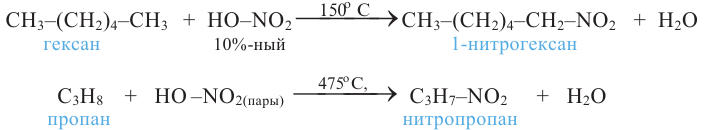
Ароматические углеводороды, по сравнению с другими углеводородами, легче нитруются. Их нитрование обычно проводят смесью концентрированных азотной и серной кислот:
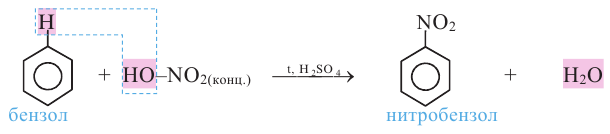
Нитросоединения получают также взаимодействием алкилгалогенидов с нитритом натрия:
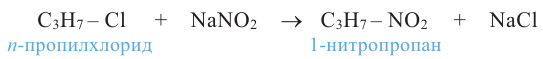
Важнейшее химическое свойство нитросоединений - превращение их в амины при восстановлении водородом:
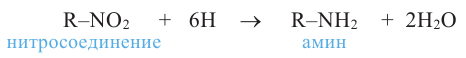
Нитросоединения используются в производстве аминов, альдегидов, карбоновых кислот. Полинитросоединения, например, 2,4,6-тринитротолуол, применяются в качестве взрывчатых веществ.
Амины
Номенклатура и изомерия:
В конце XIX века было установлено, что у людей, длительное время употребляющих очищенный рис, наблюдаются потеря веса и признаки расстройства нервной системы. В результате исследований было установлено, что причиной заболевания является отсутствие в пище этих людей вещества, содержащего аминогруппу (—NН2) и названного "витамином" (амин жизни), который присутствует только в кожуре риса.
Номенклатура: По Международной номенклатуре название предельного первичного амина составляют добавлением приставки "амино" к названию алкана, соответствующего углеводородному радикалу амина, например:

Начиная с амина состава C3H7NH2, цифрой указывают также и положение аминогруппы в цепи. Нумерацию атомов углерода цепи начинают с того конца, куда ближе аминогруппа:

По рациональной номенклатуре названия первичных аминов составляют путем прибавления к названию радикала слова "амин": CH3-NH2 метиламин, CH3-CH2-NH2 этиламин и др.
Вторичные и третичные амины называют в основном по рациональной номенклатуре; при этом радикалы называют в порядке от меньшего к большему.
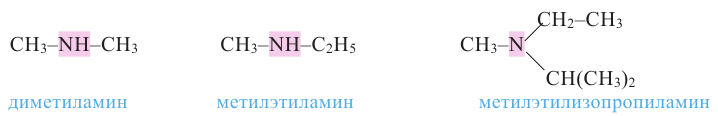
Примечание: Соединения, в которых атом азота соединен с четырьмя атомами или группами атомов, называют следующим образом: [RNН3]+ - катион алкиламмония, [(C2H5)2NH2]Cl - хлорид диэтиламмония и т.д.
Изомерия: У аминов структурная изомерия наблюдается по трем причинам:
1) по строению углеводородного радикала, например:

CH3-CH2-CH2-CH2-NH2
2) по положению аминогруппы -NH2 в углеводородной цепи, например:

3) по числу радикалов, присоединенных к атому азота, например:
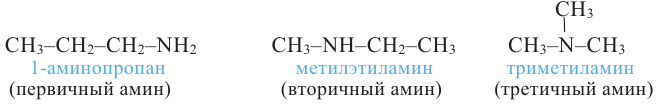
У аминов оптическая изомерия начинается с 2-аминобутана. В его молекуле вторичный атом углерода связан с 4 различными атомами и группами атомов (-Н, -NH2, -СН3, -С2Н5), в результате чего молекула существует в виде двух оптических изомеров.
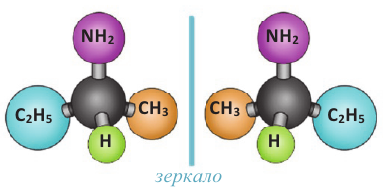
оптические изомеры 2-аминобутана
Получение, строение и физические свойства:
Алкиламины и ароматические амины, используемые в качестве лекарств, обычно принимают внутрь в виде их гидрохлоридных солей.
Получение: Предельные амины получают в основном восстановлением нитросоединений водородом:
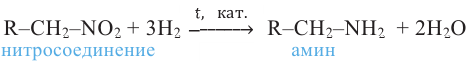
Алкиламины получают также и действием аммиака на спирты или алкилгалогениды:
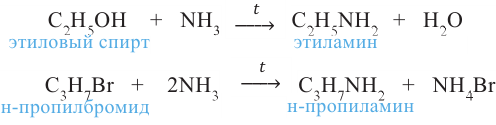
В последних двух реакциях образуется смесь первичных, вторичных и третичных аминов (RNH2, R2NH, R3N).
Электронное строение аминов: В молекулах аминов, как и в молекуле аммиака, атом азота находится в состоянии sp3 гибридизации и неподеленная пара электронов расположена на этой орбитали (а). Поэтому алкиламины, как и аммиак, обладают основными свойствами, т.е. амины - органические основания.
Поскольку алкильная группа, по сравнению с атомом водорода, имеет электронодонорные свойства, то на атоме азота алкиламина электронная плотность больше, чем в случае аммиака. Поэтому алкиламины проявляют большие основные свойства, чем аммиак. С ростом числа алкильных групп в молекуле основные свойства аминов усиливаются.
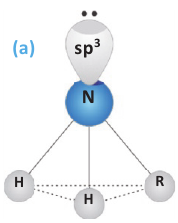
Поскольку фенильная группа, по сравнению с атомом водорода, имеет электроноакцепторные свойства, то на атоме азота анилина (С6Н5NН2) электронная плотность меньше, чем в случае аммиака. И, как следствие, у анилина основные свойства выражены слабее, чем у аммиака.
С ростом числа фенильных групп в молекуле ароматических аминов их основные свойства ослабляются.
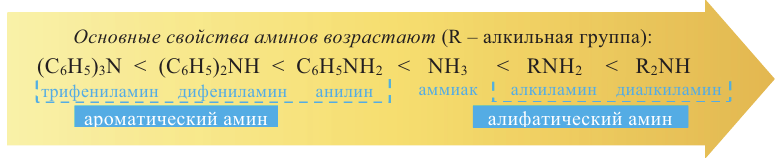
Пример №4
Расположите вещества в порядке возрастания их основных свойств.
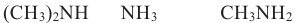
Решение:
Поскольку алкильная (метильная) группа имеет электронодонорные свойства, то основные свойства увеличиваются в ряду 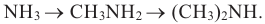
Физические свойства: Первые представители предельных аминов - метиламин, диметиламин, триметиламин - газы, хорошо растворимые в воде и обладающие аммиачным запахом, средние члены - жидкости с запахом тухлой рыбы, высшие амины 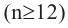 - твердые вещества без запаха.
- твердые вещества без запаха.
В водных растворах молекулы аминов образуют водородную связь с молекулами воды. Поэтому амины, по сравнению с углеводородами примерно одинаковой молекулярной массы, в воде лучше растворяются. С ростом относительной молекулярной массы растворимость уменьшается. Межмолекулярная водородная связь в алкиламинах.
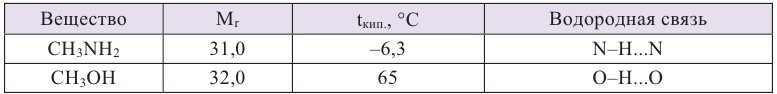
Первичные и вторичные амины содержат полярную N-H связь. Поэтому их молекулы также образуют между собой водородную связь типа N-H...N.
Однако водородная связь N-H...N слабее водородной связи O-Н...O. По этой причине метиламин кипит при более низкой температуре, чем метанол, имеющий почти такую же относительную молекулярную массу:
Химические свойства и применение:
Из-за схожести запаха низших аминов с запахом аммиака их путали с аммиаком. Лишь в 1849 г. Француский химик Шарль Вюрц обратил внимание на то, что амины горят на воздухе, и на основании своих новых представлений ему удалось синтезировать метиламин и этиламин.
Химические свойства предельных аминов, главным образом, определяются их основными свойствами.
Химические свойства: Поскольку алкиламины обладают основными свойствами, то в водном растворе они окрашивают лакмус в синий цвет:
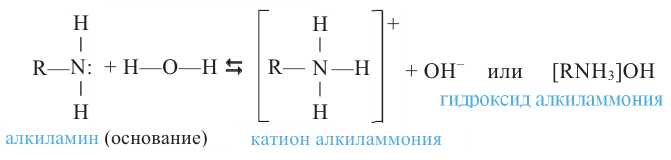
Другими словами, амины - органические основания. По этой причине предельные амины с водой образуют гидроксиды алкиламмония, с кислотами - растворимые в воде соли алкиламмония:

Соли алкиламмония в воде диссоциируют, а при действии щелочей разлагаются с выделением амина:
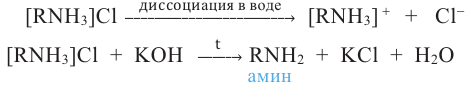
В отличие от аммиака амины горят на воздухе:
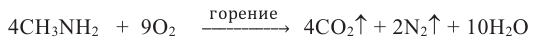
Пример №5
Завершите схемы и назовите органические вещества реакций:

Решение:
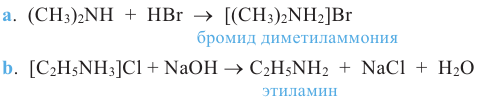
Применение. Предельные амины используются в качестве оснований, ингибиторов, флотореагентов и экстрагентов, а также в синтезе некоторых лекарственных препаратов, синтетических волокон (нейлона) и др.
Анилин
Анилин, как и некоторые амины, очень ядовитое вещество. Он, проникая через кожу в кровь, нарушает функции гемоглобина. При больших концентрациях или длительном воздействии анилина возможен и смертельный исход. Поэтому при попадании на кожу анилина его быстро смывают ватой, смоченной в спирте.
Анилин С6Н5NН2: (аминобензол, фениламин) - простейший представитель ароматических аминов (по арабе, an-nil- темно-синий).
Получение: Анилин получают в основном восстановлением нитробензола. Эту реакцию впервые осуществил Н. Н. Зинин, который в качестве восстановителя использовал сульфид аммония:
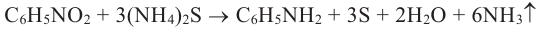

Н. Н. Зинин (1812-1880) Русский химик-органик
В 1842 году открыл реакцию восстановления ароматических нитросоединений и получил анилин. Доказал основные свойства аминов.
В промышленности анилин получают восстановлением нитробензола атомарным водородом или в присутствии катализатора молекулярным водородом:
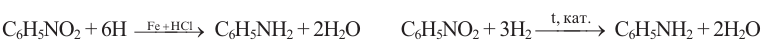
Анилин можно получить также взаимодействием хлорбензола с аммиаком:
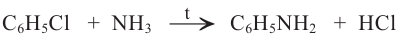
Физические свойства: Анилин - бесцветная маслянистая жидкость, с характерным запахом, тяжелее воды, ядовит. В воде плохо, а в спирте, эфире и бензоле хорошо растворим. На воздухе темнеет (чернеет) в результате частичного окисления.
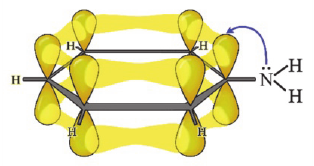
Строение: Электронное строение анилина приведено на схеме. Из схемы видно, что неподеленная пара электронов атома азота смещается в сторону 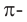 электронной системы бензольного кольца. Это смещение находит свое отражение в химических свойствах анилина:
электронной системы бензольного кольца. Это смещение находит свое отражение в химических свойствах анилина:
- 1) из-за уменьшения электронной плотности на атоме азота основные свойства анилина по сравнению с аммиаком ослабевают;
- 2) реакция замещения бромом атомов Н, соединенных с атомами C в положениях кольца 2,4,6-, облегчается по сравнению с бензолом.
Химические свойства:
I. Основные свойства (влияние фенильной группы на аминогруппу). Из-за уменьшения основных свойств анилина по сравнению с аммиаком он, в отличие от алкиламинов и аммиака, в водном растворе не изменяет фиолетовый цвет лакмуса, однако с сильными кислотами образует соли:
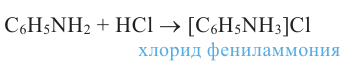 или
или 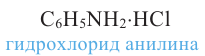
При действии щелочей эти соли разлагаются, выделяя анилин:

II. Реакции бензольного кольца (влияние аминогруппы на бензольное I кольцо). Из-за влияния аминогруппы на бензольное кольцо реакции замещения атомов водорода, соединенных с атомами углерода в положениях кольца о 2,4,6-, облегчаются. Например, анилин, в отличие от бензола, легко реагирует (без нагревания и без катализатора) не только с бромом, но даже с бромной водой, образуя белый осадок 2,4,6-триброманилина:
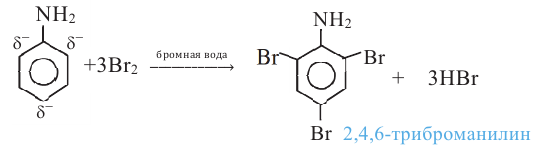
Бензол же с бромной водой не реагирует. В отличие от бензола, анилин также окисляется кислородом воздуха и другими окислителями, образуя вещества разной окраски, например, применяемый в качестве красителя "черный анилин".
Применение. Анилин как исходное сырье используется для получения анилиновых красителей, лекарственных веществ (белый стрептоцид, новокаин, сульфадемизин и др.), анилииформальдегидных смол и и др.
Определение. Анилин определяют по образованию фиолетовой окраски при действии на него хлорной известью.
Аминоксилоты
Номенклатура, изомерия, получение и строение:
Аминокислоты в организме выполняют различные функции. Например, большинство аминокислот, поступающих в организм в виде белков, участвуют в построении клеток мышечных тканей.
Аминокислоты - это органические вещества, в молекулах которых содержатся и амиио- (-NH2), и карбоксильная (-СООН) группы.
Аминокислоты рассматриваются как производные карбоновых кислот, в углеводородном радикале которых атом водорода замещен на аминогруппу (-NH2), обладающую основными свойствами, например:

Гидролизом природных белков получено около 20 аминокислот. У природных аминокислот амино- и карбоксильная группы соединены с одним и тем же атомом углерода. Такие аминокислоты называют 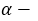 аминокислотами. Общую формулу
аминокислотами. Общую формулу 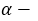 аминокислот изображают так:
аминокислот изображают так:
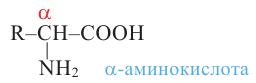
Ряд аминокислот синтезирован и в химических лабораториях. Такие аминокислоты называют синтетическими аминокислотами.
Примерно половина из 20 природных аминокислот называются незаменимыми аминокислотами (например, валин, лейцин и др.), поскольку они не могут быть синтезированы в организме человека. По этой причине они должны поступать в организм при приеме пищи. Аминокислоты же, которые синтезируются в организме в процессе обмена веществ, называются заменимыми аминокислотами (например, глицин, аланин и др.).
Номенклатура: Названия аминокислот по Международной номенклатуре образуют из названия соответствующей карбоновой кислоты с добавлением приставки "-амино" и указанием положения аминогруппы в цепи цифрой.
Нумерацию атомов углерода цепи начинают с атома углерода карбоксильной группы:
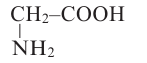
Международная ном-ра: аминоэтановая кислота
Тривиальная ном-ра: глицин или гликоколь
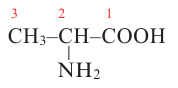
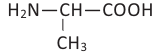
Международная ном-ра: 2-аминопропановая кислота
Тривиальная ном-ра: 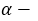 аланин
аланин
По рациональной номенклатуре положение аминогруппы в цепи указывают буквами греческого алфавита 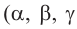 и др.). В этом случае обозначение начинают с атома углерода, связанного с карбоксильной группой:
и др.). В этом случае обозначение начинают с атома углерода, связанного с карбоксильной группой:
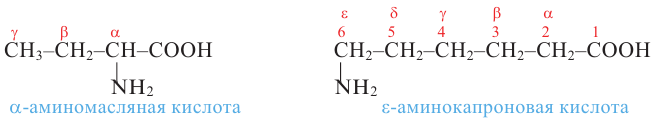
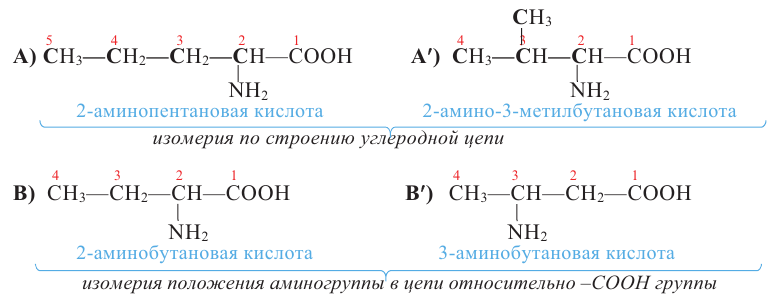
Изомерия: Для аминокислот характерны два вида изомерии - структурная и пространственная (стереоизомерия). Структурная изомерия обусловлена строением углеродной цепи 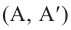 и положением аминогруппы в цепи относительно карбоксильной -СООН группы
и положением аминогруппы в цепи относительно карбоксильной -СООН группы 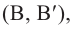 например:
например:
Стереоизомерия (оптическая активность) аминокислот:
Из-за наличия в молекуле аминокислот (за исключением глицина) асимметрического атома углерода аминокислоты обладают стереоизомерией.
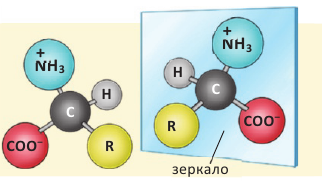
Получение: Аминокислоты получают гидролизом белков
а также действием аммиака на галогенпроизводные карбоновых кислот и др. способами:

Строение: Поскольку в молекулах аминокислот содержатся амино- и карбоксильная группы, то они проявляют и основные, и кислотные свойства, т.е. аминокислоты - органические амфотерные соединения. В их водных растворах происходит реакция внутримолекулярной нейтрализации: ион водорода карбоксильной группы, присоединяясь к аминогруппе, образует внутреннюю соль (биполярный ион, цвиттер-ион):
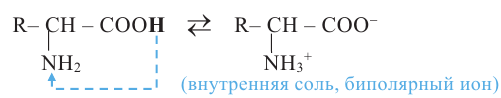
Такое же строение аминокислоты имеют и в твердом состоянии. В растворе и в твердом состоянии аминокислоты не существуют в виде молекул. Биполярное строение объясняет многие их физические и химические свойства.
Свойства и применение:
В результате изучения строения аминокислот, было установлено, что наряду с неорганическими амфотерными соединениями, существуют также и органические амфотерные соединения.
Физические свойства: Аминокислоты - бесцветные кристаллические вещества, хорошо растворимые в воде и плавящиеся с разложением при температуре выше 250°С. Их водные растворы проводят электрический ток. Многие из них имеют сладкий вкус.
Химические свойства:
A Действие на индикаторы. Растворы аминокислот, в молекуле которых содержится одинаковое число амино- и карбоксильных групп, имеют нейтральную среду и на индикаторы не действуют.
Аминокислоты со слабыми кислотными и основными свойствами:
Если в молекуле аминокислоты число карбоксильных групп больше, чем число аминогрупп, то она проявляет слабые кислотные свойства (А), если больше число аминогрупп (В), то среда имеет слабые основные свойства, например:
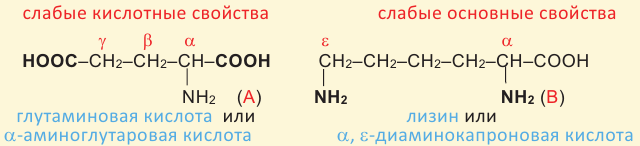
B Кислотные свойства. Аминокислоты реагируют с активными металлами, основными оксидами, основаниями, солями слабых кислот и со спиртами:
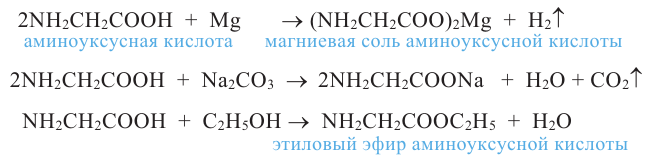
C Основные свойства. Аминокислоты с участием аминогруппы взаимодействуют с сильными неорганическими кислотами, образуя соли:

Таким образом, аминокислоты - органические амфотерные соединения.
D Образование пептидной связи. Аминокислоты также реагируют и между собой, за счет -СООН группы одной кислоты и -NH2 группы другой:
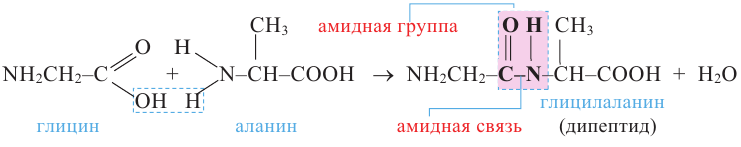
Группа атомов -CO-NH- называется пептидной или амидной группой, а связь между атомами углерода и азота - пептидной или амидной связью.
Продукт реакции, состоящий из остатков двух кислот, называют дипептидом. Поскольку дипептид также содержит амино- и карбоксильную группы, то он может вступать в реакцию с третьей, четвертой и т.д. молекулами аминокислоты. В зависимости от числа молекул аминокислот, вступивших в реакцию, образуются дипептиды, трипептиды, тетрапептиды и т.д., например: (А изображает аминокислоту, А' - остаток аминокислоты):
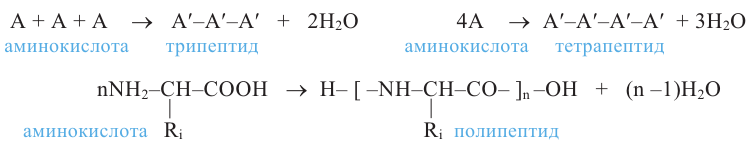
Последняя реакция называется реакцией поликонденсации.
Применение: В живых организмах белки синтезируются из аминокислот. Человек и животные получают эти аминокислоты с белковой пищей. В медицине аминокислоты используются как лечебные средства (лизин, гистидин, триптофан, метионин), в сельском хозяйстве - в качестве добавок к кормам животных (лизин, метионин). Из 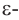 аминокапроновой и
аминокапроновой и 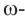 аминоэнантовой кислот, имеющих неразветвленную углеродную цепь, получают волокна капрона и энанта.
аминоэнантовой кислот, имеющих неразветвленную углеродную цепь, получают волокна капрона и энанта.
Белки
Строение:
Белки мяса, молока и яиц, с точки зрения питательной ценности для человека, более важны, чем растительные, потому что аминокислотный состав первых ближе к аминокислотному составу органов и клеток человека.
Белки - это высокомолекулярные органические соединения сложного состава и строения, в молекулах которых остатки а-аминокислот соединены между собой пептидной связью.
Белки образованы, в основном, 20 разными  аминокислотными остатками. В таблице приведены названия и формулы некоторых
аминокислотными остатками. В таблице приведены названия и формулы некоторых  аминокислот.
аминокислот.
Ряд аминокислот, полученных из белков (в скобках указано их сокращенное обозначение)
| заменимые | незаменимые |
|
Глицин (Гли) |
Валин (Вал) |
|
Аланин (Ала) |
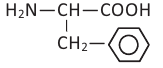
Фенилаланин (Фен) |
|
Цистеин (Цис) |
Лейцин (Лей) |
Белки (протеины) образуются поликонденсацией  аминокислот. В молекулах белков аминокислотные остатки связаны между собой пептидной связью (-CO-NH-):
аминокислот. В молекулах белков аминокислотные остатки связаны между собой пептидной связью (-CO-NH-):
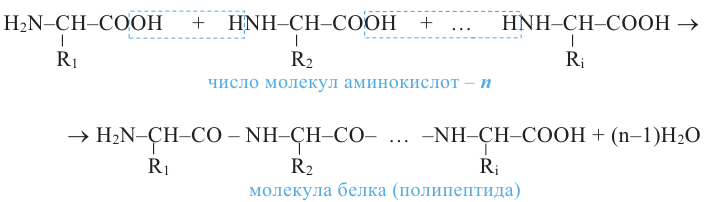
Важные данные о строении и химии белков были получены в результате исследований русского биохимика А. Я. Данилевского и немецкого химика-органика Э. Фишера.
Белки могут быть классифицированы по различным признакам:
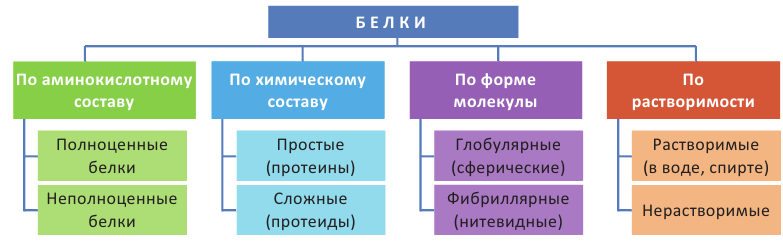
Белки, содержащие в своем составе наряду с остатками заменимых аминокислот и остатки всех незаменимых аминокислот, называются полноценными, не содержащие их - неполноценными белками. Полноценные белки в основном имеют животное происхождение. Так, в яичном белке содержатся почти все необходимые человеку аминокислоты и в нужном соотношении.
При гидролизе протеинов образуются только 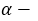 аминокислоты. При гидролизе же протеидов, наряду с
аминокислоты. При гидролизе же протеидов, наряду с 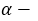 аминокислотами, образуются также вещества небелковой природы (углеводы, нуклеиновые кислоты, ортофосфорная кислота, липиды и др.).
аминокислотами, образуются также вещества небелковой природы (углеводы, нуклеиновые кислоты, ортофосфорная кислота, липиды и др.).
Растворимые белки обычно имеют сферическую форму. К таким белкам относятся, например, гемоглобин (белок крови), альбумин (яичный белок), инсулин (белок поджелудочной железы).
Нерастворимые белки, как правило, имеют нитевидную форму. К ним относятся, например, фиброин (белок природного шелка), коллаген (белок мыщц и соединительной ткани), 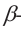 кератин (белок волос и ногтей) (1).
кератин (белок волос и ногтей) (1).
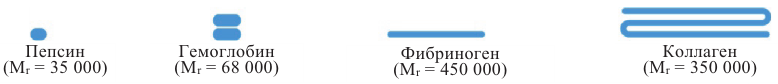
(1) Формы молекул и относительные молекулярные массы некоторых белков
Белки подразделяют также и по тем функциям, которые они выполняют в организме.
Структура белков:
Установлены первичная, вторичная, третичная и четвертичная структуры молекулы белка.
Первичная структура белка - это последовательность аминокислотных остатков в полипептидной цепи. Так, первичная структура белка, изображенного на схеме 1, определяется a-b-c-d-e-f-g... последовательностью аминокислотных остатков, образующих этот белок.
Если в цепи аминокислотных остатков изменяется их последовательность или число, то первичная структура также изменяется. По этой причине из 20 различных 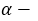 аминокислот возможно образование тысяч и миллионов белков.
аминокислот возможно образование тысяч и миллионов белков.
(1) Первичная, вторичная, третичная и четвертичная структуры простого белка
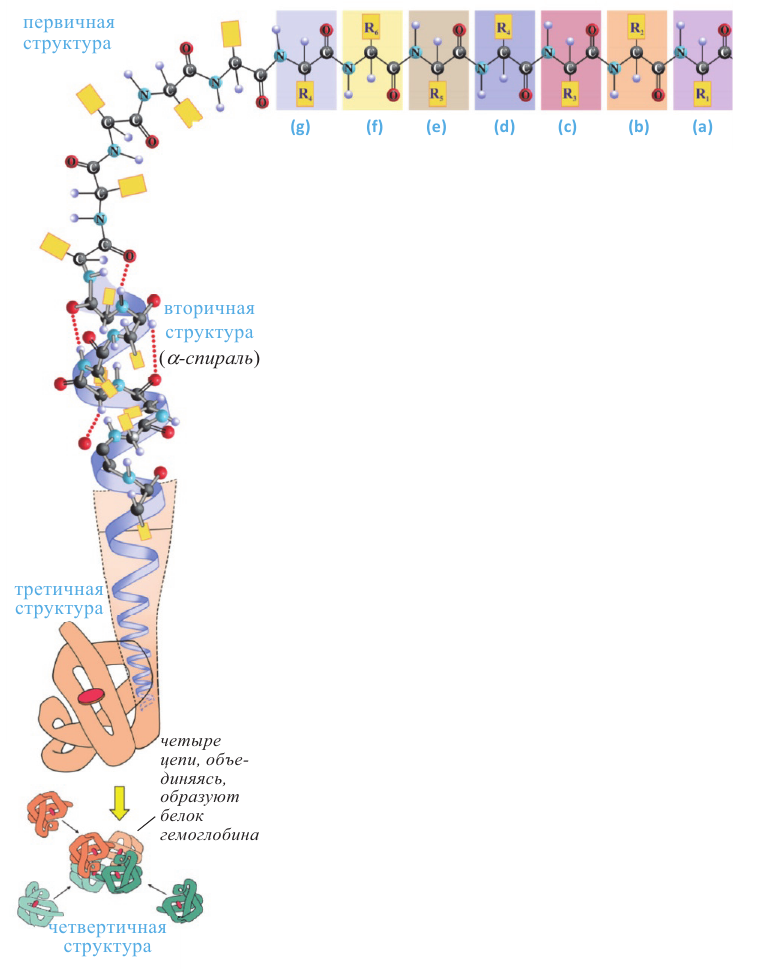
Вторичная структура белка - это форма, которую имеют отдельные участки полипептидной цепи в пространстве. Полипептидные цепи многих природных белков имеют спиралеобразную форму. Такая форма вторичной структуры белка получила название 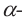 спирали (см: сx. 1 - вторичная структура).
спирали (см: сx. 1 - вторичная структура).
Вторичная структура образуется за счет водородных связей (C=O...H-N), которые возникают между -СО-и -NH группами, расположенными на соседних витках спирали.
Третичная структура белка - это форма, которую приобретает спираль в пространстве. В простейшем случае третичную структуру молекулы белка можно представить в виде клубка, как например, в случае клубка одной полипептидной цепи гемоглобина (см: сх.1)
Третичная структура белка образуется за счет дисульфидных (-S-S-) и солевых (-H3N+... -ООС-) мостиков, а также сложноэфирных (-COO-R) и водородных (-CO...HN-) связей, возникающих между функциональными группами, направленными наружу от спирали.
Биологическая активность белка определяется, главным образом, его третичной структурой.
Четвертичная структура белка связана с определенным расположением в пространстве нескольких полипептидных цепей белковой молекулы.
Эта структура наблюдается, если белок состоит из нескольких полипептидных цепей (обычно у таких белков 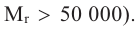 Например, четвертичная структура молекулы гемоглобина (Мr = 68 000) обусловлена расположением четырех полипептидных цепей, так как это показано на схеме 1.
Например, четвертичная структура молекулы гемоглобина (Мr = 68 000) обусловлена расположением четырех полипептидных цепей, так как это показано на схеме 1.
Четвертичная структура возникает за счет тех же сил, которые определяют третичную структуру белка, однако в этом случае они действуют между разными полипептидными цепями.
Содержание белков в некоторых продуктах питания (в %)
| Мясо | 18-22 | Сыр | 20-36 | Ржаной хлеб | 7,8 | Молоко | 3,5 |
| Рыба | 17-22 | Яйцо | 13 | Рис | 8 |
Свойства и применение:
Впервые белок был выделен в 1728 г итальянским ученым Я. Б. Беккари из пшеничной муки. При изучении свойств белков было установлено, что они, в отличие от жиров, углеводов и других органических веществ, обладают "специфическим свойством". По этой причине белки выделили в отдельный биологический класс веществ.
Физические свойства: Часть белков (глобулярные) растворяются в воде с образованием коллоидных растворов, другая часть - в разбавленных растворах солей, а фибриллярные белки в воде не растворяются совсем. Некоторые белки существуют и в кристаллическом состоянии. Белки - электролиты.
Химические свойства: Характерные химические свойства белков обусловлены их способностью вступать в цветные реакции, подвергаться гидролизу и денатурации.
Гидролиз: Гидролиз белков - одно из важнейших их свойств. Гидролиз белков происходит или под действием ферментов, или же при нагревании их с кислотами или щелочами. Конечный продукт гидролиза - 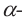 аминокислоты:
аминокислоты:
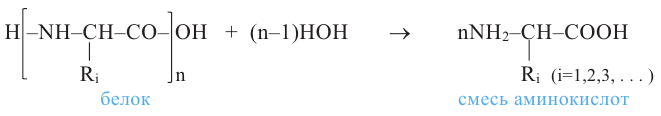
Данные о составе и химическом строении белков получают именно в результате их гидролиза. Гидролиз белков - основа процесса пищеварения.
Денатурация - это разрушение вторичной и третичной структуры белка (1). Денатурация происходит под действием щелочей, сильных кислот, этанола, солей тяжелых металлов (Hg, Pb, Fe и др.), радиации и нагревания.
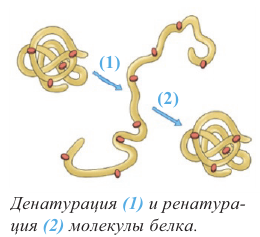
При варке яиц, приготовлении пищи, свертывании крови, скисании молока и в др. случаях мы наблюдаем явление денатурации.
При денатурации белок теряет специфическую пространственную форму молекулы (1), биологическую активность и растворимость в воде.
Если фактор, вызывающий денатурацию, действует кратковременно или слаб, то первоначально осажденный белок растворяется, восстанавливая исходное строение и свойства (2). Такое явление называют ренатурацией.
Определение (цветные реакции): Белки определяют по их характерным цветным реакциям (а, b, с), а также по запаху жженых перьев при сильном нагревании белков.
- a При действии на растворы белков в щелочной среде сульфатом меди (II) раствор окрашивается в красно-фиолетовый цвет (d). Эту реакцию называют биуретовой реакцией и используют для доказательства присутствия в веществе пептидной связи.
- b При действии концентрированной азотной кислоты на белки, молекулы которых содержат ароматическую аминокислоту, наблюдается желтое окрашивание (бензольное кольцо нитруется).
- c При действии на растворы белка, содержащего в своем составе серу, ацетата свинца (II) и гидроксида натрия с последующим нагреванием наблюдается выпадение черного осадка сульфида свинца (II).
Получение: Белки образуются в клетках человека, животных и растений. Процесс образования белков из аминокислот, протекающий в клетках живых организмов, называется биосинтезом. Биосинтез протекает с участием нуклеиновых кислот.
Значение белков и их применение: Белки - важная составная часть живых организмов. Они входят в состав протоплазмы и ядра растительных и живых клеток. Белки регулируют характерные признаки и функции живых организмов - рост, наследственность, движение, деятельность органов чувств, природу заболеваний, явление иммунитета и др. Недостаток белка в пище вызывает серьезные заболевания.
В настоящее время многие из белковых веществ, например, гормоны и ферменты, получают биотехнологическими методами с помощью микроорганизмов. В промышленности белки применяются в виде природных волокон (шелка, шерсти), кожи, пластмасс и клеев.
Выводы:
- Амины - это производные аммиака, в молекуле которого атомы водорода
- замещены углеводородными радикалами.
- Амины состава RNH2, R1R2NH и R1R2R3N называются, соответственно, первичными, вторичными и третичными.
- Метиламин (CH3NH2)- предельный, фениламин (C6H5NH2)- ароматический амин.
- Структурная изомерия аминов обусловлена строением углеводородного радикала, положением аминогруппы в цепи и числом радикалов, присоединенных к атому азота.
- Амины - органические основания.
- Основные свойства аминов обусловлены наличием неподеленной электронной пары атома азота.
- Алкиламины проявляют более сильные основные свойства, чем аммиак.
- С ростом числа алкильных радикалов основные свойства аминов усиливаются.
- Основные свойства анилина слабее, чем у аммиака.
- С ростом числа фенильных радикалов основные свойства ароматических аминов ослабевают.
- Предельные амины получают восстановлением нитросоединений водородом.
- Нитрометан (CH3NO2) и 2,4,6-тринитробензол [С6Н3(МO2)3] - нитросоединения.
- Предельные амины с кислотами образуют соли алкиламмония.
- При действии щелочи на соли аминов они разлагаются с выделением амина.
- В молекуле анилина аминогруппа и фенильный радикал влияют друг на друга.
- Водный раствор анилина не изменяет цвет красной лакмусовой бумаги.
- Аминокислоты - органические вещества, содержащие в своем составе амино-и карбоксильную группы.
- В
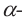 аминокислотах -NH2 и -СООН группы присоединены к одному атому С.
аминокислотах -NH2 и -СООН группы присоединены к одному атому С. - У аминокислот наблюдается структурная и пространственная изомерия.
- При гидролизе белков образуются аминокислоты.
- В водных растворах аминокислот протекает внутримолекулярная нейтрализация.
- Аминокислоты существуют в виде внутренней соли или биполярного иона.
- Аминокислоты - органические амфотерные соединения.
- Поликонденсацией аминокислот образуются полипептиды.
- Группу -CO-NH- называют пептидной группой, а связь C-N пептидной связью.
- В молекулах белков остатки аминокислот соединены между собой пептидной связью.
- Белки имеют первичную, вторичную, третичную и четвертичную структуры.
- Важнейшим химическим свойством белков является их гидролиз.
- Денатурация - разрушение вторичной и третичной структур белка.
- Белки определяют по характерным цветным реакциям и по появлению запаха жженых перьев при их сильном нагревании.
| Рекомендую подробно изучить предметы: |
| Ещё лекции с примерами решения и объяснением: |