
Для реакции, указанной в условии задачи, выписываем необходимые справочные данные
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
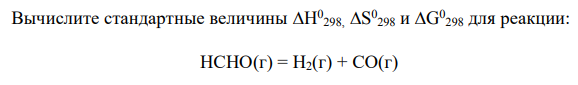
Объясните знак изменения энтальпии и энтропии. Возможно ли самопроизвольное протекание данной реакции при стандартных условиях?
Решение
H (энтальпия), S (энтропия) и G (свободная энергия Гиббса или термодинамический потенциал) являются термодинамическими функциями состояния и обладают общим свойством: их изменение в ходе химической реакции не зависит от пути этой реакции, а определяется только начальными и конечными веществами.
Это позволяет вычислять 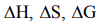 для реакции общего вида aA + bB = cC + dD по формулам:
для реакции общего вида aA + bB = cC + dD по формулам:
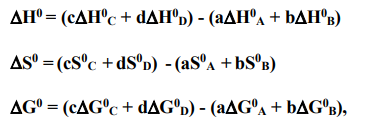


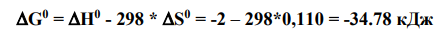
Изменения термодинамических функций H, S, G в ходе химической реакции позволяют судить об особенностях протекания данной реакции и ее природе. 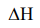 определяет величину теплового эффекта химической реакции. Процесс, характеризующийся величиной говорит о том, что тепло в ходе реакции поглощается, такие реакции называются эндотермическими. В данной реакции величина
определяет величину теплового эффекта химической реакции. Процесс, характеризующийся величиной говорит о том, что тепло в ходе реакции поглощается, такие реакции называются эндотермическими. В данной реакции величина 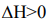 следовательно, тепло выделяется, и реакция является экзотермической. S характеризует изменение степени неупорядоченности системы. Возрастание энтропии
следовательно, тепло выделяется, и реакция является экзотермической. S характеризует изменение степени неупорядоченности системы. Возрастание энтропии 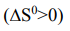 говорит о возрастании неупорядоченности в расположении и перемещении частиц в ходе химической реакции. Это происходит, например, при превращении твердых веществ в жидкие или газообразные или при увеличении количеств газообразных веществ. Напротив, уменьшение энтропии
говорит о возрастании неупорядоченности в расположении и перемещении частиц в ходе химической реакции. Это происходит, например, при превращении твердых веществ в жидкие или газообразные или при увеличении количеств газообразных веществ. Напротив, уменьшение энтропии 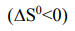 что свидетельствует об увеличении (увеличении или уменьшении?) неупорядоченности в данной системе. Действительно, из уравнения реакции видно, что в ходе реакции из 1 моль газообразных веществ HCHO(г) образуется 2 моль газообразных веществ H2(г) и CО(г), следовательно, степень неупорядоченности увеличивается (увеличивается или уменьшается?).
что свидетельствует об увеличении (увеличении или уменьшении?) неупорядоченности в данной системе. Действительно, из уравнения реакции видно, что в ходе реакции из 1 моль газообразных веществ HCHO(г) образуется 2 моль газообразных веществ H2(г) и CО(г), следовательно, степень неупорядоченности увеличивается (увеличивается или уменьшается?).
Величина 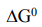 позволяет судить о принципиальной возможности самопроизвольного протекания химической реакции при стандартных
позволяет судить о принципиальной возможности самопроизвольного протекания химической реакции при стандартных
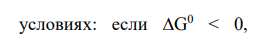 данная химическая реакция принципиально осуществима при стандартных условиях, если же
данная химическая реакция принципиально осуществима при стандартных условиях, если же 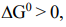 то нет (в этом случае осуществима обратная реакция). Состояние химического равновесия в системе отвечает равенству
то нет (в этом случае осуществима обратная реакция). Состояние химического равновесия в системе отвечает равенству 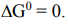
Для рассматриваемой в задаче реакции вычисленная величина 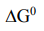
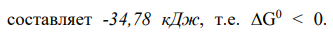 Следовательно, данная химическая реакция при стандартных условиях принципиально осуществима (осуществима или не осуществима).
Следовательно, данная химическая реакция при стандартных условиях принципиально осуществима (осуществима или не осуществима).

Похожие готовые решения по химии:
- Укажите, как необходимо изменить внешние параметры (температуру, общее давление, концентрации реагентов), чтобы сместить равновесие вправо
- Нужно провести вычисления и найти недостающие величины водных веществ и заполнить таблицу
- Для ответов на вопросы задачи вычислим степени окисления атомов, входящих в состав приведенных в уравнении реакции веществ, руководствуясь следующими правилами
- Более отрицательной величиной электродного потенциала характеризуется металл Mn, поэтому именно он и будет участником анодного процесса
- Как будет происходить электролиз водного раствора электролита NaCl (t = 25 мин, I = 8 А)? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях
- Следовательно, заряд ядра атома есть суммарный заряд его протонов (нейтроны заряда не несут), а массовое число – суммарная масса протонов и нейтронов
- Охарактеризуйте валентные состояния атомов данного элемента в основном и возбужденных состояниях с помощью электронно-графических формул
- Определите тип химической связи (неполярная ковалентная, полярная ковалентная или ионная) в веществах нитрид лития и дихлорид серы
- Определите тип химической связи (неполярная ковалентная, полярная ковалентная или ионная) в веществах нитрид лития и дихлорид серы
- Охарактеризуйте валентные состояния атомов данного элемента в основном и возбужденных состояниях с помощью электронно-графических формул
- В краткосрочном периоде фирма производит 500 ед. продукции. Средние переменные издержки составляют 2 ден.ед., средние постоянные
- В течение рабочего дня две швеи А и Б шьют пальто и куртки. Швея А может сшить 5 пальто

