
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
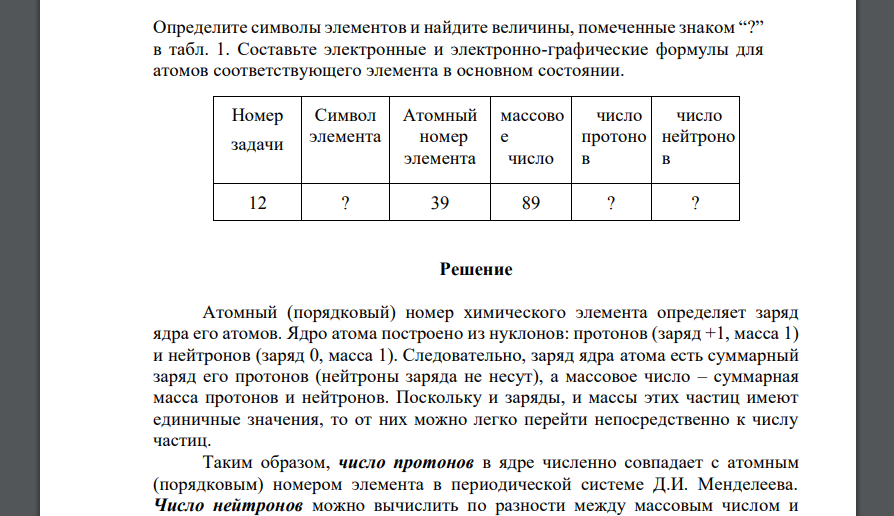
Определите символы элементов и найдите величины, помеченные знаком
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16800 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
Определите символы элементов и найдите величины, помеченные знаком “?” в табл. 1. Составьте электронные и электронно-графические формулы для атомов соответствующего элемента в основном состоянии. Номер задачи Символ элемента Атомный номер элемента массово е число число протоно в число нейтроно в 12 ? 39 89 ? ?
Решение
Атомный (порядковый) номер химического элемента определяет заряд ядра его атомов. Ядро атома построено из нуклонов: протонов (заряд +1, масса 1) и нейтронов (заряд 0, масса 1). Следовательно, заряд ядра атома есть суммарный заряд его протонов (нейтроны заряда не несут), а массовое число – суммарная масса протонов и нейтронов. Поскольку и заряды, и массы этих частиц имеют единичные значения, то от них можно легко перейти непосредственно к числу частиц. Таким образом, число протонов в ядре численно совпадает с атомным (порядковым) номером элемента в периодической системе Д.И. Менделеева. Число нейтронов можно вычислить по разности между массовым числом и числом протонов. Массовое число указывается верхним индексом слева от символа элемента. Для указанного в условии задачи элемента: Символ элемента атомный номер (порядковый номер) заряд ядра массовое число число протонов число нейтронов Суммарный отрицательный заряд электронов в атоме компенсирует положительный заряд его ядра. Следовательно, число электронов в атоме равно числу протонов в его ядре. Для рассматриваемого в задаче элемента иттрий Y число электронов составляет: Электронная формула атома - это условная запись, в которой зашифровано распределение электронов данного атома по энергетическим уровням и подуровням. Энергетические подуровни заполняются электронами в порядке, соответствующем росту их энергии: Максимальная емкость подуровней: электрона, d - 10 электронов, p - 6 электронов, f – 14 электронов Электронная формула атома рассматриваемого элемента имеет вид: 1 При составлении электронно-графической формулы необходимо каждый энергетический подуровень представить графически как
Решение
Атомный (порядковый) номер химического элемента определяет заряд ядра его атомов. Ядро атома построено из нуклонов: протонов (заряд +1, масса 1) и нейтронов (заряд 0, масса 1). Следовательно, заряд ядра атома есть суммарный заряд его протонов (нейтроны заряда не несут), а массовое число – суммарная масса протонов и нейтронов. Поскольку и заряды, и массы этих частиц имеют единичные значения, то от них можно легко перейти непосредственно к числу частиц. Таким образом, число протонов в ядре численно совпадает с атомным (порядковым) номером элемента в периодической системе Д.И. Менделеева. Число нейтронов можно вычислить по разности между массовым числом и числом протонов. Массовое число указывается верхним индексом слева от символа элемента. Для указанного в условии задачи элемента: Символ элемента атомный номер (порядковый номер) заряд ядра массовое число число протонов число нейтронов Суммарный отрицательный заряд электронов в атоме компенсирует положительный заряд его ядра. Следовательно, число электронов в атоме равно числу протонов в его ядре. Для рассматриваемого в задаче элемента иттрий Y число электронов составляет: Электронная формула атома - это условная запись, в которой зашифровано распределение электронов данного атома по энергетическим уровням и подуровням. Энергетические подуровни заполняются электронами в порядке, соответствующем росту их энергии: Максимальная емкость подуровней: электрона, d - 10 электронов, p - 6 электронов, f – 14 электронов Электронная формула атома рассматриваемого элемента имеет вид: 1 При составлении электронно-графической формулы необходимо каждый энергетический подуровень представить графически как
Похожие готовые решения по химии:
- На основании положения химического элемента № 49 и его электронной формулы составьте прогноз его химических свойств
- Определите тип химической связи (неполярная ковалентная, полярная ковалентная или ионная) в веществах хлорид калия и трихлорид фосфора
- Вычислите стандартные величины H 0 298, S 0 298 и G 0 298 для реакции: C2Cl4(г) + Cl2(г) = C2Cl6(г) Объясните знак изменения энтальпии и энтропии
- Для реакции: C2Cl4(г) + Cl2(г) = C2Cl6(г) составьте кинетическое уравнение; составьте выражение для константы равновесия
- Вычислите константы равновесия окислительно-восстановительных реакций, сделайте вывод о направлении и полноте протекания реакций
- Рассчитайте окислительно-восстановительный потенциал полуреакции
- Подберите коэффициенты в следующих уравнениях реакций
- При спектральном определении содержания меди в сплаве получены следующие значения
- Раствор соляной кислоты был подвергнут электролизу в приборе для определения чисел переноса с платиновыми электродами.
- По данным для моляльности m и среднем ионном коэффициенте активности электролита А вычислите среднюю ионную активность и
- Оцените величины ΔН и ΔS реакции Fe2O3+3/2С(к)=3/2СО2(г)+2Fe(к). На их основании определите условия ее
- Числа переноса ионов в 0.9992 -нормальном растворе KCl определялись методом перемещения границы с индикаторным 0,80 -

