
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Проставьте степени окисления элементов в исходных веществах и продуктах реакции MnO2 + KClO3 + KOH = K2MnO4 + KCl + H2O
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16953 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
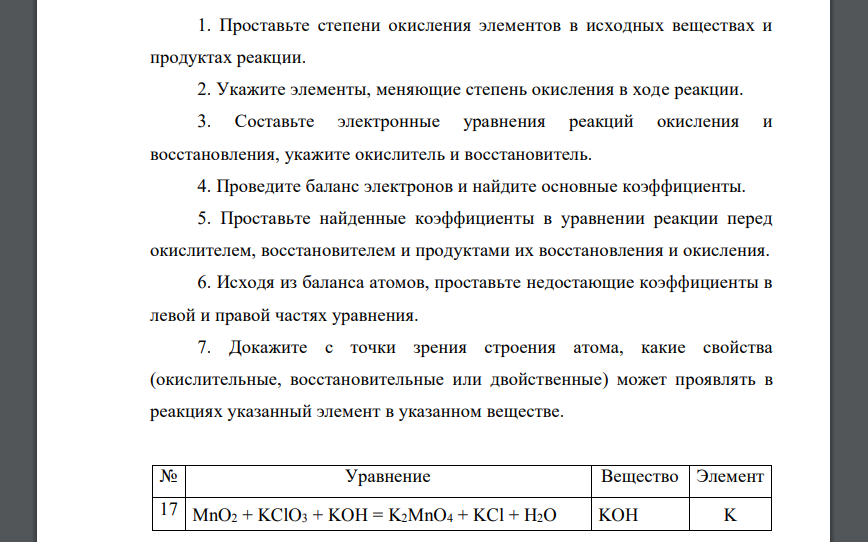
Проставьте степени окисления элементов в исходных веществах и продуктах реакции. 2. Укажите элементы, меняющие степень окисления в ходе реакции. 3. Составьте электронные уравнения реакций окисления и восстановления, укажите окислитель и восстановитель. 4. Проведите баланс электронов и найдите основные коэффициенты. 5. Проставьте найденные коэффициенты в уравнении реакции перед окислителем, восстановителем и продуктами их восстановления и окисления. 6. Исходя из баланса атомов, проставьте недостающие коэффициенты в левой и правой частях уравнения. 7. Докажите с точки зрения строения атома, какие свойства (окислительные, восстановительные или двойственные) может проявлять в реакциях указанный элемент в указанном веществе. № Уравнение Вещество Элемент 17 MnO2 + KClO3 + KOH = K2MnO4 + KCl + H2O KOH K
Решение:
Определим степени окисления всех элементов в соединениях. Степени окисления меняют Запишем уравнения процессов окисления и восстановления: Окисление: Восстановление: Окислителем является в восстановителем – Число отданных электронов должно быть равно числу принятых. Исходя из этого, составим схему электронного баланса и определим основные коэффициенты: (основные коэффициенты) Подберем остальные коэффициенты в уравнении реакции: Степень окисления равна Условно можно так записать электронно-графическую формулу в данной степени окисления: В данной степени окисления калий может только принимать электроны, заполняя свой пустой внешний уровень, т.е. проявляет только свойства окислителя.

Похожие готовые решения по химии:
- Исходя из значений стандартных электродных потенциалов, сделайте вывод, какой из электродов является анодом, какой – катодом Электроды 17 Zn, Со
- Определите анодные и катодные участки. При необходимости подберите нужный металл согласно заданию Посеребренное железо
- Приведите формулировки основных стехиометрических законов 20 N2O Ba(OH)2
- дайте названия по формулам и укажите формулы по названиям а иодид аммония, перманганат калия, ортофосфат цезия, перхлорат лития, карбонат калия
- Укажите характер связей в молекуле, для чего изобразите графическую формулу указанного соединения и рассчитайте H2CO3 GaCl3 [Cr(H2O)6]Cl3
- На основании агрегатных состояний веществ, участвующих в реакции, предположите ВаСО3(к) = ВаО(к) + СО2
- Запишите выражение закона действия масс (ЗДМ) для уравнения реакции данного варианта 2H2(г) + O2(г) = 2H2O
- Запишите выражение для константы равновесия для заданного уравнения реакции А(г) + В(г) = = С(г) + Д(г)
- Константа скорости реакции, протекающей по схеме 2А + В = С, 8 равна 5∙10-4 . Вычислите скорость реакции, если концентрации веществ А и В соответственно равны
- Запишите выражение для константы равновесия для заданного уравнения реакции А(г) + В(г) = = С(г) + Д(г)
- Исходя из значений стандартных электродных потенциалов, сделайте вывод, какой из электродов является анодом, какой – катодом Электроды 17 Zn, Со
- Из приведенных ниже значений термодинамических функций укажите те, которые являются критерием состояния равновесия в изолированной системе (Р, Т=const

