
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Запишите выражение для константы равновесия для заданного уравнения реакции H2(г) + Br2(г) = 2HBr(г)
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16953 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
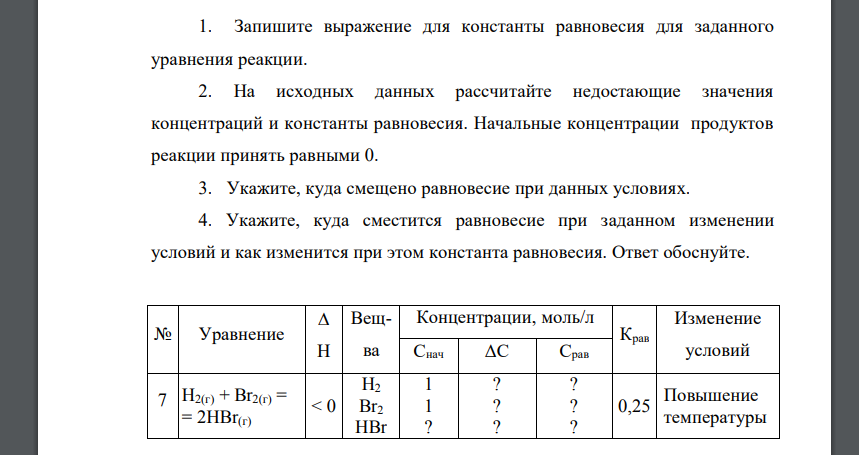
Запишите выражение для константы равновесия для заданного уравнения реакции. 2. На исходных данных рассчитайте недостающие значения концентраций и константы равновесия. Начальные концентрации продуктов реакции принять равными 0. 3. Укажите, куда смещено равновесие при данных условиях. 4. Укажите, куда сместится равновесие при заданном изменении условий и как изменится при этом константа равновесия. Ответ обоснуйте. № Уравнение Н Вещва Концентрации, моль/л Крав Изменение Снач ΔС Срав условий 7 H2(г) + Br2(г) = = 2HBr(г) < 0 H2 Br2 HBr 1 1 ? ? ? ? ? ? ? 0,25 Повышение температуры
Решение:
Выражение для константы равновесия: 2. Рассчитаем недостающие значения концентраций. Вещ-ва Концентрации Пусть в реакцию вступило По уравнению реакции определяем, что в ходе реакции образовалось Тогда равновесные концентрации равны: Подставляем в выражение для константы равновесия: 2 равн3. Поскольку Кравн то равновесие смещено влево, в сторону обратной реакции. 4. По принципу Ле-Шателье, при повышении температуры химическое равновесие сместится в сторону эндотермической реакции, т.е. влево

Похожие готовые решения по химии:
- Проставьте степени окисления элементов в исходных веществах и продуктах реакции Na2SO3 + KIO3 + H2SO4 = I2 + Na2SO4 + K2SO4 + H2O Na2SO3 S
- Исходя из значений стандартных электродных потенциалов, сделайте вывод, какой из электродов является анодом, какой – катодом 7 Ag, Pb
- Определите анодные и катодные участки. При необходимости подберите нужный металл согласно заданию Посеребренная медь
- Приведите формулировки основных стехиометрических законов SO2 NH4NO3
- Для приведенных элементов (см. задания в таблице 3): 1) укажите строение изотопов 32S,33S,34S,36S
- Укажите характер связей в молекуле, для чего изобразите графическую формулу указанного соединения и рассчитайте NaClO3
- На основании агрегатных состояний веществ, участвующих в реакции, предположите, как должна меняться энтропия системы 6H2O(г) + 4NO(г) = 5O2(г) + 4NH3(г)
- Запишите выражение закона действия масс (ЗДМ) для уравнения реакции данного варианта N2O(г) + H2O(ж) = 2NO(г) + H2(г)
- Сколько моль кальция вступило в реакцию с водой, если объем выделившегося водорода при 27 0С и 8,2 атм равен 3 л?
- Запишите выражение закона действия масс (ЗДМ) для уравнения реакции данного варианта N2O(г) + H2O(ж) = 2NO(г) + H2(г)
- Приведите структурные формулы, латинские и химические названия фурацилина (нитрофурал), фуразолидона
- К 100 мл 8% раствора HNO3 (ρ = 1,46 г/мл) прибавили 400 мл H2O. Получился раствор с плотностью 1,128 г/мл. Чему равна массовая доля (%) и

