
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Для приведенных элементов (см. задания в таблице 3): 1) укажите строение изотопов 32S,33S,34S,36S
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16953 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
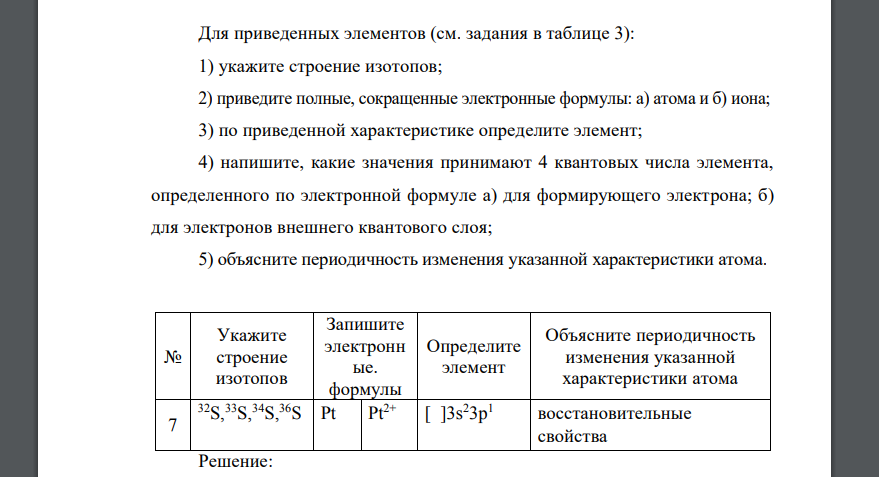
Для приведенных элементов (см. задания в таблице 3): 1) укажите строение изотопов; 2) приведите полные, сокращенные электронные формулы: а) атома и б) иона; 3) по приведенной характеристике определите элемент; 4) напишите, какие значения принимают 4 квантовых числа элемента, определенного по электронной формуле а) для формирующего электрона; б) для электронов внешнего квантового слоя; 5) объясните периодичность изменения указанной характеристики атома. № Укажите строение изотопов Запишите электронн ые. формулы Определите элемент Объясните периодичность изменения указанной характеристики атома 7 32S,33S,34S,36S Pt Pt2+ [ ]3s23p1 восстановительные свойства
Решение:
Ядро каждого атома состоит главным образом из протонов и нейтронов, вокруг которого движутся электроны. Почти вся масса атома сосредоточена в ядре. Заряд ядра определяется числом находящихся в нем протонов и равен Z. Сумма числа протонов и нейтронов дает массовое число (M) Совокупность атомов с одинаковым зарядом ядра называется химическим элементом. Разновидности элементов, атомы которых имеют одинаковый заряд ядра, но разные массовые числа, называют изотопами. Вид атомов Состав ядра Электронная оболочка 2) Платина имеет порядковый номер 78, что равно общему числу электронов. полная электронная формула сокращенная электронная формула. Ион содержит электронов. полная электронная формула сокращенная электронная формула иона. 3) III период, сумма внешних электронов ( группа, A подгруппа) − это алюминий 4) Формирующий электрон: Электроны внешнего электронного слоя: 5) Восстановительные свойства определяются способностью атомов отдавать электрон. По периоду слева направо увеличивается заряд ядра и уменьшается радиус атома, поэтому восстановительные свойства ослабевают. По группе сверху вниз увеличивается радиус атома, поэтому восстановительные свойства усиливаются.

Похожие готовые решения по химии:
- Укажите характер связей в молекуле, для чего изобразите графическую формулу указанного соединения и рассчитайте NaClO3
- На основании агрегатных состояний веществ, участвующих в реакции, предположите, как должна меняться энтропия системы 6H2O(г) + 4NO(г) = 5O2(г) + 4NH3(г)
- Запишите выражение закона действия масс (ЗДМ) для уравнения реакции данного варианта N2O(г) + H2O(ж) = 2NO(г) + H2(г)
- Запишите выражение для константы равновесия для заданного уравнения реакции H2(г) + Br2(г) = 2HBr(г)
- Исходя из значений стандартных электродных потенциалов, сделайте вывод, какой из электродов является анодом, какой – катодом Zn, Ag
- Определите анодные и катодные участки. При необходимости подберите нужный металл согласно заданию 1 Железное изделие + протектор
- Приведите формулировки основных стехиометрических законов NH3 Mg(OH)2
- дайте названия по формулам и укажите формулы по названиям нитрат гидроксокальция, оксид кобальта (III), гидросульфид калия, сульфат алюминия
- Дайте характеристику кислотно-основных и окислительновосстановительных свойств тримекаина, ксикаина, дикаина. Опишите
- Определите тип химических связей в молекулах, указанных в таблице 3. Изобразите схемы перекрывания валентных орбиталей при образовании ковалентных связей.
- Укажите типы реакций, приводящих к изменению веществ при хранении под влиянием факторов окружающей среды. Приведите примеры
- Обоснуйте определение подлинности кофеина по методике ГФ Х (ст. 172): к 0,01 г препарата помещают в фарфоровую чашку

