
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Кондуктометрия. Измерение сопротивления в методе кондуктометрии
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №16800 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
Кондуктометрия. Измерение сопротивления в методе кондуктометрии.
Ответ:
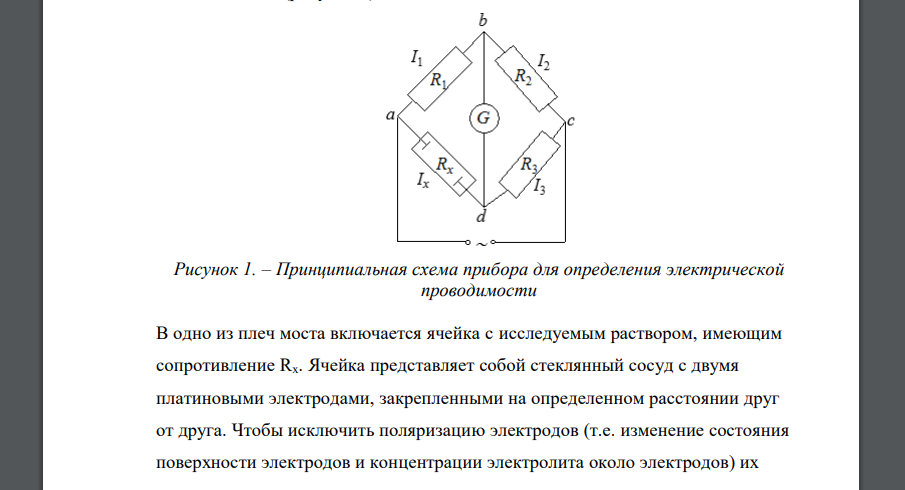
Методы исследования свойств растворов электролитов, основанные на определении электрической проводимости, называются кондуктометрическими (кондуктометрией). Наиболее часто кондуктометрия используется для определения концентрации растворов электролитов (кондуктометрическое титрование), определения констант диссоциации (или ионной ассоциации) электролитов, в физико-химическом анализе. В основе приборов для определения электрической проводимости лежит мостовая схема (рисунок 1). Рисунок 1. – Принципиальная схема прибора для определения электрической проводимости В одно из плеч моста включается ячейка с исследуемым раствором, имеющим сопротивление Rx. Ячейка представляет собой стеклянный сосуд с двумя платиновыми электродами, закрепленными на определенном расстоянии друг от друга. Чтобы исключить поляризацию электродов (т.е. изменение состояния поверхности электродов и концентрации электролита около электродов) их 268 покрывают платиновой чернью, а для питания используют обычно переменный ток. Установив определенную величину сопротивления R3, подбирают сопротивления R1 и R2 так, чтобы ток не проходил на участке ab. В момент, когда нуль-инструмент G (гальванометр, осциллограф) показывает отсутствие тока, согласно закону Кирхгофа Отсюда следует, что По значениям Rx рассчитывают удельную электрическую проводимость раствора:
Ответ:
Методы исследования свойств растворов электролитов, основанные на определении электрической проводимости, называются кондуктометрическими (кондуктометрией). Наиболее часто кондуктометрия используется для определения концентрации растворов электролитов (кондуктометрическое титрование), определения констант диссоциации (или ионной ассоциации) электролитов, в физико-химическом анализе. В основе приборов для определения электрической проводимости лежит мостовая схема (рисунок 1). Рисунок 1. – Принципиальная схема прибора для определения электрической проводимости В одно из плеч моста включается ячейка с исследуемым раствором, имеющим сопротивление Rx. Ячейка представляет собой стеклянный сосуд с двумя платиновыми электродами, закрепленными на определенном расстоянии друг от друга. Чтобы исключить поляризацию электродов (т.е. изменение состояния поверхности электродов и концентрации электролита около электродов) их 268 покрывают платиновой чернью, а для питания используют обычно переменный ток. Установив определенную величину сопротивления R3, подбирают сопротивления R1 и R2 так, чтобы ток не проходил на участке ab. В момент, когда нуль-инструмент G (гальванометр, осциллограф) показывает отсутствие тока, согласно закону Кирхгофа Отсюда следует, что По значениям Rx рассчитывают удельную электрическую проводимость раствора:

Похожие готовые решения по химии:
- Рассчитайте растворимость соли А в воде и ее произведение растворимости по значениям удельного сопротивления насыщенного раствора малорастворимой
- Типы электродов и их потенциалы
- Гальванические цепи – химические и концентрационные. Цепи без переноса и с переносом ионов. Расчет ЭДС цепи
- По данным, приведенным в табл. (даны номера вариантов), составьте: а) гальванический элемент, состоящий из двух окислительновосстановительных
- Как протекает электрохимическая коррозия в .......................... среде при контакте металлов ......... и .......... ? Какой из металлов разрушается
- Как будет происходить электролиз водного раствора электролита NaNO3 (t = 45 мин, I = 7 А)? Приведите уравнение диссоциации электролита и поясните
- Электрическая проводимость растворов (удельная, эквивалентная, молярная). Зависимость электрической проводимости
- Закон независимого движения ионов
- К 25,00 см3 раствора KMnO4 с титром, равным 0,003161 г/см3 прибавили кислоту и йодид калия. Выделившейся йод
- Закон независимого движения ионов
- Чему равна молярная концентрация раствора нитрата серебра, если на титрование 25,00 см3 этого раствора пошло
- Имеются результаты измерения роста 100 студентов. Рост (см) 154 – 158 158 – 162 162 – 166 166 – 170 170 – 174 174 – 178 178 – 182 182 – 186 Число студентов 6 18

