
Как будет происходить электролиз водного раствора электролита ZnSO4 (t = 1 ч 15 мин, I = 12 А)? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Как будет происходить электролиз водного раствора электролита ZnSO4 (t = 1 ч 15 мин, I = 12 А)? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях. Составьте электронные уравнения процессов, протекающих на инертных электродах. Вычислите массу (для твердых и жидких) или объем (для газообразных) веществ, образующихся на электродах.
Решение
Электролиз - это окислительно-восстановительная реакция, происходящая на электродах при пропускании электрического тока через расплав или раствор электролита. В таких системах электролиты подвергаются диссоциации – распаду на положительно- (катионы) и отрицательно- (анионы) заряженные ионы. Уравнение диссоциации электролита имеет вид:

При электролизе расплавов веществ на катоде происходит процесс восстановления катионов (процесс присоединения электронов), а на аноде - процесс окисления анионов (процесс отдачи электронов). В результате, как правило, происходит разрядка ионов, т.е. переход их в нейтральное состояние:
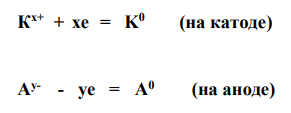
Если электролизу подвергается водный раствор, то необходимо учитывать возможность участия воды как в катодном, так и в анодном процессе.
Преимущественное участие молекул воды в катодном процессе:
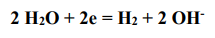
происходит в том случае, если в состав электролита входят катионы электрохимически активных металлов:
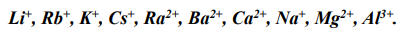
Такие катионы требуют для своей разрядки значительно больше энергии, чем ее затрачивается на выделение водорода из воды, поэтому получить эти металлы электролизом водных растворов их соединений невозможно.
Поскольку в состав электролита, указанного в условии задачи, входят катионы Zn2+, то электронное уравнение катодного процесса имеет вид:
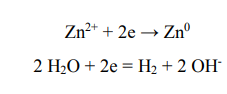
Если в состав электролита входят анионы кислородсодержащих кислот:(NO3 - , NO2 - , SO3 2- , SO4 2- , PO4 3- , CO3 2- и т.п.), а также фторид-анион F- , то по тем же энергетическим причинам в анодном процессе участвуют не анионы электролита, а молекулы воды:
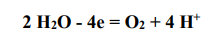
В состав рассматриваемого в задаче электролита входят анионы SO4 2- , поэтому электронное уравнение анодного процесса выглядит следующим образом:
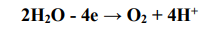
Продуктами данного электролиза являются: - непосредственно выделяющиеся на электродах Zn, H2 и O2, - а также результаты вторичных взаимодействий между ионами, входящими в состав исходного электролита и не принимающие участие в электродных реакциях и ионами, образующимися в результате электродных реакций
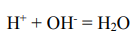
Для вычислений массы m (для газов - объема V) веществ, образующихся на электродах в результате электролиза, необходимо воспользоваться законом Фарадея:

В условии задачи дано: I =12 A, t = 1 ч 15 мин или 4500 сек Первый продукт электролиза H2 является газообразным (твердым, жидким или газообразным) веществом, поэтому для него необходимо вычислить объем (массу или объем). Подставляем в соответствующую формулу необходимые значения: 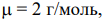 z = 2.
z = 2.
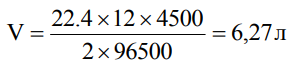
Второй продукт электролиза О2 (формула) является газообразным (твердым, жидким или газообразным) веществом, поэтому для него необходимо вычислить объем (массу или объем). Подставляем в соответствующую формулу необходимые значения: = 32 г/моль, z = 4
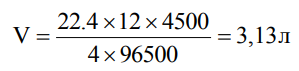
Третий продукт электролиза Zn (формула) является твердым (твердым, жидким или газообразным) веществом, поэтому для него необходимо вычислить массу (массу или объем). Подставляем в соответствующую формулу необходимые значения: = 65 г/моль, z = 2.
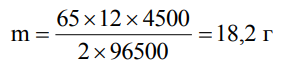

Похожие готовые решения по химии:
- На нейтрализацию 3,28 г основания израсходовано 2,14 г HCl. Вычислите эквивалент основания. Какую массу магния можно окислить этим же количеством кислоты
- Определите скорость химической реакции N2(г) + 3Н2(г) = 2NH3(г) при исходных концентрациях [N2] = 2 моль/л и [H2] = 8 моль/л и в момент времени, когда концентрация азота уменьшилась на 10%
- В сосуде емкостью 10 л установилось равновесие в газовой системе СО + Cl2 ↔ COCl2 + Q. Состав равновесной системы: 11 г СO; 36 г Cl2; 42 г COCl2. Вычислите константу равновесия (КС) и исходные концентрации CO и Cl2. Как изменится численное значение КС при увеличении температуры и почему
- Вычислите концентрацию ионов и их количество, содержащихся в 100 мл 0,01 М раствора HNO2 (КД = 4⋅10–4 ). Запишите уравнение диссоциации и выражение для константы диссоциации, как изменятся значения α и КД HNO2 при уменьшении концентрации раствора
- Необходимо произвести вычисления и найти недостающие величины в водных растворах величины под номером 113
- Степени окисления атомов в простых веществах (построенных из атомов одного и того же элемента) принимаются равными нулю
- Электрохимическая схема - это условная запись, в которой представлена информация о аноде и катоде с указанием металлов, состава электролитов, а также особенностях конструкции данного гальванического элемента
- Объясните механизм защиты подземного стального трубопровода с помощью магниевого протектора, если почвенные воды в данной местности имеют ярко выраженный кислотный характер. Приведите электронные уравнения анодного и катодного процессов
- Рассмотрим модель Лоренца для условной страны. Пусть в этой стране только две группы жителей: «богатые» и «бедные
- Объясните механизм защиты подземного стального трубопровода с помощью магниевого протектора, если почвенные воды в данной местности имеют ярко выраженный кислотный характер. Приведите электронные уравнения анодного и катодного процессов
- В цехе три рабочих за смену (8 ч) произвели 35 деталей А, на которые установлена норма времени 40 мин за единицу, и 60 деталей
- По данным таблицы рассчитать снижение трудоёмкости продукции и рост производительности труда в плановом периоде (в %): Показатели

