
Автор Анна Евкова
Преподаватель который помогает студентам и школьникам в учёбе.
Объясните механизм защиты подземного стального трубопровода с помощью магниевого протектора, если почвенные воды в данной местности имеют ярко выраженный кислотный характер. Приведите электронные уравнения анодного и катодного процессов
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
Описание заказа и 38% решения ( + фото):
Объясните механизм защиты подземного стального трубопровода с помощью магниевого протектора, если почвенные воды в данной местности имеют ярко выраженный кислотный характер. Приведите электронные уравнения анодного и катодного процессов.
Решение
Механизм действия протекторной защиты заключается в превращении всей поверхности защищаемой стальной конструкции в один общий неразрушающийся катод. Анодами при этом будут являться подключенные к защищаемой конструкции электроды из более электроотрицательного металла – магниевые протекторы.
Электродные процессы:
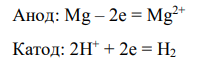

Похожие готовые решения по химии:
- Как будет происходить электролиз водного раствора электролита ZnSO4 (t = 1 ч 15 мин, I = 12 А)? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях
- На нейтрализацию 3,28 г основания израсходовано 2,14 г HCl. Вычислите эквивалент основания. Какую массу магния можно окислить этим же количеством кислоты
- Определите скорость химической реакции N2(г) + 3Н2(г) = 2NH3(г) при исходных концентрациях [N2] = 2 моль/л и [H2] = 8 моль/л и в момент времени, когда концентрация азота уменьшилась на 10%
- В сосуде емкостью 10 л установилось равновесие в газовой системе СО + Cl2 ↔ COCl2 + Q. Состав равновесной системы: 11 г СO; 36 г Cl2; 42 г COCl2. Вычислите константу равновесия (КС) и исходные концентрации CO и Cl2. Как изменится численное значение КС при увеличении температуры и почему
- Большинство химических реакций являются обратимыми: одновременно с прямой реакций протекает обратная. В момент выравнивания скоростей прямой и обратной реакций в системе наступает состояние химического равновесия
- Необходимо произвести вычисления и найти недостающие величины в водных растворах величины под номером 113
- Степени окисления атомов в простых веществах (построенных из атомов одного и того же элемента) принимаются равными нулю
- Электрохимическая схема - это условная запись, в которой представлена информация о аноде и катоде с указанием металлов, состава электролитов, а также особенностях конструкции данного гальванического элемента
- Кривая спроса на продукцию монополиста задана как Р = 30 - 0,2Q, где Q — количество товара, продаваемого за год; Р — цена товара
- Электрохимическая схема - это условная запись, в которой представлена информация о аноде и катоде с указанием металлов, состава электролитов, а также особенностях конструкции данного гальванического элемента
- Как будет происходить электролиз водного раствора электролита ZnSO4 (t = 1 ч 15 мин, I = 12 А)? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях
- Рассмотрим модель Лоренца для условной страны. Пусть в этой стране только две группы жителей: «богатые» и «бедные

