
В чем различия в коррозии оцинкованного и луженого железа при нарушении целостности покрытий во влажной атмосфере? Приведите электронные уравнения анодного и катодного процессов в обоих случаях. Укажите продукты коррозии
 |
 |
Химия |
 |
 |
Решение задачи |
 |
 |
|
 |
 |
Выполнен, номер заказа №17022 |
 |
 |
Прошла проверку преподавателем МГУ |
 |
 |
|
Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! |
|
Закажите у меня новую работу, просто написав мне в чат! |
В чем различия в коррозии оцинкованного и луженого железа при нарушении целостности покрытий во влажной атмосфере? Приведите электронные уравнения анодного и катодного процессов в обоих случаях. Укажите продукты коррозии.
Решение
Электрохимическая коррозия металлов происходит в среде электролита (растворы кислот, щелочей, солей, влажный воздух) и может быть представлена как совокупность анодного (окисление) и катодного (восстановление) процессов. При контакте металлов разной электрохимической активности коррозионному разрушению в первую очередь подвергается металл с наиболее отрицательной величиной электродного потенциала E0 .
При этом такой металл выполняет функции анода в электрохимической системе и окисляется.
Электронное уравнение анодного процесса можно представить в общем виде:
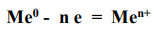
Рассмотрим железную пластину, покрытую оловом.
Из двух металлов анодом является Fe, т.к. его электродный потенциал (E0 = -0,44 В) является величиной более отрицательной, чем электродный потенциал Sn (Е0 = -0,14 В). Следовательно, в данном случае коррозионному разрушению будет подвергаться железная пластина. Анодный процесс имеет вид:
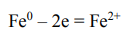
В катодном процессе при электрохимической коррозии участвуют частицы-окислители, находящиеся в электролите:

Продукты коррозии определяются результатами анодного и катодного процессов:
- в кислой среде выделяется газообразный водород и образуется соль металла-анода и кислоты, создающей среду;
- в нейтральной среде продуктом коррозии является гидроксид металлаанода (как результат взаимодействия катионов металла-анода и гидроксидионов, образующихся на катоде).
Во влажной среде протекает превращение:
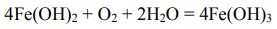
В рассматриваемой в задаче системе продуктами коррозии являются: Fe(OH)3. Рассмотрим железную пластину, покрытую цинком
Из двух металлов анодом является Zn, т.к. его электродный потенциал (E0 = -0,76 В) является величиной более отрицательной, чем электродный потенциал Fe (Е0 = -0,44 В). Следовательно, в данном случае коррозионному разрушению будет подвергаться цинк. Анодный процесс имеет вид:


Похожие готовые решения по химии:
- Как будет происходить электролиз водного раствора электролита NaCl (t = 25 мин, I = 8 А)? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях
- Следовательно, заряд ядра атома есть суммарный заряд его протонов (нейтроны заряда не несут), а массовое число – суммарная масса протонов и нейтронов
- Охарактеризуйте валентные состояния атомов данного элемента в основном и возбужденных состояниях с помощью электронно-графических формул
- Определите тип химической связи (неполярная ковалентная, полярная ковалентная или ионная) в веществах нитрид лития и дихлорид серы
- Укажите соответствие между положением элемента в периодической системе Д.И. Менделеева и его электронной формулой (номером внешнего энергетического уровня, общим числом валентных электронов, характером их распределения по энергетическим подуровням
- Электроотрицательность (EN) характеризует способность атомов элементов к смещению электронной плотности. В периоде системы элементов Д. И. Менделеева она возрастает слева направо, в подгруппе убывает сверху вниз (для s- и p-элементов
- Атомы элементов P в первой реакции и O во второй реакции (а также и вещества, в состав которых они входят PH3 в первой реакции и KClO3 во второй реакции) являются восстановителями (отдают электроны) и участвуют в процессе окисления (процессе отдачи электронов
- Катодный процесс заключается в восстановлении катионов, входящих в состав соли – электролита катода
- Катодный процесс заключается в восстановлении катионов, входящих в состав соли – электролита катода
- Атомы элементов P в первой реакции и O во второй реакции (а также и вещества, в состав которых они входят PH3 в первой реакции и KClO3 во второй реакции) являются восстановителями (отдают электроны) и участвуют в процессе окисления (процессе отдачи электронов
- Проведя статистический анализ деятельности компании, экономисты вывели следующие уравнения регрессии, увязывающие показатели баланса и отчета о прибылях и убытках
- Как будет происходить электролиз водного раствора электролита NaCl (t = 25 мин, I = 8 А)? Приведите уравнение диссоциации электролита и поясните возможность участия каждого из образующихся ионов в электродных реакциях

